PNAS:解答10年谜题:eIF4E蛋白与癌症
2013-08-22 koo bio360
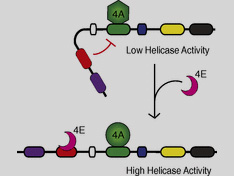
很久以前研究人员就已经知道,人类细胞中一种特异的蛋白质高水平与肿瘤生长相关,但却对这一具体机制却不是很清楚。 现在,来自加州大学戴维斯分校生命科学学院的研究人员取得了一项突破性的发现,他们阐明了真核起始因子 4E(eukaryotic initiation factor 4E, eIF4E )蛋白对促癌信使 RNA 分子起作用的机制。当翻译之时,这类 mRNA 可以触发失控性
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#PNAS#
73
谢谢分享!
53