Lancet Oncol:围手术期大剂量甲氨蝶呤、长春碱、阿霉素和顺铂治疗肌层浸润性膀胱癌(VESPER):一项开放标签、随机、3期研究中5年的生存终点
2024-01-22 daikun MedSci原创 发表于上海
该研究旨在比较密集型甲氨蝶呤、长春碱、多柔比星和顺铂(dd-MVAC)与吉西他滨和顺铂(GC)在肌层浸润性膀胱癌患者围手术期化疗中的疗效,该研究支持dd-MVAC方案作为新辅助化疗。
肌层浸润性膀胱癌的标准治疗包括新辅助化疗和根治性膀胱切除术,但最佳化疗方案仍有争议。过去十年的回顾性研究或早期前瞻性研究报道了dd-MVAC和GC的疗效,但没有随机对照试验。近期发表在《The Lancet Oncology》上的一篇文章报道了一项名为VESPER的III期随机对照研究,旨在比较密集型甲氨蝶呤、长春碱、多柔比星和顺铂(dd-MVAC)与吉西他滨和顺铂(GC)在肌层浸润性膀胱癌患者围手术期化疗中的疗效。

方法:该试验设计为开放标签、随机对照III期试验。入组对象为18-80岁肌层浸润性膀胱癌患者。患者被随机分为dd-MVAC组(每2周1个周期,共6个周期)和GC组(每3周1个周期,共4个周期)。主要研究终点为3年无进展生存率,次要终点包括化疗毒性、病理反应率、总生存率、膀胱癌特异性生存期等。该研究报道的是5年随访期的总生存率和无进展生存率。
1.人群和基线特征
研究对象为肌层浸润性膀胱癌患者,年龄在18-80岁之间。总体人群:500例患者,其中90%为男性,中位年龄63岁。新辅助化疗亚组:437例患者,占89%,其中男性占90%,中位年龄63岁。辅助化疗亚组:56例患者,占11%,其中男性占87%,中位年龄61岁。dd-MVAC组和GC组在人口统计学和临床特征上分布相似。根据T、N、M分期,患者的临床T分期在T2-T4a之间,N分期为N0,M分期为M0。入组标准包括初发膀胱癌、病理证实为肌层浸润性尿路上皮癌,以及未接受过化疗的患者。入组对象被随机分配到dd-MVAC组或GC组。由于该研究入组的是初治膀胱癌患者,而非晚期膀胱癌,因此对新辅助化疗的效果进行了研究。
2.疗效分析
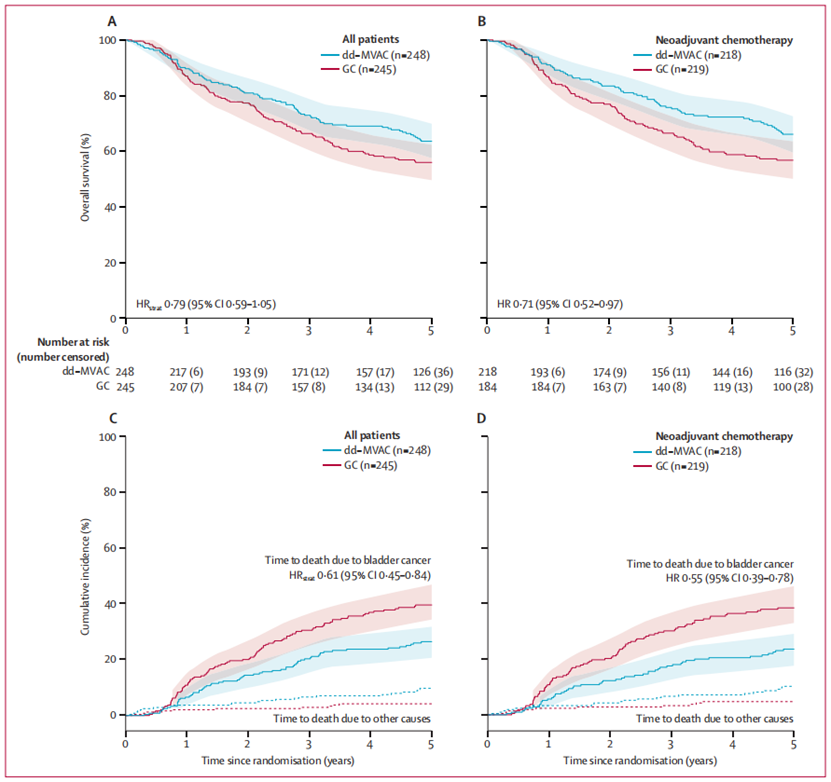
VESPER试验中,dd-MVAC组和GC组的3年PFS无显著差异。在围手术期整体人群中,HRstrat为0.78 (95% CI 0.59-1.02)。在围手术期整体人群中,dd-MVAC组和GC组的5年OS无显著差异,HRstrat为0.79 (95% CI 0.59-1.05)。dd-MVAC组与GC组相比,5年因膀胱癌死亡累积发病率较低(27% vs 40%, HRstrat 0.61, 95% CI 0.45-0.84)。在术前化疗亚组中,dd-MVAC组与GC组相比,5年OS改善(66% vs 57%, HR 0.71, 95% CI 0.52-0.97),5年因膀胱癌死亡累积发病率也较低(24% vs 38%, HR 0.55, 95% CI 0.39-0.78)。在术后化疗亚组中,由于样本量较小,两组的疗效差异未达到统计学显著水平。在围手术期整体人群中,dd-MVAC组和GC组的5年PFS无显著差异,HRstrat为0.78 (95% CI 0.59-1.02)。在术前化疗亚组中,dd-MVAC组的5年PFS优于GC组,HR为0.74 (95% CI 0.55-0.99)。
3.安全性分析
在dd-MVAC组中,出现了4例死亡病例,均为化疗毒性相关。其中3例死亡原因为突然死亡、肺栓塞和脓毒症。在GC组中,也出现了1例死亡病例,原因为突然死亡。DD-MVAC组化疗毒性较重,包括乏力、贫血、发热性中性粒细胞减少、胃肠道反应等,但90%以上患者完成了dd-MVAC方案。GC组化疗毒性较轻。术后并发症两组相当,DD-MVAC组为7%,GC组为10%。肾功能损害导致化疗剂量减少。肌层浸润性膀胱癌化疗毒性仍然存在,需要进一步优化化疗方案。
结论
在围手术期总体人群中,两组的总生存率相当,而dd-MVAC组无进展生存期较长。在新辅助化疗亚组中,dd-MVAC组的总生存率和无进展生存期均优于GC组。在辅助化疗亚组中,由于样本量较小,两组的疗效差异未达到统计学显著水平。死亡原因主要为膀胱癌进展,其他原因包括心血管事件、化疗毒性等。dd-MVAC组化疗毒性较重,但可接受。该研究支持dd-MVAC方案作为新辅助化疗,但对辅助化疗的疗效仍需进一步研究。化疗毒性仍然需要优化。
原始出处
Pfister C, et al. 2023. Perioperative dose-dense methotrexate, vinblastine, doxorubicin, and cisplatin in muscle-invasive bladder cancer (VESPER): survival endpoints at 5 years in an open-label, randomised, phase 3 study. The Lancet Oncology.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#围手术期# #肌层浸润性膀胱癌# #3期研究#
44