中科院长春应化所金永东/齐国华《自然·通讯》:可穿戴电刺激增强型光热贴片用于皮肤肿瘤治疗
2024-01-27 BioMed科技 BioMed科技 发表于陕西省
系统性的细胞研究揭示了eT-patch在PES治疗下的抗肿瘤机制,发现eT-patch在PES治疗下可以协同触发癌细胞凋亡和焦亡,共同导致黑色素瘤细胞死亡。
一种可穿戴的生物贴片,能够在不影响日常活动的情况下,对光和电产生多重响应,对于皮肤癌治疗来说是非常理想的,但仍然是一个关键挑战。在这里,中科院长春应化所金永东/齐国华开发并应用了一种皮肤可穿戴的电刺激增强型光热贴片(eT-patch),该贴片由掺杂MXene(Ti3C2Tx)的透明离子凝胶组成,用于在0.5 W/cm2的光刺激下治疗黑色素瘤。设计的eT-patch由于离子凝胶中掺杂了MXene,提供了高光热转换效率和电导率作为介质,因此具有优越的光热和电学特性。同时,基于离子凝胶的eT-patch具有出色的光学透明度,实现了在光热和电刺激(PES)联合治疗下对皮肤反应和黑色素瘤治疗过程的实时观察。系统性的细胞研究揭示了eT-patch在PES治疗下的抗肿瘤机制,发现eT-patch在PES治疗下可以协同触发癌细胞凋亡和焦亡,共同导致黑色素瘤细胞死亡。由于在健康器官中相对安全且副作用较少,开发的eT-patch为皮肤肿瘤提供了一个有前景的、成本效益高的治疗策略,并为离子凝胶在生物医学应用中的新途径铺平了道路。该研究以题为“A wearable electrostimulation-augmented ionic-gel photothermal patch doped with MXene for skin tumor treatment”的论文发表在《Nature Communications》上。

图1展示了基于离子凝胶的eT-patch用于皮下肿瘤治疗的示意图。该示意图描绘了生物eT-patch是如何从掺杂MXene的离子凝胶制备而来,并应用于皮肤肿瘤治疗的。在协同光热和电刺激下,eT-patch能够实现对肿瘤的有效治疗。研究结果表明,eT-patch在光热和电刺激联合治疗(PES)下,能够显著抑制肿瘤生长,并且通过细胞水平的抗肿瘤机制研究,揭示了eT-patch在PES治疗下能够触发肿瘤细胞的凋亡和焦亡,这两种细胞死亡方式共同导致了黑色素瘤细胞的死亡。这些发现为开发新型的、非侵入性的皮肤肿瘤治疗方法提供了新的视角,并展示了离子凝胶在生物医学应用中的潜力。
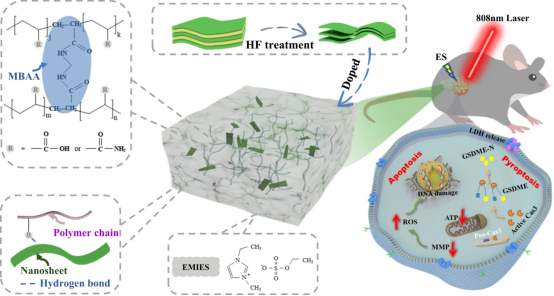
图1.用于皮下肿瘤治疗的基于离子凝胶的eT-patch
【eT-patch的制备和表征】
图2展示了MXene纳米片的微观结构和光学性质,以及它们在离子凝胶中的分散情况。首先,通过透射电子显微镜(TEM)和扫描电子显微镜(SEM)成像,观察到了Ti3C2Tx纳米片的超薄二维层状结构,并通过原子力显微镜(AFM)测量确认了纳米片的厚度约为2纳米。X射线衍射(XRD)分析显示了Ti3C2Tx纳米片的晶体结构,以及通过X射线光电子能谱(XPS)分析确认了纳米片表面的化学成分,包括Ti-C键和Ti2+、Ti3+的氧化态。此外,UV-Vis吸收光谱揭示了Ti3C2Tx纳米片在水溶液中的吸收特性,特别是在768纳米处的吸收峰,这对于后续的光热治疗至关重要。这些结果表明,MXene纳米片具有良好的分散性和光学性质,能够有效地吸收近红外光并转换为热能,为制备高效的光热治疗贴片提供了基础。
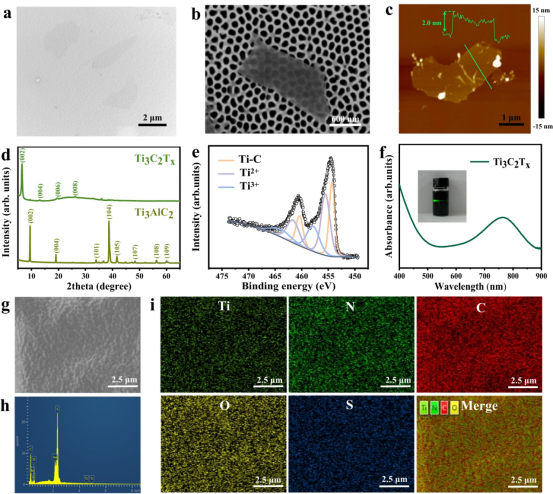
图2. 光热剂MXene和离子凝胶的表征
【eT-patch性能测量】
图3展示了eT-patch的性能测试,包括其机械性能、热稳定性和电学特性。通过拉伸测试,观察到eT-patch在不同MXene掺杂浓度下的应力-应变曲线,发现随着MXene含量的增加,贴片的断裂伸长率和韧性得到显著提升。在808纳米激光照射下,eT-patch的循环温度曲线显示了其在连续光照下的热稳定性,即使经过五次10分钟的激光照射,贴片的温度变化仍然保持稳定。此外,通过热成像和温度-时间曲线,证实了eT-patch在激光和电刺激(ES)联合治疗下,其温度随照射时间的延长而显著升高,且贴片内部的温度分布基本均匀。电流-电压(I-V)曲线和电流-时间(I-t)曲线进一步证实了eT-patch即使在扭曲状态下也具有良好的导电性,并且随着MXene掺杂浓度的增加,电流值逐渐增大。这些结果表明,eT-patch不仅在机械和热学性能上表现出色,而且在电学特性上也具有优势,使其成为实现高效光热和电刺激联合治疗的有力工具。
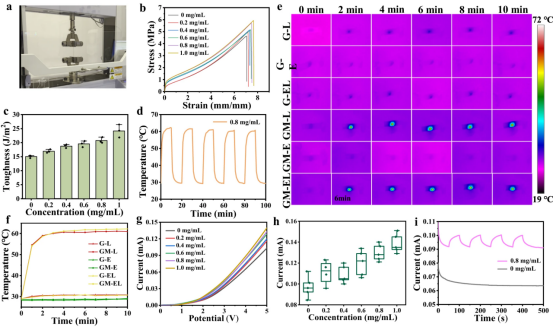
图3.eT-patch性能测量
【PES处理过程中细胞死亡的机制】
图4展示了PES(光电刺激)治疗对B16F10细胞的影响及其诱导细胞死亡的机制。结果表明,PES治疗通过影响细胞的能量代谢和线粒体功能,以及诱导ROS产生,有效地促进了肿瘤细胞的死亡,为皮肤肿瘤治疗提供了一种新的治疗策略。
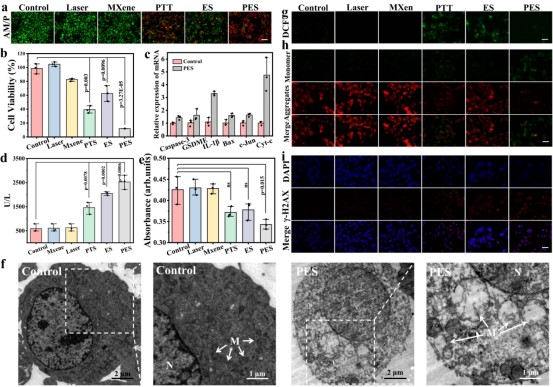
图4. PES诱导细胞死亡的机制研究
【eT-patch治疗黑色素瘤的疗效评价】
图5展示了eT-patch在体内黑色素瘤模型治疗中的应用及其效果。通过建立B16F10肿瘤携带的C57BL/6J小鼠模型,并将小鼠随机分为五组接受不同治疗(对照、激光、PTT、ES和PES),观察了治疗过程中肿瘤表面温度的变化、肿瘤体积的测量、肿瘤组织的重量和体积、以及治疗后小鼠的体重变化。结果显示,PES治疗组在15天后显示出最显著的肿瘤抑制效果,肿瘤体积和重量均有所减少,且小鼠体重保持稳定,表明治疗具有较低的系统毒性。此外,通过组织学和免疫荧光染色分析,PES治疗组显示出最明显的肿瘤损伤和增殖抑制。这些结果证实了eT-patch在体内治疗黑色素瘤的有效性,并且具有较高的生物安全性和稳定性,为开发非侵入性的皮肤肿瘤治疗方法提供了新的希望。

图5. 黑色素瘤模型的体内治疗
【小结】
该研究开发了一种可穿戴的电刺激增强型光热贴片(eT-patch),该贴片由掺杂MXene的透明离子凝胶组成,用于通过光热和电刺激(PES)联合治疗高效治疗黑色素瘤。eT-patch具有良好的透明度,可以实现对皮肤反应和治疗过程的实时观察。研究揭示了PES治疗的细胞机制,表明eT-patch在PES治疗下能够触发癌细胞的凋亡和焦亡,这两种细胞死亡方式共同促进了抗肿瘤效果。由于eT-patch在健康器官中表现出相对安全且副作用较少的特性,它为皮肤肿瘤治疗提供了一种有前景的、成本效益高的治疗策略,并为离子凝胶在生物医学领域的应用开辟了新途径。
原文链接:
https://www.nature.com/articles/s41467-024-45070-z
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















学习学习!!!!!!!!
0
#电刺激# #皮肤肿瘤# #光热贴片#
99