JCO:HER2+/HR+乳腺癌新辅助治疗∣高颜值T-DM1能否替代化疗?
2017-07-16 wrangx 肿瘤资讯
乳腺癌新辅助治疗“降阶梯策略”即无化疗方式可行吗?来自德国研究者选取HER2+/HR+乳腺癌患者,使用T-DM1用于新辅助治疗。该随机、对照的Ⅱ期研究于2017年7月6日在JCO在线发表,含T-DM1无化疗方案pCR率超过40%,使部分患者避免化疗。 背景 HER2+早期乳腺癌(BC)预后差,但是因为标准化疗及1年曲妥珠单抗治愈率较高。曲妥珠单抗联合帕妥珠单抗已批准用于早期BC新辅助治疗,
乳腺癌新辅助治疗“降阶梯策略”即无化疗方式可行吗?来自德国研究者选取HER2+/HR+乳腺癌患者,使用T-DM1用于新辅助治疗。该随机、对照的Ⅱ期研究于2017年7月6日在JCO在线发表,含T-DM1无化疗方案pCR率超过40%,使部分患者避免化疗。
背景
HER2+早期乳腺癌(BC)预后差,但是因为标准化疗及1年曲妥珠单抗治愈率较高。曲妥珠单抗联合帕妥珠单抗已批准用于早期BC新辅助治疗,T-DM1为曲妥珠单抗偶联细胞毒药物DM1,是HER2+治疗又一选择。3期EMILIA试验与标准二线方案卡培他滨联合拉帕替尼比较后,T-DM1批准用于转移性BC二线治疗。3期MARIANNE试验一线治疗转移性BC,T-DM1联合帕妥珠单抗在PFS非劣效与曲妥珠单抗联合多西他赛,但T-DM1组3级以上毒性发生率低且维持健康QOL时间更长。
在晚期BC中,T-DM1与紫杉联合曲妥珠单抗疗效类似,但T-DM1毒性更低,特别是不可逆的多发神经病,因此T-DM1成为BC新辅助治疗候选药物。西德研究组(WSG)针对HER2+/HR+早期BC开展新辅助治疗试验,比较T-DM1±内分泌治疗(ET)和曲妥珠单抗+ET。
方法
前瞻性、随机、多中心、Ⅱ期研究。纳入≥18岁、早期无转移BC、ER和/或PR+(≥1%)、HER2+、PS评分≤1分(或KPS评分≤80分)。
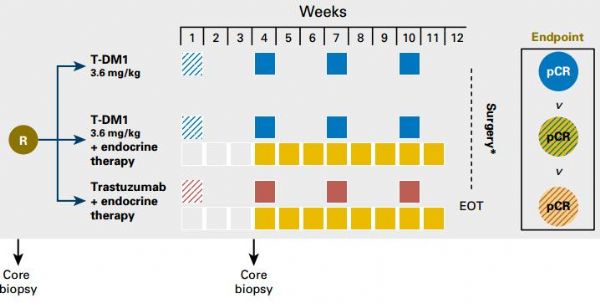
研究分组见上图。1:1:1分入T-DM1组(3.6 mg/kg三周一次,共4周期)、T-DM1+ET组、曲妥珠单抗+ET组。ET绝经前使用三苯氧胺,绝经后使用芳香化酶抑制剂,绝经前允许使用GnRH-A类药物。新辅助治疗结束后3周内手术,术后进行标准辅助治疗。早期反应指标较基线,治疗后3周Ki67下降≥30%或细胞缓解。
首要研究终点pCR率(ypT0/is/ypN0),次要终点安全性、早期反应对pCR率的预测。
结果
1. 基本特点 2012年10月至2015年3月,48个中心筛选患者463例,最终随机375例。T-DM1组119例、T-DM1+ET组127例、曲妥珠单抗+ET组129例,三组新辅助治疗完成率98.3%、94.5%和90.7%;三组中位年龄分别为50岁、51岁和51.5岁;三组cT1期分别为50.4%、48.8%和46.5%;三组cN0期分别为71.4%, 75.6%和70.5%;三组PR阴性分别为17.6%、15.7%和16.3%。
2. pCR率 手术切除359例 ,占95.7%。T-DM1组pCR率41.0%,T-DM1+ET组pCR率41.5%,曲妥珠单抗+ET组pCR率15.1%。T-DM1±ET组较曲妥珠单抗+ET组pCR率明显增加(两者P<.001)。T-DM1组、T-DM1+ET组、曲妥珠单抗+ET组接近pCR(ypT1a 或ypT0/is)分别为52.9%、52.9%和19.3%。T-DM1组绝经后和绝经前pCR率分别为44.1%和37.9%,T-DM1±ET组绝经后和绝经前pCR率分别为45.0%和38.1%,曲妥珠单抗+ET组绝经后和绝经前pCR率分别为16.7% 和13.6%。尽管绝经后pCR率有所提高,但无统计学差异。早期反应患者pCR率(35.7%,71/199)没有早期无缓解反应患(19.8%,20/101)明显提高,OR值为2.2。
3.安全性 T-DM1增加1~2级毒性,主要是血小板减少、恶心和肝转氨酶升高。3级以上不良事件发生率T-DM1±ET组和曲妥珠单抗+ET组分别为7.5%和4.1%(P = .26)。
结论
针对HER2+/HR+早期乳腺癌,ADAPT试验说明12周T-DM1新辅助治疗(联合或不联合内分泌治疗)pCR率高,使部分患者避免系统化疗。
启示
T-DM1治疗HER2过表达晚期BC表现为低毒高效,是早期BC新辅助治疗理想的选择药物。pCR能作为HER2+/HR+乳腺癌理想替代终点吗?FDA已深入探讨pCR率作为生存替代终点的价值。纳入11955例Meta分析,pCR定义为ypT0/ypN0 或 ypT0/is/ypN0,证明pCR与生存率提高相关,其中,pCR与三阴性BC(EFS,HR0.24)及HER2+/HE阴性BC(HR0.15)长期生存相关性强,且与HER2+/HE阳性pCR与生存显着相关。纳入HER2过表达研究Meta分析(n=5746例),pCR与临床结局关系密切,在非选择HER2+患者HR0.37,HR阴性HR0.29,HR阳性HR0.52,尽管较HER2+/HE阴性,HER2+/HE阳性乳腺癌pCR与生存关系有所下降,但在HER2+新辅助治疗中pCR仍是理想替代终点。
T-DM1新辅助治疗pCR率与历史数据比较如何?本研究含T-DM1新辅助治疗 pCR率超过40%,TRYPHAENA试验评价双靶向抗HER2(帕妥珠单抗+曲妥珠单抗)联合不同化疗药物,在HER2+/HE阳性患者pCR率联合CEF、多西他赛46.2%和48.6%。尽管其他研究中看到更高数值pCR率,但本研究T-DM1方案pCR超过40%,数值高且临床意义较大,因为毒性更低,避免了脱发及外周多发神经病、粒细胞缺乏性发热。
4周期T-DM1新辅助治疗与标准多西他赛联合曲妥珠单抗治疗HER2+/HR+乳腺癌pCR率不分伯仲。T-DM1有效可作为不适合化疗患者选择,另外增加内分泌治疗作用不大。
原始出处:
Nadia Harbeck, Oleg Gluz, et al. De-Escalation Strategies in Human Epidermal Growth Factor Receptor 2 (HER2)–Positive Early Breast Cancer (BC): Final Analysis of the West German Study Group Adjuvant Dynamic Marker-Adjusted Personalized Therapy Trial Optimizing Risk Assessment and Therapy Response Prediction in Early BC HER2- and Hormone Receptor–Positive Phase II Randomized Trial—Efficacy, Safety, and Predictive Markers for 12 Weeks of Neoadjuvant Trastuzumab Emtansine With or Without Endocrine Therapy (ET) Versus Trastuzumab Plus ET. Journal of Clinical Oncology - published online before print July 6, 2017 DOI: 10.1200/JCO.2016.71.9815
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#JCO#
64
#新辅助#
68
很好,不错,以后会多学习
81
继续学习中谢谢
92
学习了,谢谢分享
90
学习了,谢谢
91
值得推荐一下
85
不错的,学习了,谢谢分享!
59
学习了谢谢分享
48
谢谢分享,学习了
49