《自然 · 综述》:免疫细胞,正成为衰老相关疾病的潜在治疗策略
2023-08-15 步步先生 干细胞者说 发表于上海
T细胞功能紊乱造成的免疫耐受下降,可能是老年病的主要原因。因此,基于T细胞免疫疗法的新兴治疗方法,正在成为衰老相关疾病的很有希望的治疗策略。
衰老是一种不可逆转的自然过程,人总是要老的。随着年龄的增长,机体诸多方面出现功能性下降。免疫系统也逐渐被岁月侵蚀,机体面对病原体和癌细胞的反应能力也逐渐减弱。T细胞是免疫系统的重要组成部分,在细胞免疫反应中起着核心作用。
人类很好奇,衰老究竟是如何发生的,这个过程是否可被调控呢?如果T细胞衰老了,那么机体在衰老过程中会发生哪些变化呢?国际顶级期刊 Nature Reviews Immunology 杂志上发表一篇题为“The role of T cells in age-related diseases”的综述文章。今天,我们试着解读一下。
T细胞衰老与机体衰老
衰老相关疾病通常表现为持续的炎症反应,最终导致组织内稳态的破坏。生物学家Elie Metchnikoff ,对,就是巨噬细胞的发现者,在一个多世纪前就曾提出,由结肠通透性增强引起的慢性炎症,可以影响衰老相关功能障碍。

在这篇综述中,作者讨论了T细胞在衰老相关疾病发挥的作用,比如心血管疾病(包括高血压、动脉粥样硬化和心肌梗死),以及代谢紊乱(如肥胖相关的胰岛素抵抗)。还讨论了T细胞在神经退行性疾病的作用(包括阿尔茨海默病、帕金森病和多发性硬化)。最后,讲述了T细胞在组织修复再生中的作用(屏障维持、损伤修复、组织再生)。
T细胞在衰老中的角色
随着年龄增长,最显著的变化是初始T细胞(Naive T cell,Tn)库的变小和记忆T细胞(Memory T cell,Tm)库的变大,导致可用TCR的数量减少。其主要原因是胸腺退化、初始T细胞的稳态增殖受损以及T细胞耗竭。
在老年人体内,记忆T细胞极度分化,导致CD28和CD27等共刺激分子的不再表达,从而造成T细胞衰老或耗竭。衰老和耗竭的T细胞都显出衰老的分子特征(如线粒体功能障碍和表观遗传重构)。此外,T细胞衰老可显示DNA损伤和短端粒的迹象,并可激活与衰老相关的信号通路。除了共刺激分子表达变低,人类和小鼠体内的衰老T细胞,还表达NK细胞相关标记物(KLRG1, NKG2A, NKG2C和NKG2D)。
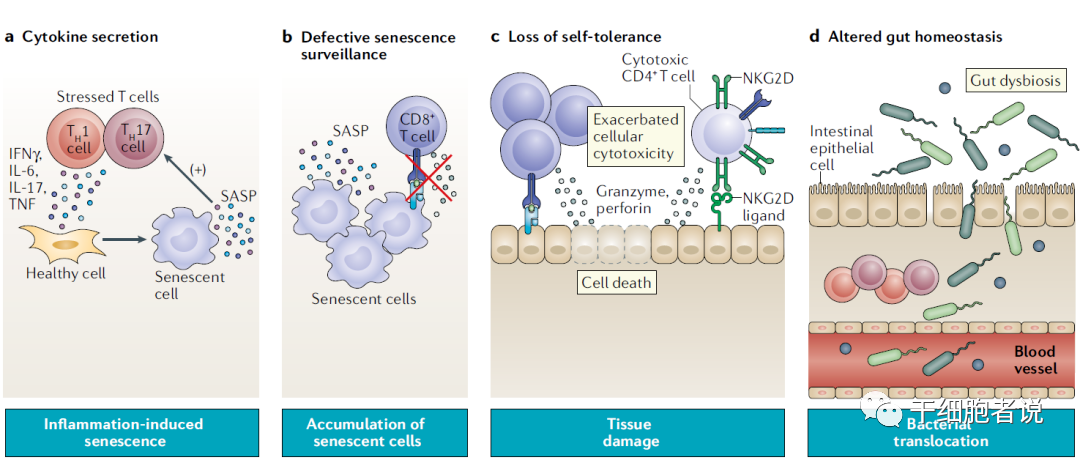
图1:T细胞对炎症和衰老的贡献机制
一句话:T 细胞功能失调,导致炎症和不健康衰老,从而引发各种相关疾病。
心血管疾病中的T细胞
心血管疾病是全球死亡最多的疾病,其引发的疾病包括动脉瘤、心力衰竭、心肌梗死和缺血性卒中等,并且发病率随着年龄增长而显著增加。
在动脉粥样硬化斑块的形成过程中,巨噬细胞可摄取低密度脂蛋白颗粒,同时分泌促炎因子,最终形成斑块的组成成分核心泡沫细胞,这增加了斑块不稳定性。不过,这也有助于免疫细胞(包括T细胞)的进一步招募。在斑块内,浸润的T细胞通过分泌促炎因子(如TNF或IFNγ),或通过抗炎因子(如IL-10)调节巨噬细胞的极化。因此,T细胞可以作为动脉粥样硬化斑块形成和维持的调节因子。
高血压可能也是许多心血管疾病的起点。在血管紧张素II(Angiotensin II)诱导的高血压小鼠模型中,T细胞已经成为血压的调控者。不同的CD4+T细胞亚群会在人类动脉粥样硬化斑块中积累。根据T细胞亚群的不同,它们既可以发挥保护作用,也可以通过变成Th1,促进疾病的进展。
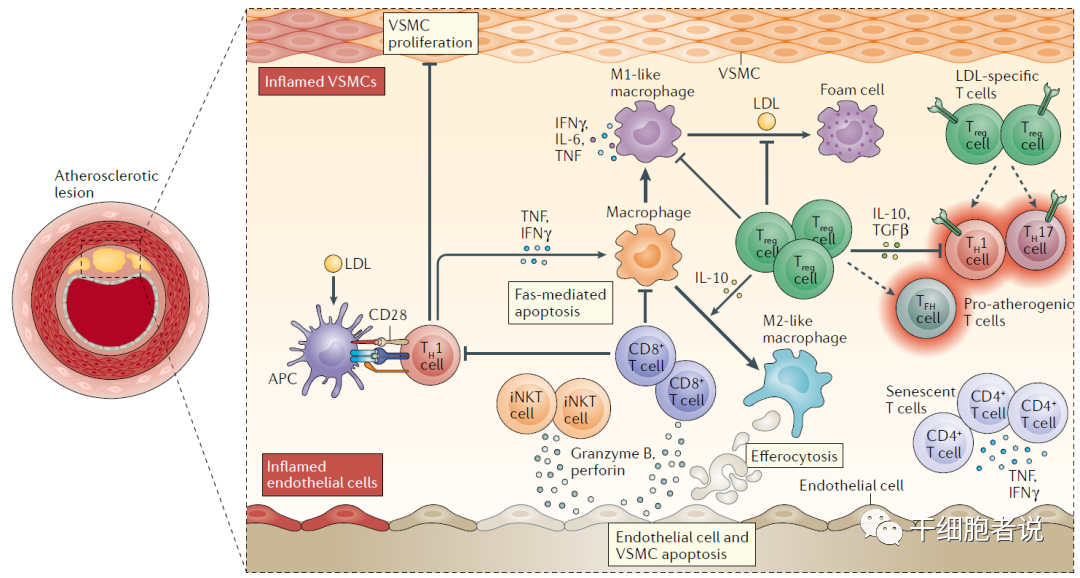
图2:T 细胞对动脉粥样硬化的贡献
一句话:T 细胞亚群众多,是各种心血管疾病的调控者,可促进,也可抑制。
代谢紊乱中的T细胞
随着人体的衰老,肌肉量逐渐减少,而脂肪却在机体中过度沉积。随着科技的发展,体力活动减少,慢性炎症引发的相关疾病越来越常见。脂肪组织中的T细胞会影响衰老相关的代谢紊乱(包括肥胖、2型糖尿病和胰岛素抵抗)。
在老年小鼠中,CD4+T细胞和CD8+T细胞在内脏脂肪组织中聚集起来,并引起肥胖和代谢紊乱。在这种情况下,脂肪组织驻留的T细胞更有可能朝着Th1细胞分化,产生对机体有害的因子IFN-γ。
随着机体衰老,内脏脂肪组织中Th1细胞和Th17细胞增加,这样促使机体逐渐肥胖,从而发生胰岛素抵抗。在发生胰岛素抵抗的小鼠内脏脂肪组织里,会出现大量浸润性CD8+T细胞,这是Th2细胞和Treg细胞减少后伴随发生的结果。Th1和Th17增加引起肥胖相关胰岛素抵抗,Th1细胞主要参与脂肪组织重塑和脂肪分解。与其他组织相比,在脂肪组织中非常规iNKT细胞和γδ T细胞群的出现频率更高。
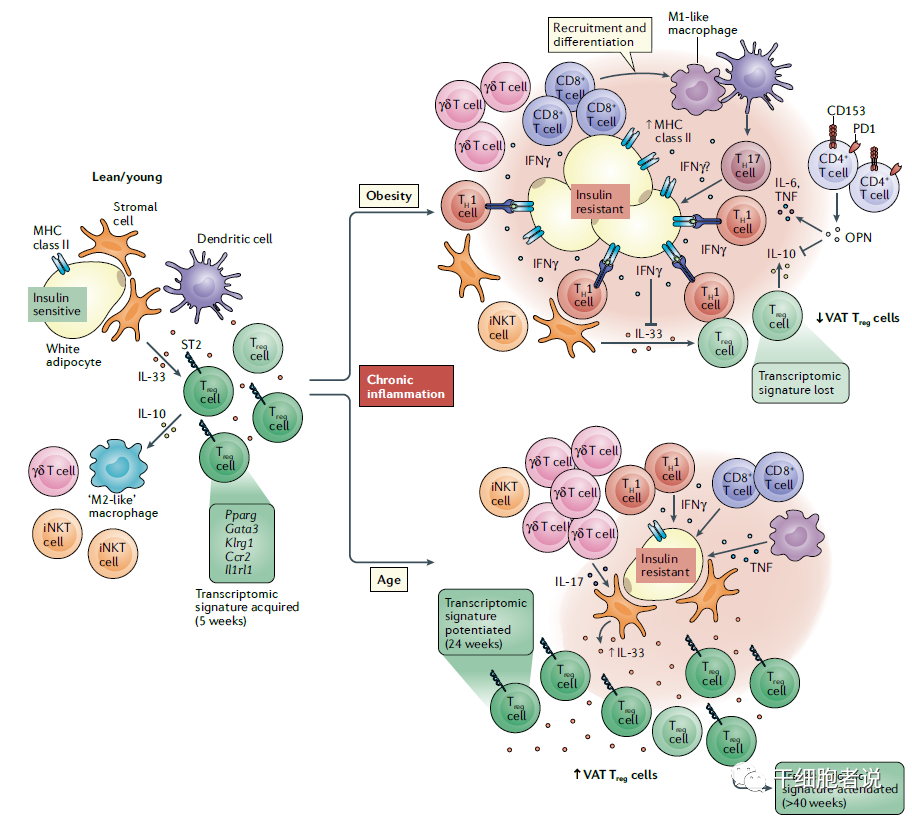
图3. T细胞对肥胖和衰老中脂肪组织的贡献
一句话:慢性炎症引起肥胖,进一步引起机体代谢紊乱。要么限制热量,要么阻断相关代谢通路(二甲双胍、雷帕霉素、NAD+)。
退行性神经病变中的T细胞
由于血脑屏障(BBB)这位大神的存在,神经元不受外界毒素入侵,大脑可以说是与外界环境最为隔绝的器官了。在稳态情况下,外周免疫细胞在大脑中的数量很低,其作用一直被低估。最近研究发现,免疫细胞可能通过脑膜淋巴管进入脑实质,即便在健康的大脑中也如此。
BBB衰竭被认为一种衰老特征,进入老年人大脑中的T细胞可能会增加。在神经退行性疾病中,BBB的破坏在增强。在多发性硬化症(MS)患者中,Th17细胞则直接破坏BBB,并通过IL-17和IL-22信号介导的机制浸润中枢神经系统。在神经功能受损的病理条件下,大脑中的T细胞可直接发挥作用。
因此,代谢应激环境中,具有促炎作用的T细胞可影响认知和协调能力。
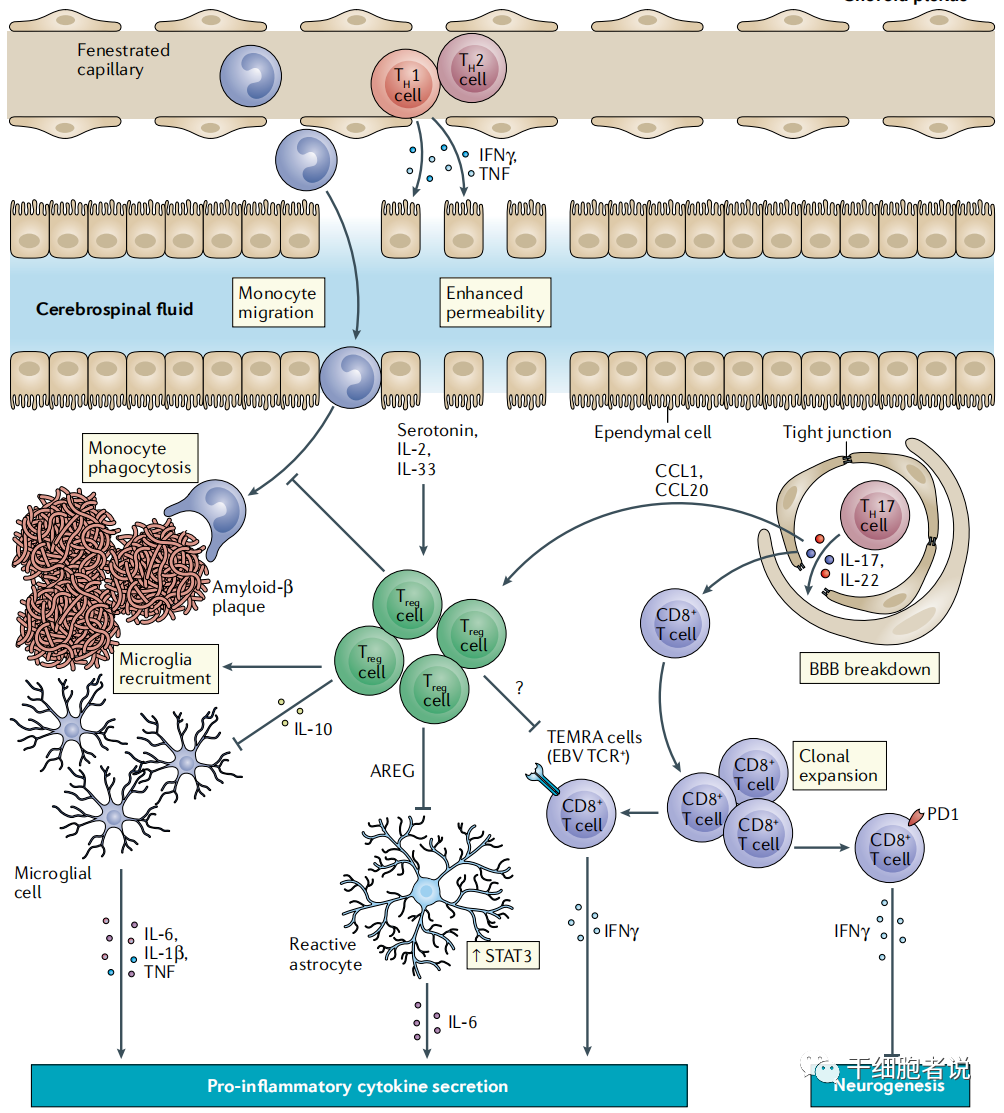
图4. T细胞对衰老相关的神经系统疾病的贡献
一句话:在阿尔茨海默病、帕金森病和缺血性中风等疾病中,T细胞水平或功能的改变可能导致老年人认知的改变。
组织修复再生中的T细胞
在屏障组织损伤后,T细胞可促进组织内稳态的恢复和组织再生。在这种情况下,如果衰老T细胞数量和功能发生改变,可能影响组织再生不良。
▉ T细胞与屏障组织维持
屏障组织的免疫反应,一要防止被破坏,二要确保共生微生物和无害抗原的耐受性。与屏障组织的维持相关的T细胞亚群,主要是γδT细胞。γδT细胞在屏障组织中大量存在,可产生大量生长因子(如KGF和IGF-1),用以调节组织内稳态并促进上皮细胞增殖。肠道中γδT细胞,还可通过分泌细胞因子(如TGF-β1、TGF-β3和Tβ4),维持肠道上皮完整性。在老年小鼠肠道中,γδT细胞比例和抗炎细胞因子的水平比较低。
Th17细胞和促炎反应,也有助于维持肠道组织的完整性,但需通过IL-33严格调节。人类的皮肤中在稳态条件下,CD8+CTL细胞(分泌IL-17或IFN-γ)会积累,这表明该T细胞亚群维持组织稳态。
▉ T细胞与组织损伤修复
当组织损伤后,γδT细胞通过分泌生长因子(比如KGF和IGF1等),减少皮肤组织损伤,促进伤口愈合。在老年患者和糖尿病患者中,αβT细胞和γδT细胞功能受损。T细胞参与多种组织的修复和维持过程(包括皮肤愈合、骨骼肌保护或肺上皮细胞增殖)。T细胞通过分泌表皮生长因子(KGF)诱导上皮细胞增殖,促进损伤后的肺修复。
CD8+T细胞主要分泌IL-17,可加速皮肤伤口愈合。在老年人身上,这种T细胞反应发生下降,并导致伤口愈合受损。衰老可加速循环CD8+T细胞积累,而这些细胞表现出高度的细胞毒性衰老表型,导致人类皮肤病变。
关于骨再生,老年人骨折愈合率较低。在人类外周血单个核细胞(PBMC)移植和后续截骨术的人源化小鼠模型中进行的研究表明,用较高比例的终末分化TEMRA细胞重建的小鼠术后骨体积分数和骨密度降低。这支持更原始T细胞群对于骨愈合能力的重要性。
▉ T细胞调控组织再生
干细胞自我更新和分化的平衡,对维持组织内环境稳态至关重要,并且受细胞因子的调控。在自我更新周期短的组织中,T细胞亚群对干细胞功能的贡献尤为重要。皮肤里的Treg细胞,可促进毛囊干细胞增殖。Th1细胞和Treg细胞之间的微调,在肌肉再生的不同阶段是必需的,促炎因子可促进肌肉干细胞的增殖。抗炎因子(IL-10等)可维持小肠上皮完整性和促进肠道干细胞(ISC)自我更新,而促炎因子可诱导肠道干细胞分化,并可能导致肠道屏障破坏。因此,过度的促炎症环境可能导致干细胞耗竭,这可能导致肠道结构和功能发生衰老。
肠道菌群调节与T细胞
肠道菌群的失调与慢性炎症有关。T细胞在调控肠道干细胞命运和维持肠道完整性中,起着主要作用。T细胞控制肠道菌群的能力,肠道菌群与T细胞的相互作用,已成为衰老相关疾病的一个重要的治疗方向。
T细胞促进生发中心局部的IgA反应,从而保证对共生肠道菌群的耐受,不会引发自身免疫病。初步看来,生发中心的应答需要Th17和Treg两种细胞保持平衡,它们未来分别分化为Tfh细胞和T滤泡调节细胞。iNKT细胞也可通过调节肠道菌群来控制IgA,还可调节肠道Treg细胞的功能。
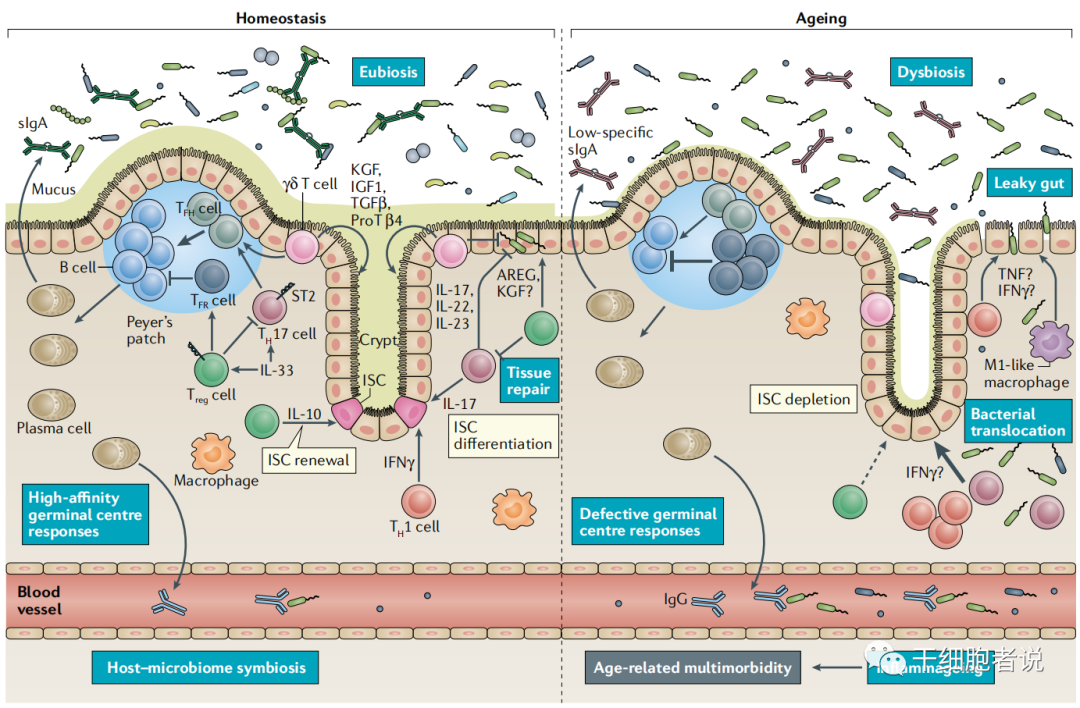
图5. 衰老过程中, T细胞对肠道稳态的贡献
一句话:正常的T细胞可维持肠道菌群的正常,而失调的T细胞可导致肠道菌群失调,可能形成与衰老相关的慢性炎症。
T细胞免疫治疗
靶向致病性T细胞的策略,可能为衰老相关疾病开辟一条新的治疗途径。从使用广泛的免疫抑制药物,到使用抗CD3+抗体直接靶向T细胞,甚至可选择性地去除致病性、高度激活或衰老的T细胞。一方面,CD153+抗原疫苗是一种长期有效方法,在预防脂肪组织中衰老T细胞积累,改善肥胖症状方面。另一方面,我们也可以通过使用CAR-T细胞,特异性地识别和清除衰老细胞。
此外,我们还可通过小分子或饮食调节治疗代谢紊乱、自身免疫病或炎性疾病。这种方法是否对衰老有关的疾病也有用,也可进一步研究。此外,二甲双胍治疗可诱导CD4+T细胞自噬,并促使炎症向非炎症状态转变,抑制Th17的分化。雷帕霉素(一种mTOR抑制剂)可对T细胞进行免疫调节,抑制Th1细胞、Th2细胞和T17细胞分化,同时促进T细胞分化。NAD+可以改善耗竭T细胞的线粒体代谢,抑制炎症的发生。
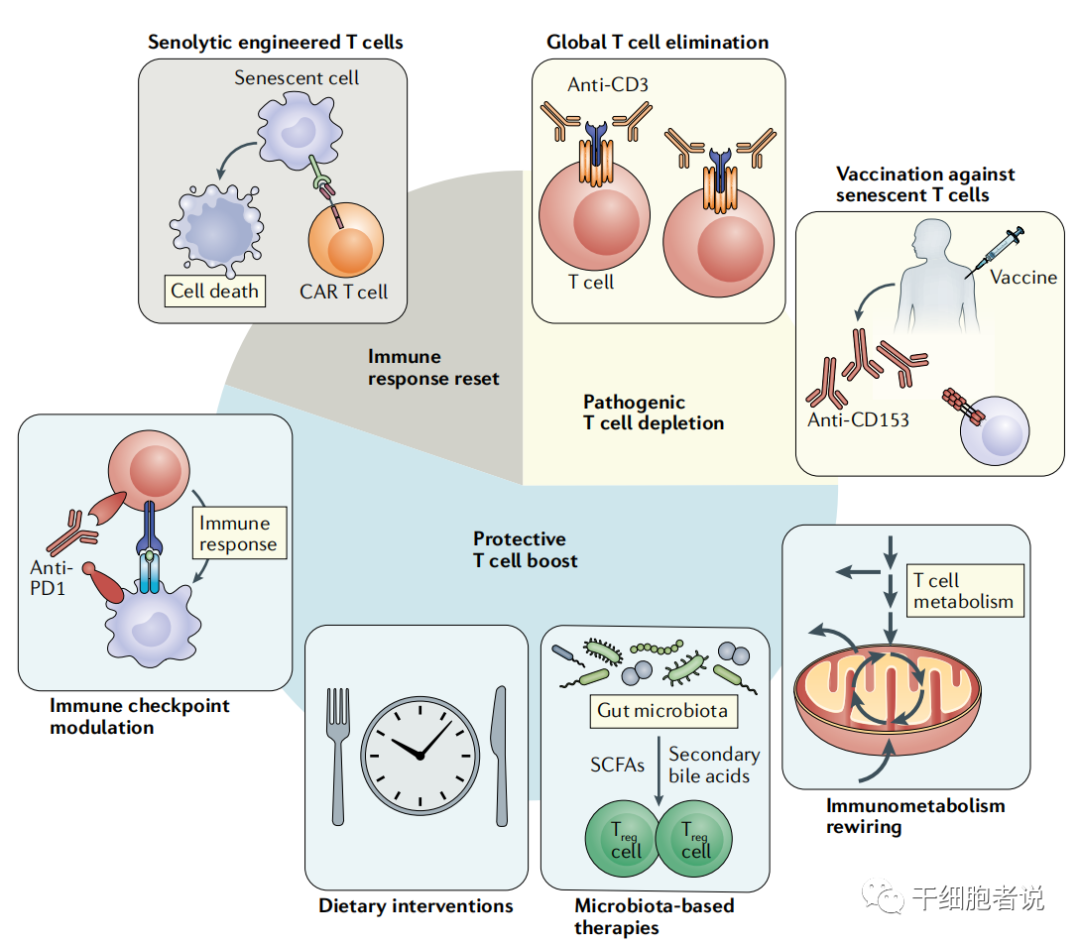
图6. 靶向T细胞的抗衰老大全
一句话:靶向T细胞疗法抗衰老大全:一是清除T细胞(比如CAR-T疗法);二是延缓衰老相关疾病发生(比如CD153疫苗、CD3单抗);三是保持T细胞的战斗力(比如热量限制方法,肠道菌群,PD-1抗体,二甲双胍、雷帕霉素、NAD+等等)。
文末小结
T细胞可调节炎症和驱动衰老,在衰老相关疾病的起着关键作用。促炎T细胞亚群(如Th1细胞和Th17细胞),通常会促进机体衰老;而Treg细胞更有可能抑制炎症反应,返老还童。然而,某些T细胞亚群可能严重依赖于微环境或所处的组织。这些不同T细胞亚群作用相互形成的平衡,将决定最终结果。
在衰老过程中,衰老的T细胞是细胞毒性和持续促炎因子产生的主要驱动因素,可促进衰老细胞的积累,最终造成组织和器官衰竭。T细胞代谢失衡是驱动衰老相关疾病的调控者。
总的来说,T细胞功能紊乱造成的免疫耐受下降,可能是老年病的主要原因。因此,基于T细胞免疫疗法的新兴治疗方法,正在成为衰老相关疾病的很有希望的治疗策略。
原文链接:
https://www.nature.com/articles/s41586-021-03531-1
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












The role of T cells in age-related diseases https://www.nature.com/articles/s41586-021-03531-1
65