Nature Commun:线粒体自噬途径相关的帕金森病潜在治疗靶标
2022-12-23 brainnew神内神外 brainnew神内神外 发表于安徽省
线粒体自噬是细胞清除体内损伤线粒体和维持自身稳态的一种重要调节机制 Parkin所介导的线粒体自噬途径可从细胞中除去受损线粒体。
导读:
线粒体自噬(mitophagy)是细胞清除体内损伤线粒体和维持自身稳态的一种重要调节机制, Parkin所介导的线粒体自噬途径可从细胞中除去受损线粒体,该通路异常可导致受损线粒体日益积累,最终导致多巴胺能神经元的死亡,有早发性帕金森病(PD)的发生机制之一,但是其具体的机制以及以其作为靶点的相关研究尚未阐明。近日,多伦多大学G. Angus McQuibban研究团队在《Nature Communication》( IF=12.121 ) 期刊发表了题为“ROCK inhibitors upregulate the neuroprotective Parkin-mediated mitophagy pathway”的研究论文,报道了ROCK可以作为Parkin介导的线粒体自噬通路的分子开关,应用ROCK抑制剂可增强Parkin介导的线粒体自噬,从而改善体内PD的相关表型,有望被开发用于靶向治疗帕金森病。
 几种ROCK抑制剂增加Parkin募集到受损线粒体
几种ROCK抑制剂增加Parkin募集到受损线粒体
线粒体损伤后,PINK1稳定在线粒体外膜上,通过介导磷酸化使得Parkin从胞浆向线粒体募集。随后,Parkin通过标记泛素来指定蛋白酶体或自噬降解的底物。针对该机制,作者开发了一种高通量的小分子筛选,应用CCCP诱导线粒体自噬后,对Parkin在受损线粒体中的募集进行量化,以确定Parkin介导的线粒体自噬的上游调节因子。作者已确定一些Parkin的调控因子,包括TOMM7、HspA1L、BAG4、SIAH3、ATPIF1和HK2。但是,在线粒体自噬级联中改变Parkin募集过程的小分子还有待进一步鉴定。
作者将平均值大于80%的小分子作为候选的靶点,而平均值低于50%则视为抑制剂;为了最大限度地提高恢复真阳性的几率,还根据共同的蛋白质靶标排列Parkin招募增强子。由于在FGFR、ROCK和MEK抑制剂中Parkin募集值最高,其中ROCK抑制剂系列的恢复率又是最高,因此,在后续研究中,作者选择了两种效应最强的ROCK抑制剂Y27632和Y39983,以及另外一种更具选择性的ROCK2抑制剂SR3677。CCCP诱导2小时,SR3677孵育16h后,可见损伤线粒体的Parkin募集增加。
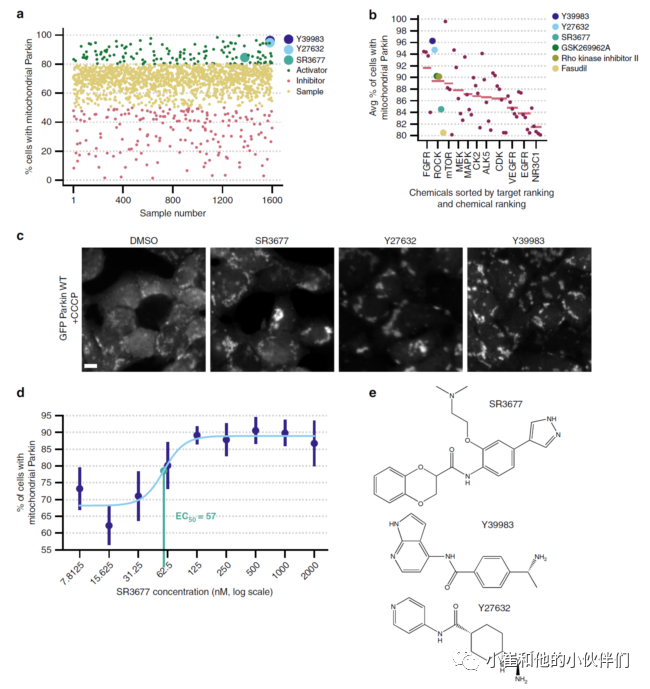 图1. ROCK抑制剂增加Parkin募集到受损线粒体
图1. ROCK抑制剂增加Parkin募集到受损线粒体
ROCK抑制剂在线粒体自噬级联反应中的几个步骤促进线粒体自噬
既往研究表明ROCK抑制在神经退行性变疾病模型中发挥保护作用,包括PD。然而,ROCK在Parkin介导的线粒体自噬通路中的作用尚未被探讨。图2可见,与Ac220相比,Y39983,SR3677增加了Mfn2的降解。由于ROCK2在神经系统中富集,SR3677对ROCK2更高的选择性可能具有治疗优势,因此,随后的验证实验主要关注SR3677。实验结果提示,SR3677增加了另一种线粒体外膜Parkin底物VDAC1的周转。另外,还定量了表达GFP-Parkin和mito-DsRed的HeLa细胞的线粒体质量,其中DsRed是针对线粒体基质的。虽然DMSO和SR3677处理的细胞在DMSO处理24小时后仍保留线粒体质量,但CCCP处理24小时后,经DMSO预处理的细胞中有47.5±8.25%的细胞保留了线粒体,而SR3677预处理的细胞只有28±8.21%。由此可见,SR3677可促进各个亚线粒体组分中的蛋白质降解。
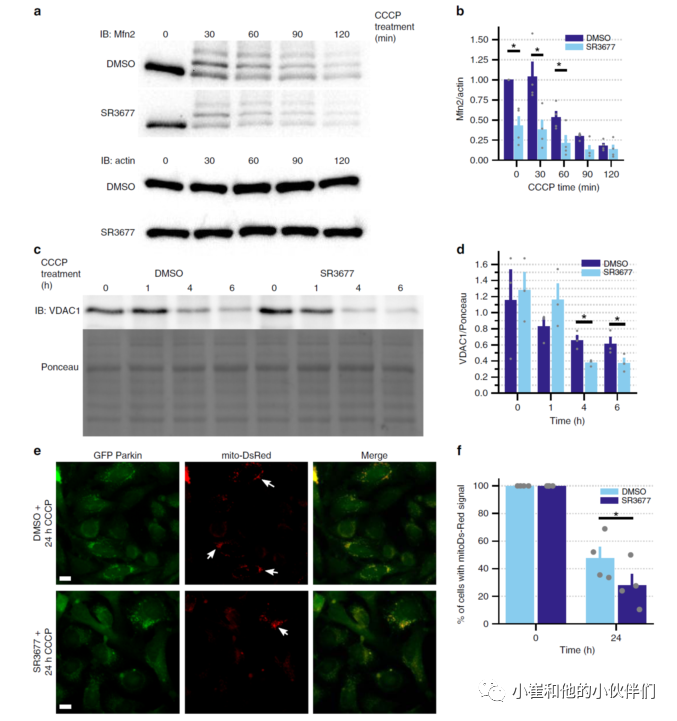
图2. 线粒体被诱导损伤后,SR3677减少线粒体质量
应用mito-QC法测定受损线粒体对溶酶体的靶向性,细胞经SR3677预处理后,线粒体靶向溶酶体增加,诱导线粒体自噬。重要的是,SR3677本身增强但却不诱导线粒体自噬。mitoQC分析也可以在果蝇身上进行,发现mitoQC基因在果蝇脑内多巴胺能神经元簇中表达。而且,SR3677和百草枯(PQ)共处理组(SR+PQ)中,单红色线粒体信号占总线粒体信号的百分比大于对照组(H2O)。以上结果表明SR3677 可增加线粒体对溶酶体的靶向作用。
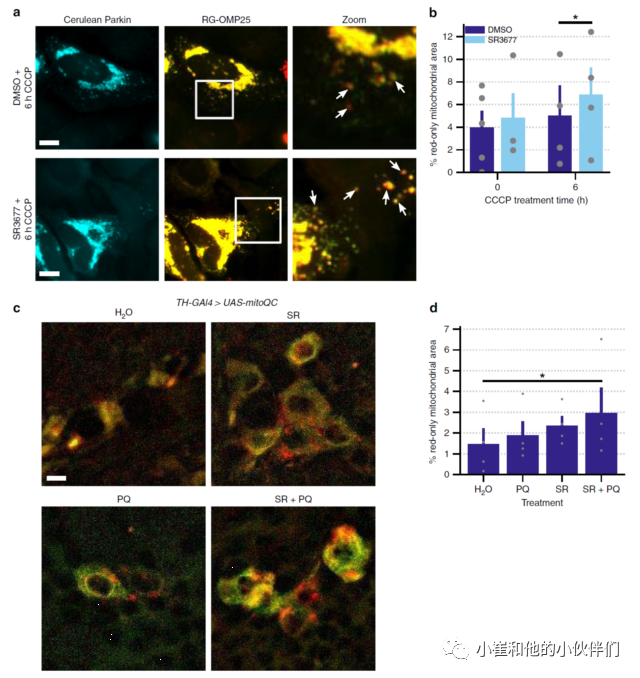
图3. SR3677 增加了线粒体对溶酶体的靶向作用
SR3677通过抑制其典型靶点ROCK2以促进线粒体自噬
建立稳定表达shRNA的细胞株,并通过western blotting验证ROCK2的敲除。发现Parkin募集在ROCK2敲除细胞中增加,而在转染Flag-ROCK2细胞中减少,提示ROCK2对Parkin募集起负调控作用。

图4.ROCK2水平的基因操作模拟SR3677介导的ROCK2抑制的效应
HK2是Parkin的正调控因子,有研究提出Akt介导的HK2活化需要Parkin募集到受损的线粒体;同时,HK2过表达可增加Parkin募集。由于HK2是Parkin底物,于是使用缺乏内源性Parkin的HeLa细胞,发现SR3677处理后可使HK2在线粒体中分布增多。此外,经SR3677处理后,在线粒体组中HK2表达量明显高于总细胞组和胞质组。最后,ROCK抑制剂处理后观察到HK2磷酸化增加。这些结果表明SR3677增加了HK2的活性和线粒体定位。通过这一机制,有可能在不降低细胞活力的情况下,实现上调Parkin介导的线粒体自噬。
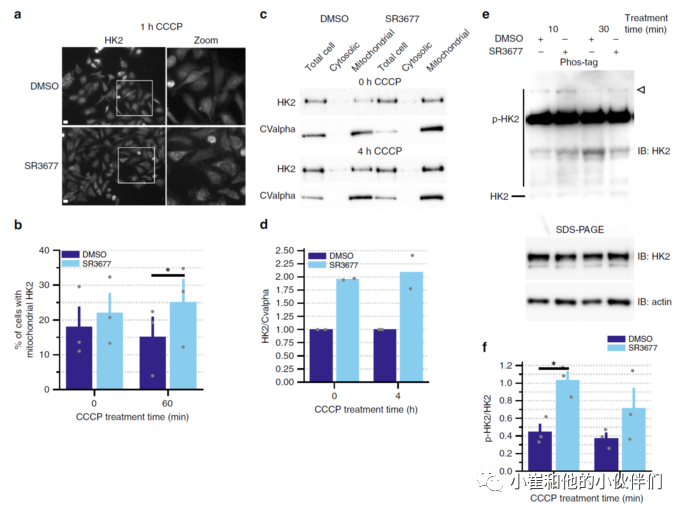 图5. SR3677激活HK2并增加其在线粒体的丰度
图5. SR3677激活HK2并增加其在线粒体的丰度
SR3677在体内的神经保护作用具有帕金森和rok依赖性
作者继续在体内验证 SR3677的功能。首先,明确SR3677是否影响果蝇的生存能力:单独应用SR3677不影响果蝇存活,但是百草枯诱导线粒体损伤后,再应用SR3677可提高遭受帕金森毒素攻击的果蝇存活率。当编码Pink1和parkin基因发生突变可导致线粒体膜电位去极化,线粒体活性氧增加,可表现为攀爬、存活能力受损等;经百草枯处理后,果蝇表现出相似的表型,这可能是线粒体功能紊乱的结果。于是,进一步验证在神经元中观察到的效应是否可以在更复杂的果蝇PD模型中重现: 百草枯可减弱果蝇攀爬能力,而SR3677可抵消百草枯对果蝇造成的损伤,恢复果蝇攀爬能力。随后,继续验证ROCK抑制剂治疗后,神经保护作用是否依赖于Parkin介导的线粒体自噬途径。将酪氨酸羟化酶(TH)-GAL4果蝇与转基因UAS-parkRNAi果蝇杂交,特异性敲除果蝇多巴胺能神经元中的Parkin,发现:在TH-GAL4中果蝇的攀爬能力无明显改善;SR3677的神经保护作用具有剂量依赖性,而且依赖于rok。
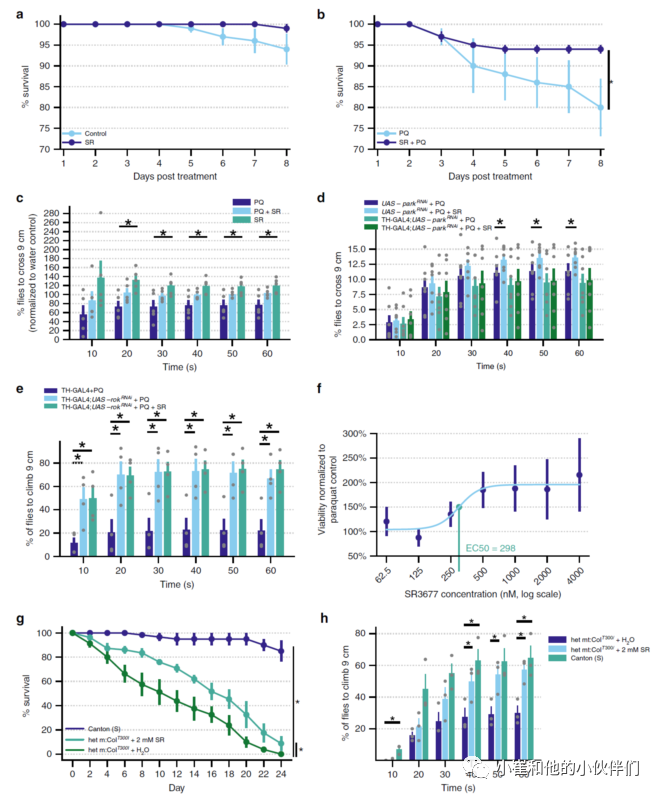
图6. SR3677改善了由遗传和化学线粒体功能障碍引起的存活和攀爬损伤
结 论
该研究认为ROCK是Parkin介导的线粒体自噬途径的关键调控因子,一方面明确了ROCK抑制剂可通过促进Parkin正调控因子HK2向线粒体募集,从而增强线粒体对溶酶体的靶向性,有效清除细胞中受损的线粒体;另一方面还提出了ROCK抑制剂对百草枯(PQ)诱导的线粒体受损果蝇具有神经保护作用,且该保护机制依赖于Parkin和rok,由此揭示了一条可调控Parkin介导的线粒体自噬的信号轴,有助于帕金森病治疗开辟新思路。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








学习#学习#
67