European Radiology:无创预测晚期肺癌免疫治疗效果的加权CT放射组学模型
2023-03-31 shaosai MedSci原创 发表于上海
基于计算机断层扫描(CT)图像的放射组学在评估肿瘤对免疫疗法的反应方面显示出良好的效果,但在病灶层面的预测汇总到病人层面的结果方面仍然存在挑战。
 在过去的十年里,随着程序性细胞死亡蛋白1(PD-1)或程序性细胞死亡蛋白配体1(PD-L1)的免疫检查点抑制剂(ICI)药物的快速发展,免疫疗法在晚期肺癌的治疗中获得了关键作用。美国国家综合癌症网络(NCCN)推荐将PD-1/PD-L1阻断疗法用于治疗没有可靶向基因突变的局部晚期和转移性非小细胞肺癌(NSCLC)。尽管如此,根据以往的文献,有益的结果只存在于15-40%的患者中。因此,确定免疫疗法反应的更有效的预测性生物标志物的需求显得愈发重要。
在过去的十年里,随着程序性细胞死亡蛋白1(PD-1)或程序性细胞死亡蛋白配体1(PD-L1)的免疫检查点抑制剂(ICI)药物的快速发展,免疫疗法在晚期肺癌的治疗中获得了关键作用。美国国家综合癌症网络(NCCN)推荐将PD-1/PD-L1阻断疗法用于治疗没有可靶向基因突变的局部晚期和转移性非小细胞肺癌(NSCLC)。尽管如此,根据以往的文献,有益的结果只存在于15-40%的患者中。因此,确定免疫疗法反应的更有效的预测性生物标志物的需求显得愈发重要。
PD-L1的表达状态在临床上被用来选择PD-1/PD-L1 ICIs的候选者,但其作为预测性生物标志物的有效性存在争议。此外,该指标湖获得是一个侵入性的程序,并不适合所有的病人。因此,仍然需要一个非侵入性的生物标志物来对接受免疫疗法的患者进行精确分层。
预后不良与一些临床特征有关,如免疫治疗的晚期行和治疗前存在远处转移,但这些发现是基于相对较小的队列。基于计算机断层扫描(CT)图像的放射组学在评估肿瘤对免疫疗法的反应方面显示出良好的效果,但在病灶层面的预测汇总到病人层面的结果方面仍然存在挑战。将相同的患者反应分配给所有病灶是一种典型的病灶放射组学分析,但该方法没有考虑到独特的免疫相关反应所引起的影响。其他患者层面的方法包括选择最大的病灶或按平均值计算,但结果远不能令人满意。最近的研究表明,基于注意力的多实例学习(a-MIL)技术可能有助于建立预测模型,可将更多的权重赋予与特定分类任务相关的最相关的子区域。
近日,发表在European Radiology杂志的一项研究探讨了使用来自治疗前CT扫描的多个肺内病变的放射组学特征的自适应加权总和在提高放射组学模型性能方面的价值,以实现临床无创预测免疫治疗长期无进展生存(PFS≥6个月)的效果。
本项单中心回顾性研究在185名患者中开发并交叉验证了一个放射组学模型,并在48名患者中进行了测试。二元终点是持久临床获益(DCB,PFS≥6个月)和非DCB(NDCB,PFS<6个月)。放射组学特征是从多个肺内病变中提取的,并通过基于注意力的多实例学习模型进行加权。然后通过L2-规则化脊回归选择汇总的特征。研究进行了五个机器学习分类器,单独使用放射学和临床特征,然后一起建立预测模型。最后,通过Kaplan-Meier生存分析验证了具有最佳性能的模型的预测价值。
与最大病灶法(AUCs:0.70-0.78)和平均总和法(AUCs:0.64-0.80)相比,基于加权放射学方法的预测模型在所有分类器中都显示出优越性能(AUCs:0.75-0.82)。其中,逻辑回归模型的性能最为均衡(AUC=0.87[95%CI 0.84-0.89],0.75[0.68-0.82],0.80[0.68-0.92],分别在训练、验证和测试队列中产生)。增加五个临床特征后,仅有放射线模型的性能明显增强(训练。AUC 0.91 [0.89-0.93], p = .042; 验证。AUC 0.86 [0.80-0.91], p = 0.011; 测试。AUC 0.86 [0.76-0.96], p = .026)。基于放射学的预测模型的Kaplan-Meier分析显示,分类器预测的DCB与NDCB之间的PFS有明显的分层(HR = 2.40-2.95,p < 0.05)。
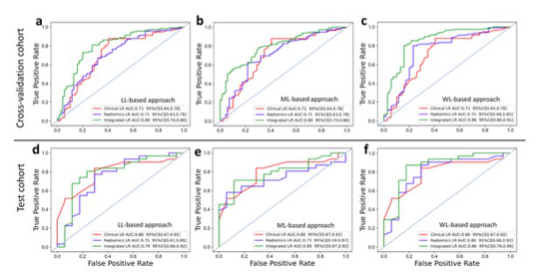
图 a-c 临床(红色)、放射组学(蓝色)和综合(绿色)逻辑回归模型的ROC曲线,这些模型采用基于LL的放射组学特征(a)、基于ML的放射组学特征(b)和基于WL的放射组学特征(c)建立,用于区分交叉验证队列中的DCB与NDCB。d-f 用基于LL的放射组学特征(d)、基于ML的放射组学特征(e)和基于WL的放射组学特征(f)建立的临床(红色)、放射学(蓝色)和综合(绿色)逻辑回归模型的ROC曲线,用于区分测试队列中的DCB与NDCB
本项研究提出的非侵入性预测模型基于来自多个肺内病灶的放射组学特征的加权总和,可作为一种新的方法为免疫疗法候选者的肺癌患者带来巨大的生存利益,且具有相当大的临床前景。
原文出处:
Zhenchen Zhu,Minjiang Chen,Ge Hu,et al.A pre-treatment CT-based weighted radiomic approach combined with clinical characteristics to predict durable clinical benefits of immunotherapy in advanced lung cancer.DOI:10.1007/s00330-022-09337-7
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言