Blood:胞外组蛋白可替代凝血酶原启动促进血管内凝血!
2021-01-14 Nebula MedSci原创
凝血酶的产生对血液生理凝块的形成和弥散性血管内凝血(DIC)的病理发展都至关重要。在危重疾病中,广泛的细胞损伤会释放组蛋白进入血液循环,这可以增加凝血酶的生成并导致DIC,但其分子机制尚不清楚。
凝血酶的产生对血液生理凝块的形成和弥散性血管内凝血(DIC)的病理发展都至关重要。在危重疾病中,广泛的细胞损伤会释放组蛋白进入血液循环,这可以增加凝血酶的生成并导致DIC,但其分子机制尚不清楚。
通常情况下,凝血酶是由凝血酶原复合物产生的,由活化的X因子(FXa)、活化辅因子V(FVa)和磷脂组成,在钙存在的情况下可裂解凝血酶原。
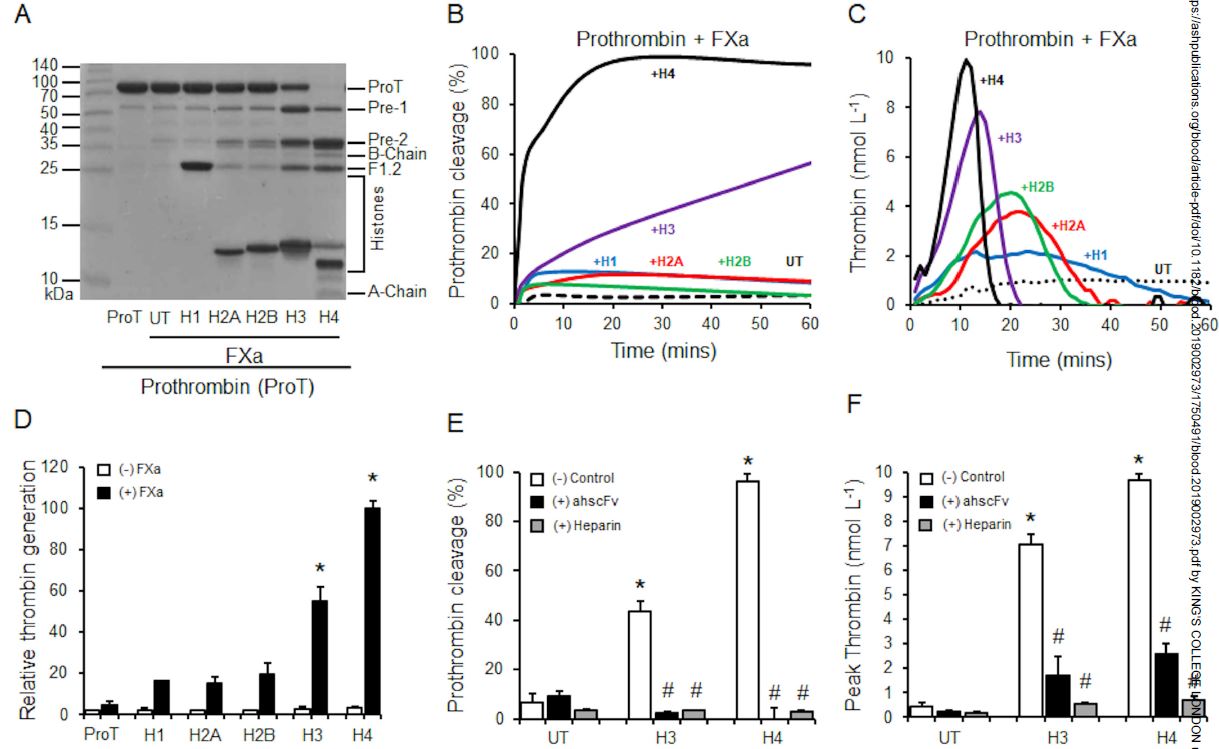
组蛋白对凝血酶原裂解和凝血酶生成的影响
在本研究中,研究人员发现,在细胞外组蛋白存在的情况下,即使没有FVa和磷脂也可以形成一种替代的凝血酶原酶。
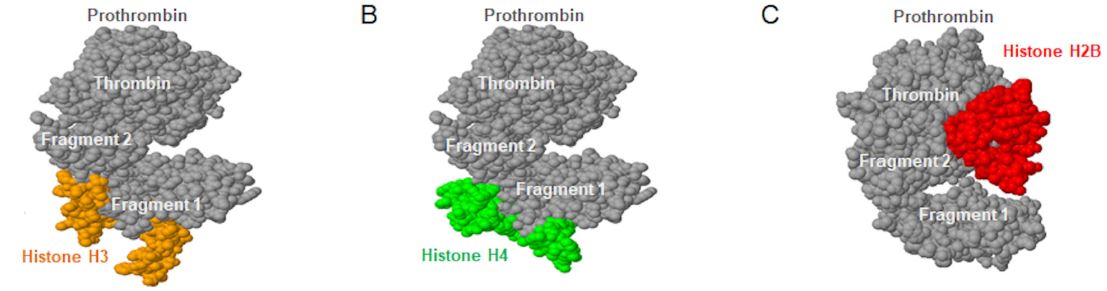
组蛋白直接与凝血酶原片段F1和片段F2结合
组蛋白直接与凝血酶原片段F1和片段F2特异性结合,促进凝血酶原FXa裂解释放活性凝血酶,不同于FVa需要磷脂表面锚定经典凝血酶原复合物。给小鼠输注组蛋白可诱发DIC,但在输组蛋白前先输注凝血酶原片段F1+F2可消除组蛋白诱发的DIC。
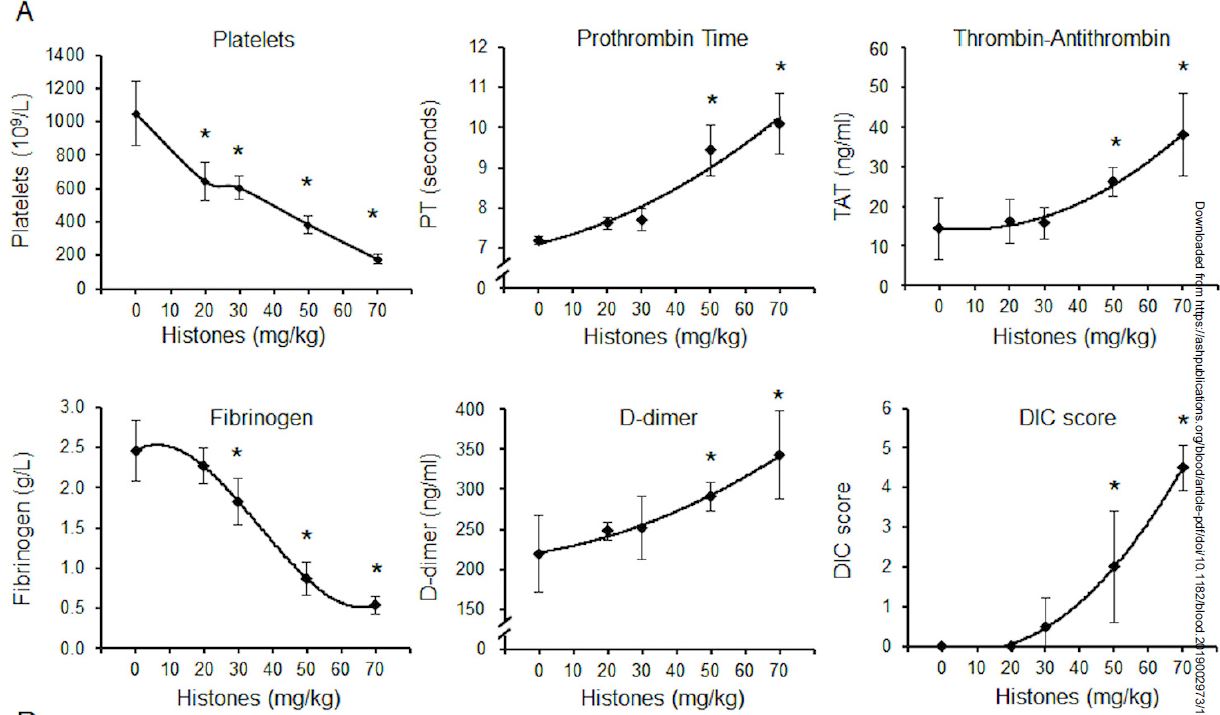
凝血酶原片段F1+F2减轻组蛋白诱发的DIC
在一组重症监护病房(ICU)的脓毒症患者(n=144)中,发生DIC的患者的循环组蛋白水平显著升高。这些数据提示,组蛋白诱导的无磷脂锚定的替代凝血酶原可导致血管内凝血,揭示了凝血酶生成和DIC发生的新分子机制。
此外,组蛋白显著降低了凝血级联对FXa的需求,使凝血因子VIII(FVIII)和FIX缺乏的血浆以及FVIII缺乏的小鼠都能够形成血凝块。
综上所述,本研究强调了一种新的凝血机制,在治疗系统性凝血激活和纠正凝血因子缺乏方面均具有一定的治疗潜力。
原始出处:
Abrams Simon T,Su Dunhao,Sahraoui Yasmina et al. Assembly of alternative prothrombinase by extracellular histones initiates and disseminates intravascular coagulation. Blood, 2021, 137: 103-114. DOI:10.1182/blood.2019002973
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#组蛋白#
61
#凝血酶原#
66
#弥散性血管内凝血#
205
666
191
哇塞
195