PHILIPS每日一例:鞍旁脑膜血管周细胞瘤1例
2022-09-07 放射沙龙 中国临床医学影像杂志
HPC虽然比较少见,但是影像学表现具有一定的特征性,包括分叶、信号不均、富含血管、不均匀强化、可有骨质破坏,这些影像学表现有助于HPC的诊断。
病例女,46岁。双眼视物模糊2月余,时有头痛、头晕,无恶心、呕吐,无心慌、胸闷,无抽搐发作,无肢体功能障碍,无多饮多尿。化验室检查均为阴性。
影像学表现:CT平扫(图1)示左侧鞍旁分叶状高密度影,大小约4.8 cm×5.6 cm,无钙化,CT值50 HU,注射对比剂后明显强化.动脉期CT值136—240 HU。病灶与左侧海绵窦分界不清,左侧中脑受压。MR示左侧鞍旁不规则团块影,T1WI呈等、低混杂信号,T2WI呈等、高、低混杂信号(图2),增强后病灶显著均匀强化、内见穿支血管(图3),肿瘤占位效应明显。颅内CTA示左侧鞍旁占位病变,血供丰富,可见瘤内血管影,左侧大脑中动脉、大脑后动脉受压移位。
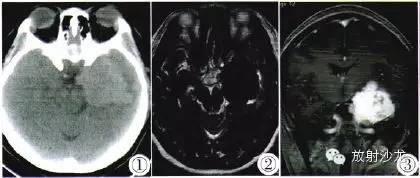
图1 CT平扫示左侧鞍旁分叶状高密度影,无钙化,CT值50 HU。图2 T2WI呈等、高、低混杂信号。图3注射对比剂后增强T2WI示明显强化,动脉期CT值136—240 HU,病灶与左侧海绵窦分界不清,左侧中脑受压。
手术所见:术中咬除左侧颞骨至中颅窝底部,悬吊硬膜.放射状剪开硬膜,镜下切除左侧部分颞极组织,暴露肿瘤,见质地较韧、呈桑葚状,血运极为丰富,中颅窝底硬膜未见明显侵犯。肿瘤内侧界包绕视神经和颈内动脉,大脑中动脉被挤向内侧上方,无蛛网膜界限,肿瘤基底膜穿破海绵窦上壁。镜下保护颈内动脉、大脑中动脉和视神经,行次全切肿瘤以减压,约5 cm×4 cm×4 cm,残留海绵窦内及与颈内动脉、视神经包绕的部分肿瘤。
病理诊断:冰冻病理示送检肿瘤组织细胞极化严重。细胞增生活跃,考虑为脑膜来源肿瘤,倾向恶性。镜下(图4)显示鹿角样增生血管及其周密集的梭形细胞。
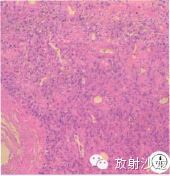
图4 石蜡切片示鹿角样增生血管及其周密集的梭形细胞。
免疫组化(图5):EMA(-),CD34(+),S-lOO(-),actin(+/-),desmin(+/-),bcl-2(+),ki-67<5%。病理诊断为脑膜血管周细胞瘤(Hemangiopericytoma,HPC)。

图5 免疫组化:EMA(-),CD34(+),S-lOO(-),actin(+/-),desmin(+/-),bcl-2(+),ki-67<5%。
讨论
HPC主要发生在皮肤和骨肌系统,颅内罕见,大约占中枢神经系统肿瘤的0.4%。HPC以中年多见。平均发病年龄为40~45岁.男性略多于女性。HPC曾经被认为是脑膜瘤亚型,后经Lolava的肿瘤酶组织化学研究和Poppff的电镜观察证实,其与软组织血管外皮细胞瘤的组织学相同。因此,1993年WHO将其定于间叶起源的非脑膜间质肿瘤。2007年版的WHO新分类中,HPC的级别被定为Ⅱ~Ⅲ级。
中枢神经系统HPC来源于脑膜间质的毛细血管Zimmerman细胞,该细胞是紧贴毛细血管网状纤维排列的梭形细胞,具有多向分化的潜能。临床上,HPC患者常以头晕、头痛为首发症状.病程数月至数年不等.但较脑膜瘤短。HPC易发生转移.常转移到肺、骨髓、肝、腹膜后淋巴结。
HPC的影像学具有一定特征性。CT平扫上HPC多呈分叶状,瘤内易坏死囊变,呈高低混杂密度,少有钙化;多数占位效应明显而水肿较轻,局部可有骨质破坏;增强扫描后多呈明显不均匀强化。MR T1WI上肿瘤多呈等、高不均匀信号,T2WI上也多呈高、等不均匀信号,瘤内可见较丰富的流空血管影,增强扫描后瘤体呈明显不均匀强化。其内还可见迂曲血管影。
HPC多位于鞍旁,常需要与以下病变相鉴别:
①鞍旁脑膜瘤:HPC与脑膜瘤的鉴别较困难。脑膜瘤多呈类圆形,CT上多为等或稍高密度,而T1WI、T2WI均呈等信号;瘤内血供丰富但少有流空血管;瘤内常有钙化;瘤体基底宽,与硬膜相贴近;增强多明显均匀强化。“硬膜尾征”是其相对特征性改变;邻近的骨质多呈增生性改变而少有侵蚀性破坏。而HPC多为分叶状。密度或信号不均,瘤内常有流空血管影,钙化很少见;窄基底与硬膜相连;不均匀强化是其增强表现;邻近骨质常侵蚀性破坏。
②三叉神经鞘瘤:肿瘤多为圆形或分叶状,边界清;CT表现为等、低密度,MRI T1WI为等或低混杂信号,T2WI为高信号,瘤内常见囊变、坏死;增强后病灶不均、环状强化;通常无瘤周水肿;三叉神经瘤沿海绵窦、桥前池生长,可引起蝶骨大、小翼或岩骨尖骨质结构吸收。
③海绵状血管瘤,因容易反复出血而病灶MRI信号复杂,取决于出血的不同时相,常为高低混杂信号,周围环绕含铁血黄素低信号(“铁环征”)为其特征性表现。
④垂体大腺瘤(累及鞍旁):肿瘤起自垂体,正常垂体组织往往缺失、显示不清,可有“腺体包绕征”;T1WI为稍低信号,而T2WI为稍高信号,瘤内常有囊变或微囊变,肿瘤自鞍内向鞍上生长,可见“束腰征”;增强后为延迟强化,强化幅度弱于正常垂体;瘤体压迫海绵窦,可引起局部骨质吸收。
⑤颈动脉瘤:CT平扫显示为鞍旁圆形略高密度影,增强后与动脉同步强化(合并的血栓不强化),CTA可清晰显示其载瘤动脉。无血栓的动脉瘤在MR TlWI和T2WI均为流空低信号;有血栓的动脉瘤,其血栓信号演变与出血信号相仿:增强后明显的与动脉同步强化。MRA对于显示其来源很有帮助。
⑥颈动脉、海绵窦瘘:CT示患侧海绵窦扩大,密度增高,对侧海绵窦也可扩大,CTA能明确显示血管团及增粗迂曲的眼上静脉。在T1WI和T2WI上因流空效应而呈低或无信号,T1WI和T2WI均呈高信号时为其内血栓形成;增强后可见杂乱血管团以及引流的静脉(DCE—MRA)。
⑦脊索瘤:大多数起源于斜坡组织,瘤内常含钙化,局部骨质破坏,有残留骨嵴;肿瘤密度或信号不均;多不均匀强化。此外,还需要与起源于中颅窝底的一些少见肿瘤,如软骨瘤(肉瘤)、骨巨细胞瘤、淀粉样瘤等相鉴别。
综上所述,HPC虽然比较少见,但是影像学表现具有一定的特征性,包括分叶、信号不均、富含血管、不均匀强化、可有骨质破坏,这些影像学表现有助于HPC的诊断。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







很好,值得学习
54
#周细胞#
46
#iPS#
55
#细胞瘤#
56