NEJM:新疗法,终于提高了这类高度恶性膀胱癌的生存率!
2024-09-26 Hanson临床科研 Hanson临床科研 发表于上海
本研究通过将免疫检查点抑制剂Durvalumab与标准新辅助化疗方案相结合,为肌层浸润性膀胱癌患者提供了一种新的治疗策略,显著提升了无事件生存率和总生存率,这可能改变当前的临床治疗模式。
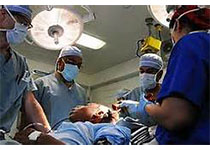
肌层浸润性膀胱癌(MIBC)是一种高度恶性的泌尿系统肿瘤,其治疗手段主要包括手术和化疗。根治性膀胱切除术是MIBC治疗的金标准,但即便经过彻底手术,仍有约50%的患者在3年内出现复发。
为了提高治疗效果,新辅助化疗被广泛用于手术前的治疗,旨在缩小肿瘤、控制微转移,并提高手术成功率。顺铂为基础的化疗方案是MIBC新辅助治疗的常用选择【1】。
近年来,免疫治疗的兴起为肿瘤治疗带来了革命性的进展。免疫检查点抑制剂,如程序性死亡蛋白-1(PD-1)及其配体(PD-L1)抑制剂,通过解除肿瘤细胞对免疫系统的抑制,恢复和增强机体对肿瘤的免疫应答。在晚期膀胱癌的治疗中,免疫检查点抑制剂已经显示出了显著的疗效。Durvalumab是一种人源化的PD-L1抑制剂,它通过特异性地结合PD-L1,阻断其与PD-1和CD80的相互作用,从而激活T细胞对肿瘤的免疫应答【2】。
2024年9月15日,Thomas Powles 等研究学者在国际顶尖医学期刊 NEJM 上发表了一项3期、开放标签、随机对照试验结果,题为 Perioperative Durvalumab with Neoadjuvant Chemotherapy in Operable Bladder Cancer 【3】。本研究旨在评估在MIBC的新辅助治疗中加入Durvalumab,是否能够提高患者的无事件生存率和总生存率,为MIBC的综合治疗提供新的策略。
研究结果显示,
-
Durvalumab组24个月的无事件生存率为67.8%,对照组为59.8%;
-
Durvalumab组的总生存率为82.2%,对照组为75.2%。
-
两组3级或4级不良事件发生率相近,分别为40.6%和40.9%。
-
这些结果表明,Durvalumab的加入可以显著改善患者的预后。

主要研究内容和结果
🔷 患者分配与治疗:
研究共纳入1063名患者,随机分配至Durvalumab组(533名)和对照组(530名)。Durvalumab组患者接受了新辅助Durvalumab联合吉西他滨-顺铂治疗四个周期,随后进行根治性膀胱切除术,并接受Durvalumab辅助治疗八个周期。对照组患者仅接受新辅助吉西他滨-顺铂化疗后进行根治性膀胱切除术。
根治性膀胱切除术的执行:Durvalumab组中有88.0%的患者接受了根治性膀胱切除术,对照组中这一比例为83.2%。
🔷 Durvalumab疗效:
-
无事件生存期(EFS):在24个月时,Durvalumab组的EFS为67.8%,而对照组为59.8%。Durvalumab组相较于对照组显示出显著的EFS改善(HR=0.68, 95% CI: 0.56-0.82; p<0.0001)。
-
总生存期(OS):在24个月时,Durvalumab组的OS为82.2%,对照组为75.2%。Durvalumab组相较于对照组在OS上也有显著改善(HR=0.75, 95% CI: 0.59-0.93; p=0.01)。
🔷 安全性:
Durvalumab组中有40.6%的患者经历了3级或4级的与治疗相关的不良事件,对照组中这一比例为40.9%。两组中因治疗相关的不良事件导致死亡的患者比例均为0.6%。
综上所述,研究结果表明,在新辅助化疗中加入Durvalumab可以显著提高肌层浸润性膀胱癌患者的无事件生存期和总生存期,且安全性可控。上述发现支持将Durvalumab联合新辅助化疗作为顺铂适用的肌层浸润性膀胱癌患者的潜在新治疗选择。
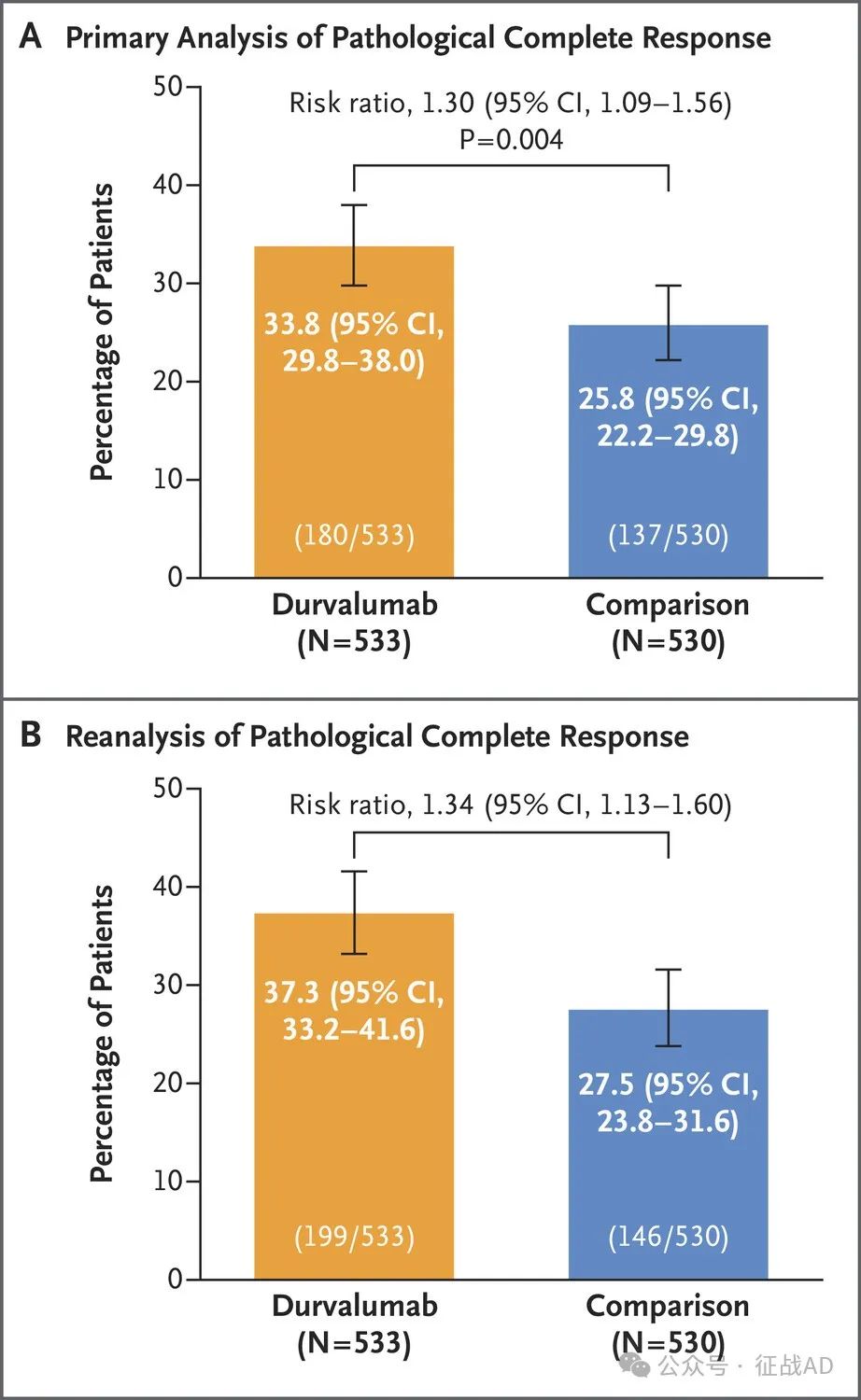
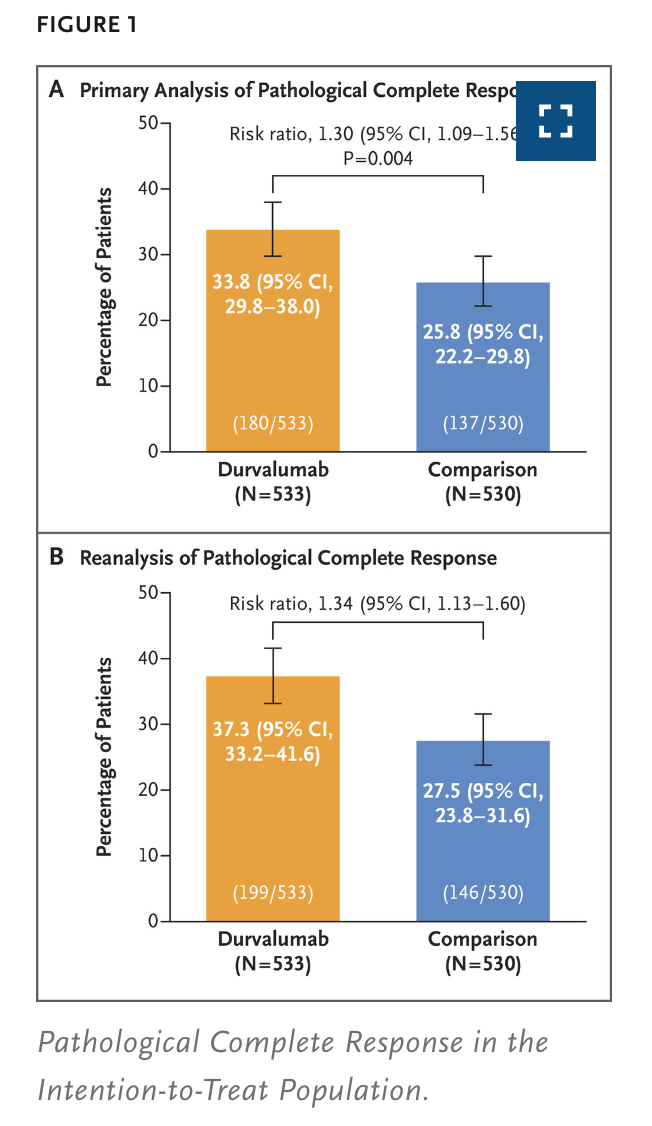
图1. 病理完全缓解的ITT人群分析
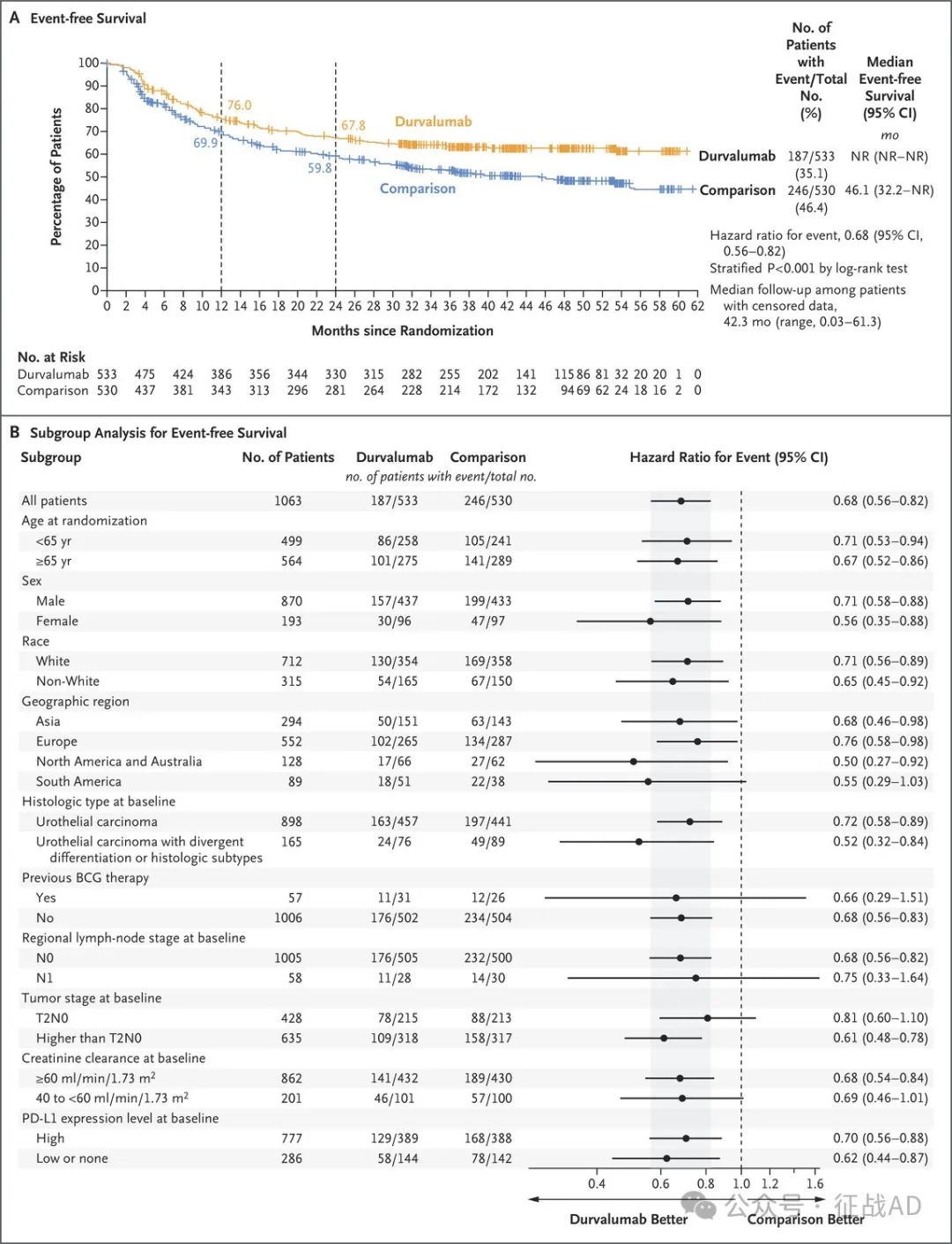
图2. ITT人群无事件生存期
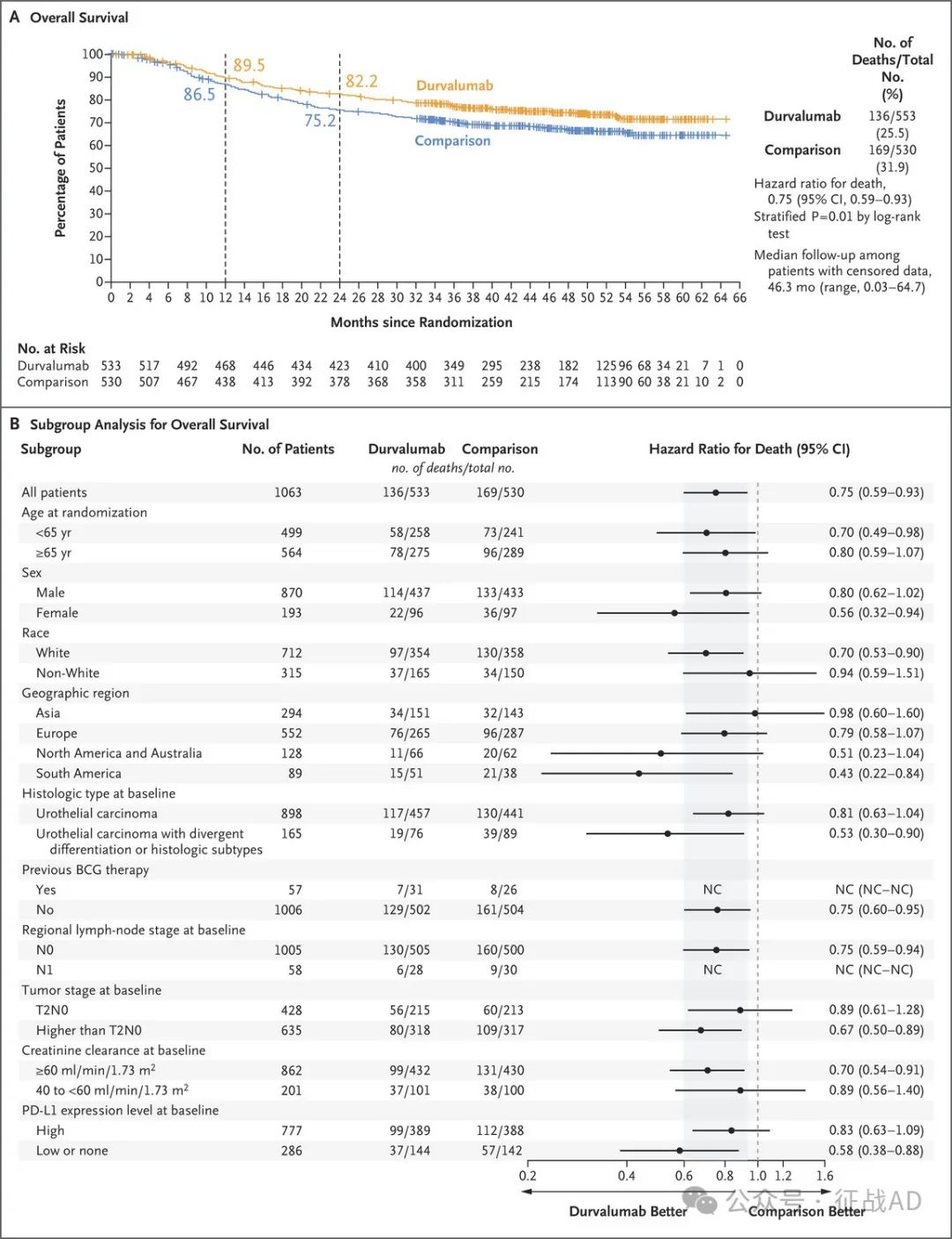
图3. ITT人群总生存期
编者按:
临床意义和科研启示:
本研究通过将免疫检查点抑制剂Durvalumab与标准新辅助化疗方案相结合,为肌层浸润性膀胱癌患者提供了一种新的治疗策略,显著提升了无事件生存率和总生存率,这可能改变当前的临床治疗模式。
科研方面,
此项研究强调了免疫治疗在膀胱癌综合治疗中的重要地位,并为未来探索更多个体化治疗方案、生物标志物的研究以及药物联合应用的策略提供了重要方向。
此外,研究结果也提示科研人员需进一步深入研究免疫微环境的作用机制,以及如何通过精准医学手段筛选出最有可能从免疫治疗中获益的患者群体。
原文链接:
【1】Sarkis J, Vannier E, Mjaess G, et al. Neoadjuvant immunochemotherapy in the treatment of nonmetastatic muscle-invasive bladder cancer: a systematic review. Immunotherapy 2022;14:1407-1417.
【2】Cathomas R, Rothschild SI, Hayoz S, et al. Perioperative chemoimmunotherapy with durvalumab for muscle-invasive urothelial carcinoma: primary analysis of the single-arm phase II trial SAKK 06/17. J Clin Oncol 2023;41:5131-5139.
【3】https://doi.org/10.1056/NEJMoa2408154
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#膀胱癌# #新辅助化疗# #Durvalumab#
61