Cell:癌症疫苗又一突破!新型单细胞测序技术成功助力!
2019-01-28 Paris 转化医学网
黑色素瘤是皮肤肿瘤中恶性程度最高的一种肿瘤,其扩散速度快,并且更偏爱男性。据《A Cancer Journal for Clinicians》2017年发表的癌症统计,黑色素瘤发病率在男性中比在女性中高约60%,死亡率在男性中比在女性中高出一倍以上。最糟糕的是黑色素瘤对放疗不敏感,所以晚期黑色素瘤患者从常规疗法中获益极少。但是免疫疗法打破了这一僵局。
导 读
黑色素瘤是皮肤肿瘤中恶性程度最高的一种肿瘤,其扩散速度快,并且更偏爱男性。据《A Cancer Journal for Clinicians》2017年发表的癌症统计,黑色素瘤发病率在男性中比在女性中高约60%,死亡率在男性中比在女性中高出一倍以上。最糟糕的是黑色素瘤对放疗不敏感,所以晚期黑色素瘤患者从常规疗法中获益极少。但是免疫疗法打破了这一僵局。
近日,以色列Weizmann Institute of Science的单细胞测序领域大牛Ido Amit实验室(李汉杰博士为论文第一作者)和Amos Tanay实验室,联合Netherlands Cancer Institute的肿瘤免疫学界大牛Ton Schumacher在Cell上发表了题为Dysfunctional CD8 T Cells Form a Proliferative, Dynamically Regulated Compartment within Human Melanoma的研究论文,揭示了免疫治疗之所以能够“全面开花”的关键:他们发现癌症中免疫细胞的异质性对免疫治疗的效果有重要影响,功能失调的CD8 T细胞在肿瘤微环境中处于动态分化和高度活跃的状态,而且很可能驱动着肿瘤特异性免疫应答。
作为免疫治疗的“头号种子”,PD-1/PD-L1抑制剂在黑色素瘤治疗中的应用经历了“几级跳”。最初是在ipilimumab(IPI,CTLA-4单抗)一线治疗失败后,采用PD-1单抗作为二线、三线治疗,结果发现疗效优于化疗,因此PD-1单抗成为IPI治疗失败后的标准治疗;之后,人们将PD-1单抗与IPI对比用于一线治疗,发现其疗效又比IPI好,于是PD-1单抗成为黑色素瘤一线标准治疗;
接着,在辅助治疗的PK中,PD-1单抗再次战胜IPI;紧随其后,PD-1单抗又“拿下”了过去一直无法逾越的“高地”——脑转移(曾任美国总统的Jimmy Carter在接受PD-1单抗药物pembrolizumab治疗后,黑色素瘤的脑转移病灶达到CR,且未出现新的脑转移灶)。
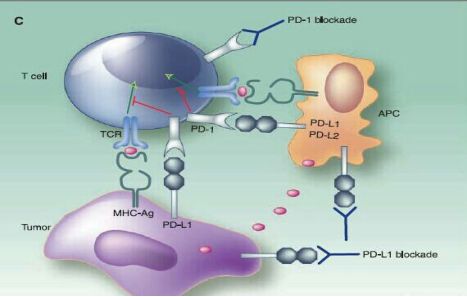
免疫疗法虽然效果显着,但它也有不可避免的副作用。根据以往的研究显示,免疫疗法的联合使用虽然会使得疗效翻倍,但是副作用也存在着叠加翻倍的现象,例如PD-1药物和CTLA-4药物联用副作用变大了。因此,需要进一步研究免疫治疗对于癌症细胞作用的关键机制以尽可能消除其毒性作用。
早在之前的研究中,科学家们对未接受过免疫治疗的黑色素瘤患者的肿瘤标本以及抗PD-1治疗期间连续性活检标本进行流式检测和免疫荧光染色。研究结果表明,CD69+CD103+肿瘤定植CD8+T细胞数目增加与未接受过免疫治疗的黑色素瘤患者黑色素瘤特异性生存改善有关。局部IL15表达水平与这些肿瘤定植T细胞数目有显着的相关性。包括PD-1和LAG3在内的几种免疫检查点表达增加,在抗PD-1免疫治疗早期这些细胞显着扩增。
之后,研究人员对25个黑素瘤患者的肿瘤内免疫细胞进行了单细胞转录组和单细胞TCR分析。他们的研究发现尽管不同免疫细胞亚型存在于大多数患者中,它们的相对丰度在不同患者中存在很大差异。值得注意的是,尽管丰度不同,所观察到的CD8T细胞的的分化途径确是高度保守的。
也就是说,大多数观察到的T细胞类群在多数患者中都存在。这表明T细胞的转录状态在不同患者之间有一定的保守性,但不同患者中不同免疫细胞类群的丰度是有较大差异的。特别地,CD8功能失调T在肿瘤浸润性T细胞中的比例最低为3.6%,最高可达72.1%。
这与我们这之前所认知的“CD-T8细胞在肿瘤微环境中处于耗竭状态”是截然不同的,不仅如此,CD8T细胞细胞实际上在肿瘤微环境中是高度增殖,且动态分化的,经过一个“过渡状态”分化为功能失调状态。这为黑色素瘤疫苗提供了更多的免疫应答!
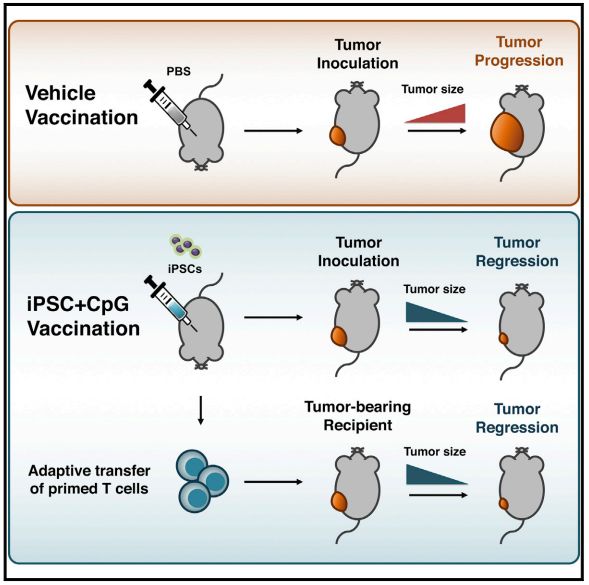
在此之前,来自德国海德堡大学医院的科学家已经证明:肿瘤中浸润的T细胞正是癌症疫苗诱导的新抗原特异性T细胞。在外周诱导出的T细胞可以穿过血脑屏障,到达颅内的病灶!
这一年来,免疫治疗可谓是,喜报频传,未来,还会有更多惊喜等着我们,让我们拭目以待!
原始出处:Li H1, van der Leun AM2, Yofe I1, et al. Dysfunctional CD8 T Cells Form a Proliferative, Dynamically Regulated Compartment within Human Melanoma. Cell. 2018 Dec 20.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#CEL#
77
#Cell#
43
学习了谢谢
0
好
81
谢谢了,学习
77