Advanced Accelerator Applications 旗下LUTATHERA获批用于胃肠胰神经内分泌肿瘤治疗
2018-01-28 MedSci MedSci原创
作为诺华公司的一员,Advanced Accelerator Applications S.A现已发展成为一家核医学领域的领导者,该公司于2018年1月26日宣布,其旗下的LUTATHERA的新药申请(new drug application,NDA)已经获得了美国FDA的批准用于治疗生长抑素受体阳性的胃肠胰神经内分泌肿瘤(GEP-NETs),包括成人的前肠,中肠和后肠神经内分泌肿瘤
作为诺华公司的一员,Advanced Accelerator Applications S.A现已发展成为一家核医学领域的领导者,该公司于2018年1月26日宣布,其旗下的LUTATHERA的新药申请(new drug application,NDA)已经获得了美国FDA的批准用于治疗生长抑素受体阳性的胃肠胰神经内分泌肿瘤(GEP-NETs),包括成人的前肠,中肠和后肠神经内分泌肿瘤。
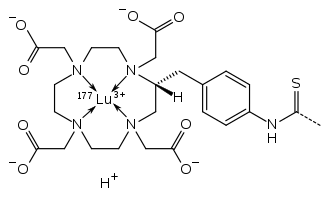
LUTATHERA是一种放射性Lu 177标记的生长抑素类似物,能够选择性地靶向II型生长抑素受体,药物一旦通过输注滴注到血流中,LUTATHERA就能够结合肿瘤细胞上的特定受体,然后被内化到靶细胞中,其中放射性组分就能从靶细胞内部破坏肿瘤细胞。作为一种已经获得FDA孤儿药认定的药物,LUTATHERA也是第一款肽受体放射性核素治疗(PRRT)药物(即带有放射性成分的靶向分子)。
NETs是一种罕见的肿瘤,起源于许多器官的神经内分泌细胞,包括胃肠道,胰腺和肺。根据美国国家癌症研究所的监测,流行病学和最终结果数据库(SEER)显示美国的NETs新发病例的发病率约为每年6.98 / 10万人。通常,NETs患者的5年生存概率为35%。
原始出处:
http://www.firstwordpharma.com/node/1539515?tsid=4#axzz55NkMXJoh
本文系梅斯医学(MedSci)原创编译整理,转载需授权!
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#ACCE#
80
#内分泌肿瘤#
91
#Advanced#
128
#ACCE#
90
#神经内分泌#
65
#CEL#
65
#分泌#
71
#ERA#
81
#胃肠胰神经内分泌肿瘤#
103
#肿瘤治疗#
74