胶质母细胞瘤(GBM)的治疗或迎新进展!DB102获得FDA快速通道资格
2020-07-18 Allan MedSci原创
生物制药公司Denovo今日宣布,美国FDA已授予DB102(enzastaurin)快速通道资格,该药物正在开发中,用于治疗初治胶质母细胞瘤(GBM)。
生物制药公司Denovo今日宣布,美国FDA已授予DB102(enzastaurin)快速通道资格,该药物正在开发中,用于治疗初治胶质母细胞瘤(GBM)。DB102(enzastaurin)是PKC beta、PI3K和AKT途径的研究性小分子丝氨酸/苏氨酸激酶抑制剂,已在3,000例实体瘤和血液肿瘤中进行了研究。DB102已从FDA和EMA获得治疗DLBCL和GBM的孤儿药称号。
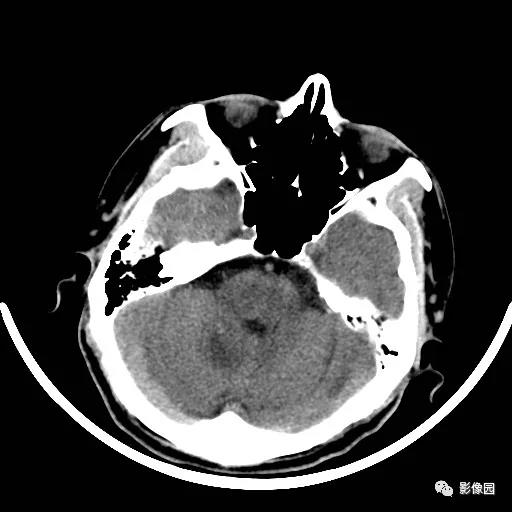
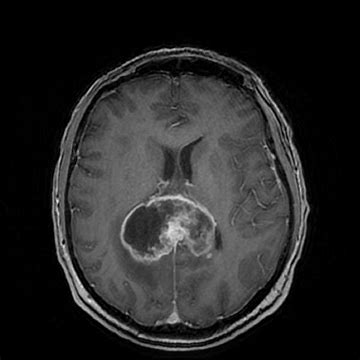
尽管众多制药公司进行了许多尝试,GBM仍然是最致命的癌症之一,一线治疗方案仍依赖替莫唑胺。许多有希望的抗癌药物,包括抗PD-1药物,都无法超过替莫唑胺的疗效。借助Denovo最新发现的生物标志物DGM1,发现DB102(enzastaurin)可以改善具有DGM1生物标志物的胶质母细胞瘤患者的生存结局,而与MGMT甲基化状态无关。Denovo计划开展DB102(enzastaurin)联合替莫唑胺的随机、双盲、安慰剂对照III期临床研究。
Denovo首席技术官Xiao-Xiong Lu博士说:“获得快速通道资格是DB102开发过程中的重要里程碑。它有可能加速DB102的开发,以满足大量未满足的医疗需求”。

原始出处:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#胶质母细胞#
0
#GBM#
59
#母细胞瘤#
48
#细胞瘤#
45
#快速通道资格#
61
学习
107
希望有突破
115
我想知道优势在哪里?
110
#胶质母细胞瘤#新药越来越多,但是突破性进展还少。
245