Nature:运动会上瘾?科学家揭示放大运动奖赏效应的肠脑轴信号
2022-12-28 周科 “神经周K”公众号 发表于上海
本文揭示了肠道菌群通过产生脂肪酸酰胺等物质,激活外周TRPV1 阳性感觉神经元,促进纹状体多巴胺的释放,增强运动的动机行为。
长期运动可减少高血压、糖尿病等慢性疾病的患病风险。最近的研究表明将经常运动小鼠的血液输注到衰老小鼠体内,可明显促进海马神经再生。对于部分人群来说,运动具有奖赏的,促进他们进行更多、更长期的运动活动。
2022年12月14日宾夕法尼亚大学佩雷尔曼医学院Christoph A. Thaiss团队揭示了机体驱动运动动机的内在机制:肠脑轴信号通过促进纹状体多巴胺的释放调控运动行为。

1
肠道菌群调控小鼠运动能力
研究人员对8个确定品系的199种多样性离系繁殖小鼠进行转轮训练,通过基因组学分析发现基因对小鼠的运动能力影响很小。经过运动训练的小鼠在接受抗生素处理后其运动技能减弱,此外,将运动训练后的小鼠肠道菌群移植到无菌小鼠中可增强其运动能力。
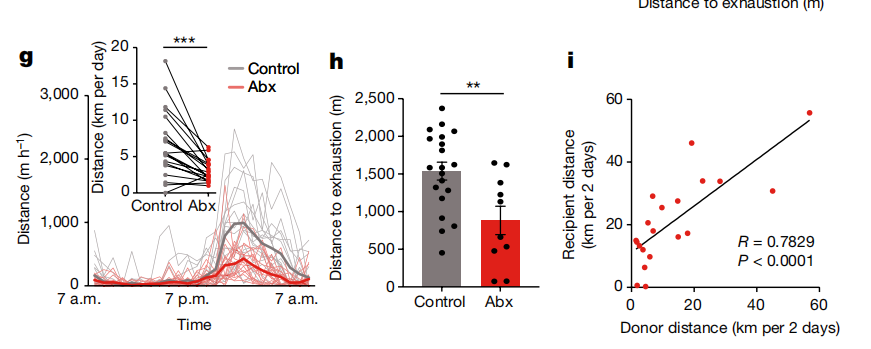
图1:接受抗生素处理后小鼠运动技能减弱
2
纹状体多巴胺驱动小鼠运动
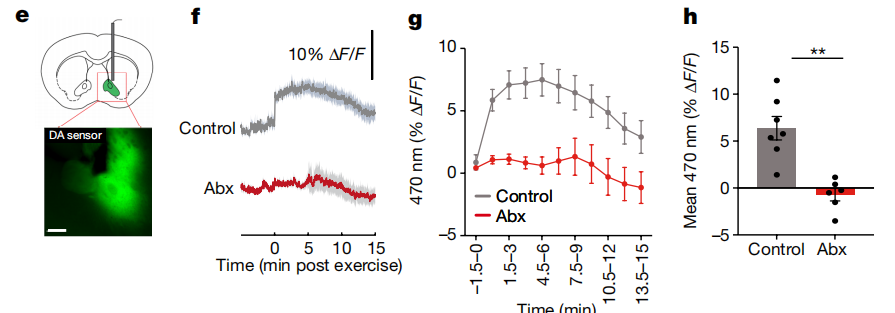
纹状体是驱动动机行为的关键脑区。在运动训练后纹状体神经元活性增加,多巴胺释放增加,在使用抗生素清除肠道微生物后运动并不能激活纹状体神经元,也不促进多巴胺释放。通过多巴胺受体激动剂激活多巴胺受体后可逆转抗生素引起的运动能力下降。
此外,多巴胺受体拮抗剂抑制多巴胺受体或通过化学遗传学慢性抑制VTA区域多巴胺神经元活性后可引起小鼠运动能力减弱,模拟出抗生素的行为效果。单胺氧化酶(MAO)介导多巴胺的降解,运动训练后小鼠纹状体中MAO表达降低。抑制MAO活性后可逆转抗生素引起的运动能力减弱。
3
肠道分泌代谢激活感觉神经元实现调控运动能力
肠道可通过微生物代谢产物或者传入神经元环路将信号传入到大脑中。大部分脊髓和迷走神经传入神经元表达离子通道受体TRPV1 ,研究人员发现在损毁TRPV1 阳性感觉神经元或抑制其活性后小鼠运动能力出现障碍。低剂量TRPV1 受体激动剂可明显改善抗生素引起的运动能力障碍。
此外,运动训练可激活背根神经节区域感觉神经元,抗生素处理后可减少该区域神经元的激活,这就表明脊髓TRPV1 阳性感觉神经元可感知肠道微生物来源的信号。
研究人员进一步通过代谢组学技术发现能够激活背根神经节区域感觉神经元的微生物代谢产物-脂肪酸酰胺(FAAs)。小鼠在进食FAAs后能够有效缓解抗生素引起的运动能力障碍。
已有研究表明FAAs的部分代谢产物可作为内源性大麻素CB1受体的激动剂。背根神经节区域TRPV1 阳性感觉神经元富集表达CB1,在敲除CB1小鼠中,运动并不会激活TRPV1 阳性感觉神经元,也不会促进纹状体多巴胺的释放。外周CB1受体拮抗剂抑制小鼠的运动能力,在激活纹状体多巴胺信号后可重新获得运动能力。此外,CB1受体激动剂促进小鼠的运动能力。
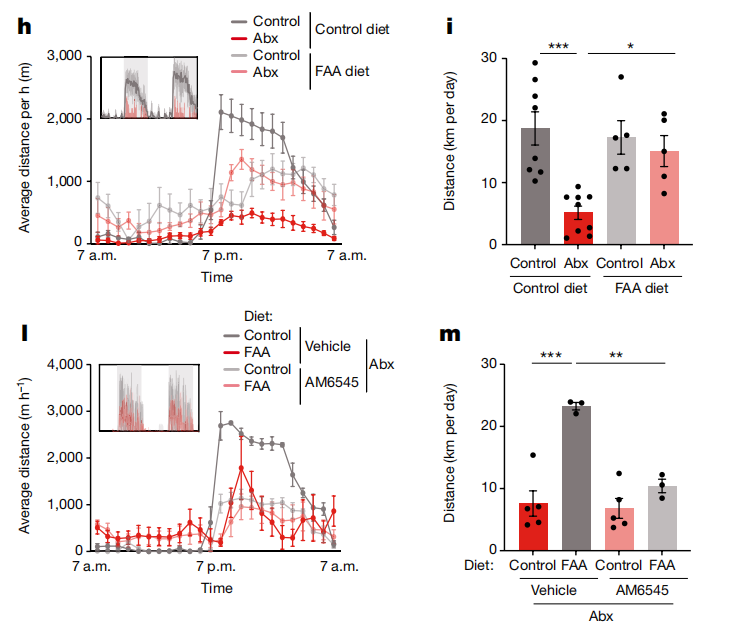
图3:肠道代谢产物FAA促进小鼠运动能力
总结
本文揭示了肠道菌群通过产生脂肪酸酰胺等物质,激活外周TRPV1 阳性感觉神经元,促进纹状体多巴胺的释放,增强运动的动机行为。
原始出处:
Dohnalová, L., Lundgren, P., Carty, J.R.E. et al. A microbiome-dependent gut–brain pathway regulates motivation for exercise. Nature 612, 739–747 (2022). https://doi.org/10.1038/s41586-022-05525-z.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言