鞘氨醇激酶2抑制剂Opaganib治疗COVID-19:II/III期研究已在墨西哥获得批准
2020-08-12 Allan MedSci原创
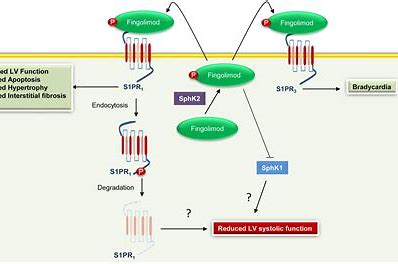
Opaganib是一款口服的鞘氨醇激酶2(SK2)选择性抑制剂,具有抗癌、抗炎和抗病毒活性,针对多种肿瘤、病毒、炎性和胃肠道适应症。
生物制药公司RedHill今日宣布,已获得墨西哥联邦卫生风险保护委员会(COFEPRIS)的批准,以开展Opaganib(Yeliva®,ABC294640)治疗重症SARS-CoV-2感染患者的II/III期临床试验。RedHill的研究现已在墨西哥、英国和俄罗斯获得批准,并且正在意大利、巴西和其他国家/地区进行审查,计划将研究进一步扩展到其他国家。
RedHill的首席运营官Raday说:“随着感染的激增,带来了新的严重病例,药物开发者必须通过严格设计和快速实施的研究来应对。Opaganib是目前正在测试用于治疗重症COVID-19的新型疗法之一”。
这项多中心、随机、双盲、平行臂、安慰剂对照的II/III期研究(NCT04467840)旨在招募多达270名需要住院治疗和补充氧气的重症COVID-19肺炎患者。受试者将以1:1的比例随机分配,以接受opaganib或安慰剂,以及护理标准疗法。该研究的主要终点是在第14天之前评估需要插管和机械通气的患者比例。
同时,opaganib的美国II期临床研究的注册已完成约50%,预计将于本月完成。这项随机、双盲、安慰剂对照研究(NCT04414618)旨在招募多达40例需要住院治疗和补充氧气的重症COVID-19肺炎患者。
Opaganib是一款口服的鞘氨醇激酶2(SK2)选择性抑制剂,具有抗癌、抗炎和抗病毒活性,针对多种肿瘤、病毒、炎性和胃肠道适应症。通过抑制SK2,Opaganib影响与癌症生长、病毒复制和病理性炎症相关的多种细胞途径。Opaganib最初是由Apogee Biotechnology开发,已完成了多项临床前研究和I期临床研究,涉及肿瘤学和炎症。
先前,Opaganib从美国FDA获得了用于治疗胆管癌的孤儿药资格,并且正在评估治疗晚期胆管癌和前列腺癌的有效性。
原始出处:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#III#
49
#III期研究#
65
#AGA#
93
#2抑制剂#
73
#抑制剂#
66
#墨西哥#
53
#鞘氨醇激酶#
79
#获得批准#
61
#激酶#
55
#III期#
61