美国FDA一个月内批准的第二个抗菌素新药Sivextro预示抗生素新药研发的春天?
2014-06-23 佚名 美中药源
6月20日下午,一种新的恶唑烷酮类抗菌素Sivextro(tedizolid phosphate,磷酸泰地唑胺)获得美国FDA批准,用于治疗金黄色葡萄球菌(包括耐甲氧西林菌株、甲氧西林敏感菌株)和各种链球菌属和粪肠球菌等革兰氏阳性细菌引起的急性细菌性皮肤和皮肤结构感染(ABSSSI)。这是FDA继5月23日批准Dalvance(dalbavancin,达巴万星)之后批准用于治疗ABSSSI感染的第
6月20日下午,一种新的恶唑烷酮类抗菌素Sivextro(tedizolid phosphate,磷酸泰地唑胺)获得美国FDA批准,用于治疗金黄色葡萄球菌(包括耐甲氧西林菌株、甲氧西林敏感菌株)和各种链球菌属和粪肠球菌等革兰氏阳性细菌引起的急性细菌性皮肤和皮肤结构感染(ABSSSI)。这是FDA继5月23日批准Dalvance(dalbavancin,达巴万星)之后批准用于治疗ABSSSI感染的第二个抗菌素新药。
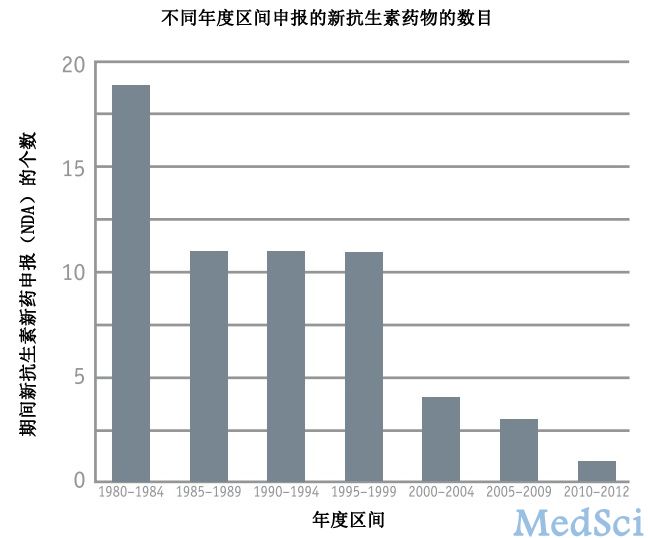
抗菌素是临床上使用最频繁的基本药物之一。由于历史原因造成的抗生素不规范使用,造成细菌对现有抗生素严重的抗药性。多药耐药(MDR)的细菌感染已经成为全球公共健康的主要威胁之一。正因为多药耐药,抗菌素的联合用药也日趋增多,药物-药物相互作用也增加了不良反应的发生风险。根据最近国家食药监总局发布的2013年国家药品不良反应监测年度报告,由抗菌素引起的不良反应高居不良反应/事件报告的首位。对目前绝大多数可用的抗生素都有抗药性的“超级细菌”也以惊人的速度在世界范围蔓延,。另一方面,新型有效的抗生素研发并没有伴随MDR细菌的增加而增加。根据美国FDA新药评价中心(CDER)的数据,自1980年以来新批准的抗生素数量反而在不断减少(见下图)。现有的抗菌素已经无法治愈日益增加的感染和耐药。
美国FDA一个月内批准的第二个抗菌素新药Sivextro预示抗生素新药研发的春天?
为了开发新型、有效的抗生素,控制多药耐药细菌的扩散以及保护公共健康的安全,现行抗生素激励(GAIN)条款作为美国FDA安全与创新法案的一部分也被写入法律,那些获得合格传染病产品(Qualified Infectious Disease Product,QIDP)认证的,用于治疗严重或危及生命感染的药物在获得食品,药品和化妆品法规定的(市场)排他期之外还享有额外5年的市场独占权。自此,抗生素药物的开发有明显增加的趋势。美国传染病协会(IDSA)已经和数十家机构合作,致力于10×20方案,目标在2020年能开发10个新的抗生素药物。
Sivextro(通用名:tedizolid磷酸盐,曾用名:TR-701)由Cubist制药公司开发,是一种恶唑烷酮类抗生素。Sivextro是一种前药,在体内可被磷酸酶迅速转化为具有生物活性的tedizolid。后者能够和细菌的核糖体50S亚基结合,从而抑制蛋白质的合成。尽管自2000年辉瑞的同类抗菌素利奈唑胺获得美国FDA批准以后,至少有10个同类化合物进入临床,但Sivextro是第一个获得FDA批准的二代恶唑烷酮类抗生素。和一代产品利奈唑胺相比,Sivextro对一些细菌的体外抑制活性要高2-8倍,安全性在一定程度上也有所提高。
在一个最近发表在《柳叶刀》子刊上的双盲三期临床实验中(ESTABLISH-2实验),667例怀疑或确认患有革兰氏阳性细菌感染的成人患者被随机分为Sivextro治疗组和现行金标利奈唑胺阳性对照组。Sivextro治疗组连续6天,每天一次口服200毫克的Sivextro和对照组连续10天,每天两次口服600毫克的利奈唑胺相比疗效无明细区分。在口服治疗之前,所有患者都接受短期的Sivextro或利奈唑胺的静脉输液治疗。在另一个有566位患者参与的三期实验中(NCT02066402),采用Sivextro和利奈唑胺治疗48-72小时后,治疗组和对照组的病灶面积都下降20%以上,达到一级实验终点。
2013年12月13日,Sivextro获得FDA的优先审查资格,处方药用户收费法(PDUFA)目标日期为2014年6月20日。2014年4月14日,FDA抗感染药物顾问委员会(AIDAC)以14:0的一致投票建议批准Sivextro。
原始出处:
Moran GJ, Fang E, Corey GR, Das AF, De Anda C, Prokocimer P.Tedizolid for 6 days versus linezolid for 10 days for acute bacterial skin and skin-structure infections (ESTABLISH-2): a randomised, double-blind, phase 3, non-inferiority trial.Lancet Infect Dis. 2014 Jun 5. pii: S1473-3099(14)70737-6.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#抗菌素#
79
#研发#
82
#抗菌#
73
#美国FDA#
90