Mol Cell:靶向SRPK1酶的抗癌药物
2012-06-25 Beyond 生物谷
近日,加州大学圣地亚哥医学院的研究人员发现一种新的专门调控RNA剪接的信号转导通路,RNA剪接是指从DNA模板链转录出的最初转录产物中除去内含子,并将外显子连接起来形成一个连续的RNA分子的过程。这一发现发表在2012年6月27日的Molecular Cell杂志上,该研究提示新发现的通路可能是一个新的抗癌药物作用环节。 早期研究证实SRPK1与癌症和其它人类疾病有关。例如SRPK1在调节血
近日,加州大学圣地亚哥医学院的研究人员发现一种新的专门调控RNA剪接的信号转导通路,RNA剪接是指从DNA模板链转录出的最初转录产物中除去内含子,并将外显子连接起来形成一个连续的RNA分子的过程。这一发现发表在2012年6月27日的Molecular Cell杂志上,该研究提示新发现的通路可能是一个新的抗癌药物作用环节。

早期研究证实SRPK1与癌症和其它人类疾病有关。例如SRPK1在调节血管内皮生长因子或血管内皮生长因子刺激血液肿瘤血管生长过程中起着关键作用。在许多癌症如肾脏、乳腺癌肺癌和胰腺癌等中SRPK1都被证实表达失调。
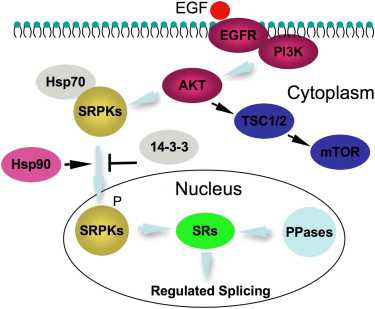
Fu和他的同事在这项新的研究中,发现了SRPK1存在于一个重要的细胞信号转导通路中,SRPK1在PI3K-Akt通路中发挥核心作用。
研究人员认为SRPK是疾病干预和治疗的一大新靶标。因为其核心作用,并且易被控制,抑制其活性可以有效抑制血管形成。

doi:10.1016/j.molcel.2012.05.014
PMC:
PMID:
The Akt-SRPK-SR Axis Constitutes a Major Pathway in Transducing EGF Signaling to Regulate Alternative Splicing in the Nucleus
Zhihong Zhou, Jinsong Qiu, Wen Liu, Yu Zhou, Ryan M. Plocinik, Hairi Li, Qidong Hu, Gourisanker Ghosh, Joseph A. Adams, Michael G. Rosenfeld, Xiang-Dong Fu
Pre-mRNA splicing is regulated by developmental and environmental cues, but little is known about how specific signals are transduced in mammalian cells to regulate this critical gene expression step. Here, we report massive reprogramming of alternative splicing in response to EGF signaling. By blocking individual branches in EGF signaling, we found that Akt activation plays a major role, while other branches, such as the JAK/STAT and ERK pathways, make minor contributions to EGF-induced splicing. Activated Akt next branches to SR protein-specific kinases, rather than mTOR, by inducing SRPK autophosphorylation that switches the splicing kinases from Hsp70- to Hsp90-containing complexes. This leads to enhanced SRPK nuclear translocation and SR protein phosphorylation. These findings reveal a major signal transduction pathway for regulated splicing and place SRPKs in a central position in the pathway, consistent with their reputed roles in a large number of human cancers.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#Cell#
56
#CEL#
48
#抗癌药物#
66
#抗癌药#
59