Nat Med:陈列平团队确定免疫治疗新靶标!又一条肿瘤免疫逃逸通路现形!
2019-03-07 Ruthy 转化医学网
迄今为止,“谈癌色变”依旧是常态。大多数恶性肿瘤患者在确诊时已处于晚期,失去了手术机会,而肿瘤免疫逃逸的恶果始终难以遏制,导致肿瘤对许多传统疗法不敏感,预后不佳,因此,在很多人眼中“患癌”就是接到了“阎王令”。
导 读
迄今为止,“谈癌色变”依旧是常态。大多数恶性肿瘤患者在确诊时已处于晚期,失去了手术机会,而肿瘤免疫逃逸的恶果始终难以遏制,导致肿瘤对许多传统疗法不敏感,预后不佳,因此,在很多人眼中“患癌”就是接到了“阎王令”。近几年来,免疫治疗因其可大力阻断肿瘤免疫逃逸而成为恶性肿瘤治疗的“杀手锏”,其中PD1/PDL-1抗体疗法更是广受好评。近日,美国耶鲁大学的华人科学家陈列平教授团队又发现了一条全新肿瘤免疫逃逸通路!并确定了未来免疫治疗的新靶标!相关结果发表于著名学术期刊《Nature Medicine》上。
肿瘤治疗难点——免疫逃逸
我们知道,机体免疫系统具有免疫监视功能,正常情况下,当体内出现恶变细胞时,免疫系统能够识别并通过免疫机制特异地清除这些“非己”细胞,抵御肿瘤的发生发展。而当恶变细胞在某些情况下通过多种机制逃避机体的免疫监视时,就会在体内迅速增殖,形成肿瘤。这些机制中最为引人注意的就是PD1/PDL-1通路。
PD-1全名为程序性死亡受体-1,主要表达于激活的T细胞表面。PD-L1是PD-1的配体,在正常情况下其功能是与T细胞表面的PD-1结合,从而抑制T细胞激活,以避免因T细胞过度激活而引起自身免疫病。而肿瘤细胞在其进化过程中会选择性高表达PD-L1,从而抑制T细胞功能,使其丧失对肿瘤细胞的杀伤能力,这就是典型的肿瘤免疫逃逸途径之一。想要彻底遏制这一过程,就必须特异性阻断PD-L1与PD-1的结合,重新激活T细胞,恢复后者的肿瘤杀伤作用,这也是正常化免疫治疗的最佳途径。所谓正常化免疫治疗就是“打通”机体正常免疫系统的反应通路、重置肿瘤微环境(TME)免疫活动,而非一昧加强免疫功能,从而以最小的身体伤害遏制肿瘤进展。如何实现这一切呢?关键自然是找到靶标。
Siglec-15——新型T细胞活性调节剂
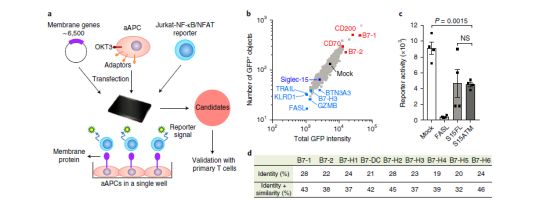
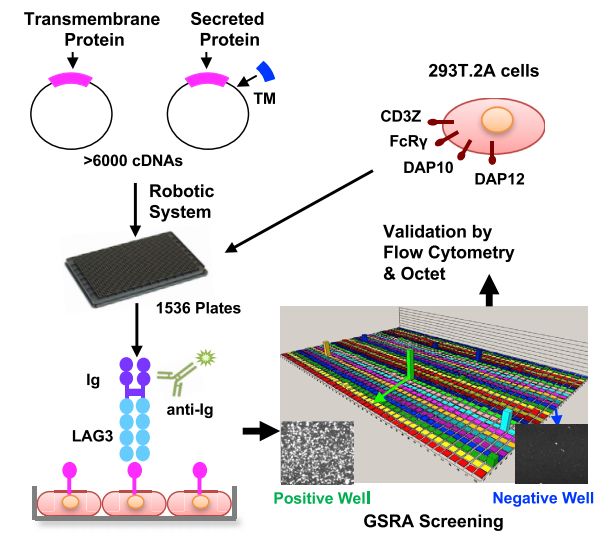
近年来已有不少相关靶标问世,极大地促进了肿瘤免疫治疗的发展。陈列平教授团队在先前研究的基础上,构建了一个包含超过6500个人类基因的高通量功能筛选系统(TCAA),设计了一种人工抗原呈递细胞系(aAPC),使用Jurkat T细胞来检测靶基因的功能及其对T细胞活性的影响,并由稳定表达的由NF-κB或NFAT反应元件驱动的绿色荧光蛋白(GFP)报告候选基因的调节效果。研究人员通过验证一些已经被报道的共刺激分子、凋亡相关基因或共抑制分子的功能证明了TCAA系统的准确性。

Siglec-15可作为TCAA的T细胞抑制因子
研究结果显示,Siglec-15可持续地抑制T细胞活性,并有可能满足正常化免疫治疗的主要特征。这是如何实现的呢?
他们发现,在大多数正常人体组织和各种免疫细胞亚群中Siglec-15mRNA只有极少量表达,但在巨噬细胞中可觅得其踪迹。Siglec-15 的细胞外结构域(ECD)中含有免疫球蛋白可变区(IgV)和2型恒定区(IgC2)区,这与T细胞的B7基因家族有超过30%的同源性,这意味着Siglec-15有可能与B7家族成员共享免疫调节功能。
Siglec-15通过调节细胞生长抑制T细胞应答
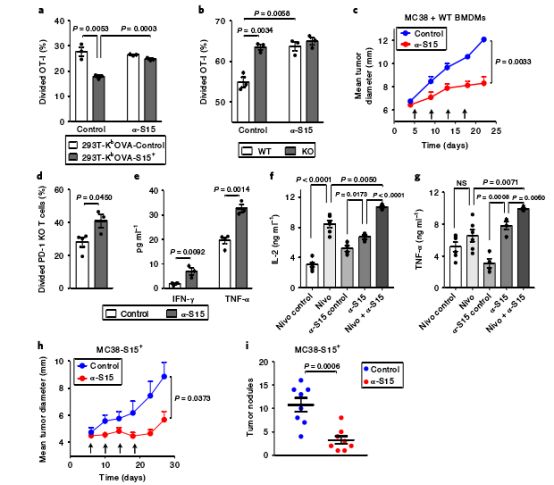
小鼠实验证明巨噬细胞上的Siglec-15可以抑制体内T细胞反应,其并不影响T细胞凋亡,而是通过调节细胞生长抑制T细胞的特异性应答。而且,Siglec-15基因敲除后并不会导致小鼠自身免疫疾病或其他症状,换言之,抑制Siglec-15是一条相对安全的抗癌途径。
随后,研究人员将肿瘤细胞接种到Siglec-15基因敲除小鼠体内,发现这些小鼠的肿瘤生长缓慢,生存期延长,CD8+T细胞,NK细胞的浸润也相应增多。他们将抗Siglec-15单克隆抗体α-S15用在多种小鼠肿瘤模型中,发现α-S15可成功阻断Siglec-15的免疫抑制作用,进而提高体内抗肿瘤免疫反应。这就证明了Siglec-15作为免疫治疗新靶标的可行性!
α-S15对肿瘤细胞的作用
虽然目前Siglec-15抑制剂仍在临床实验中,但Siglec-15作为免疫治疗靶点无疑为主流癌症免疫治疗提供了不容忽视的助力,相信在不久的将来,通过更深入的机制研究、更广泛的临床探索,能够让肿瘤免疫疗法开启下一个新时代,让攻克癌症不再是天方夜谭。
原始出处:Wang J1, Sun J1, Liu LN2, et al. Siglec-15 as an immune suppressor and potential target for normalization cancer immunotherapy. Nat Med. 2019 Mar 4.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#Nat#
79
#靶标#
96
#Med#
94