读书报告 | TITAN-RCC研究:纳武利尤单抗±伊匹木单抗作为转移性肾癌的免疫强化治疗
2024-03-29 iCombo iCombo 发表于上海
与纳武利尤单抗联合伊匹木单抗一线治疗的CheckMate-214方案相比,TITAN-RCC研究客观缓解率和完全缓解率略低,但中位无进展生存期几乎减半,中位总生存期更短。
导读
基于CheckeMate-214和CheckMate-025 III期研究,纳武利尤单抗联合伊匹木单抗被批准为中风险或低风险转移性肾细胞癌的一线方案。纳武利尤单抗单药治疗作为所有风险组的二线治疗。
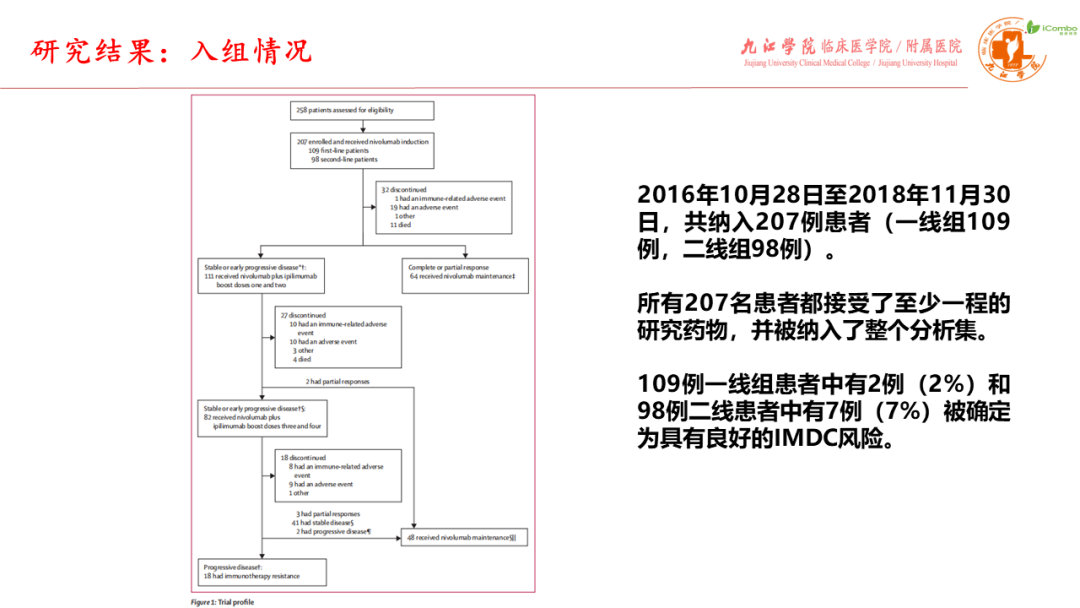
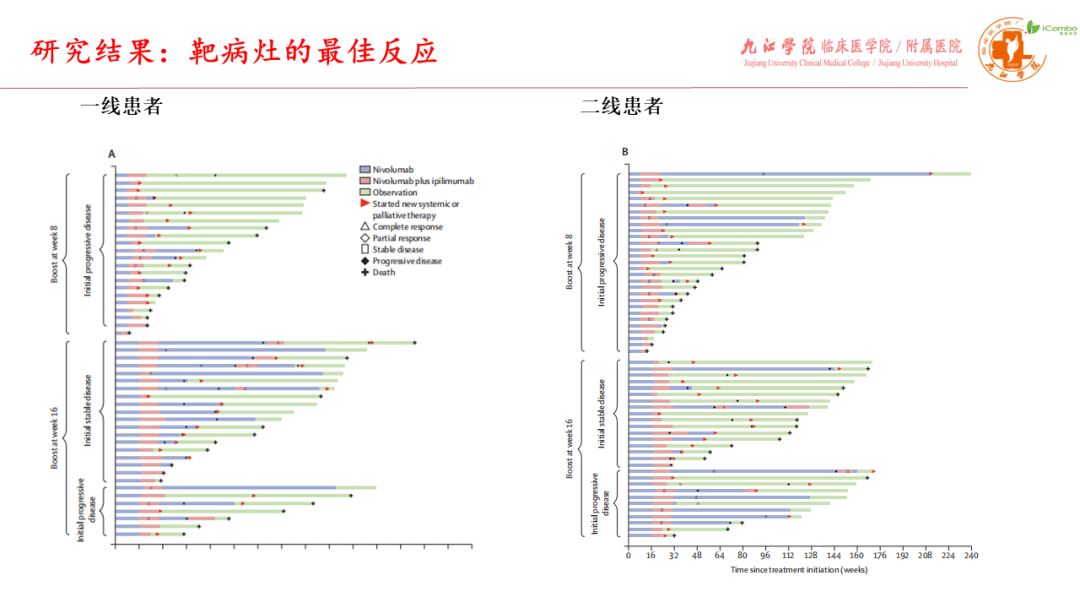
TITAN-RCC研究评估免疫免疫强化治疗作为中风险和低风险转移性透明细胞肾细胞癌患者的一线和二线治疗的有效性和安全性。研究设计为纳武利尤单抗诱导治疗,若在第8周时肿瘤进展或到16周肿瘤无应答者,纳武利尤单抗联合伊匹单抗2-4程,以后纳武利尤单抗维持治疗到进展为止。
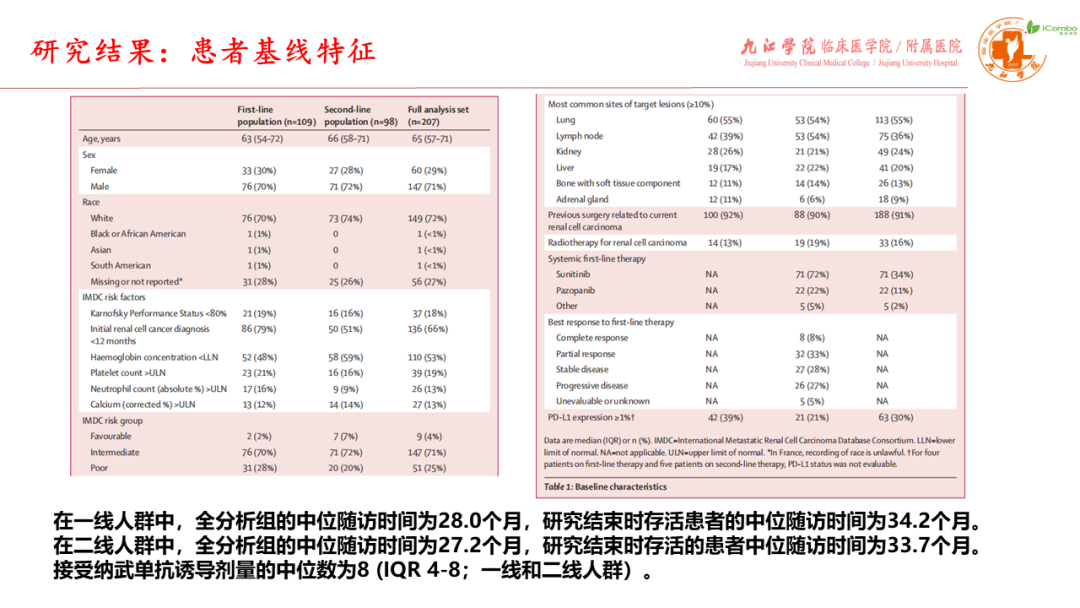
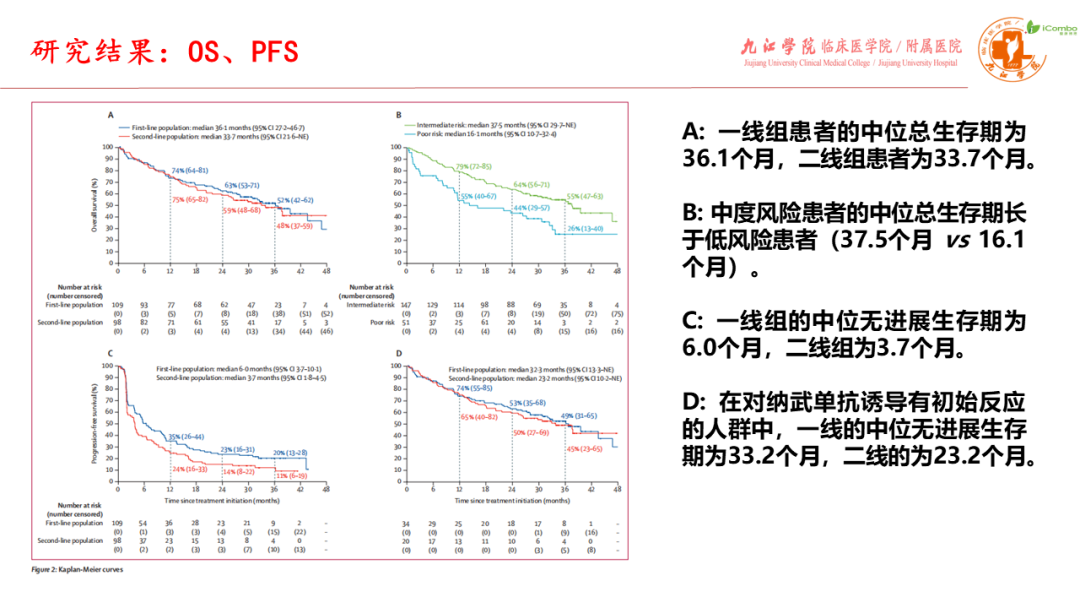
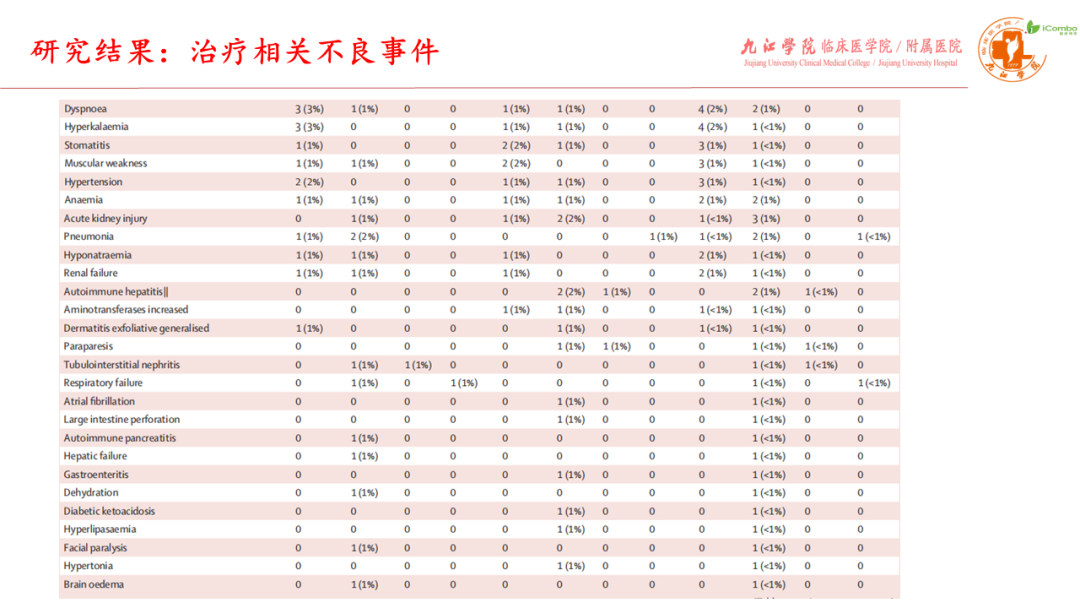
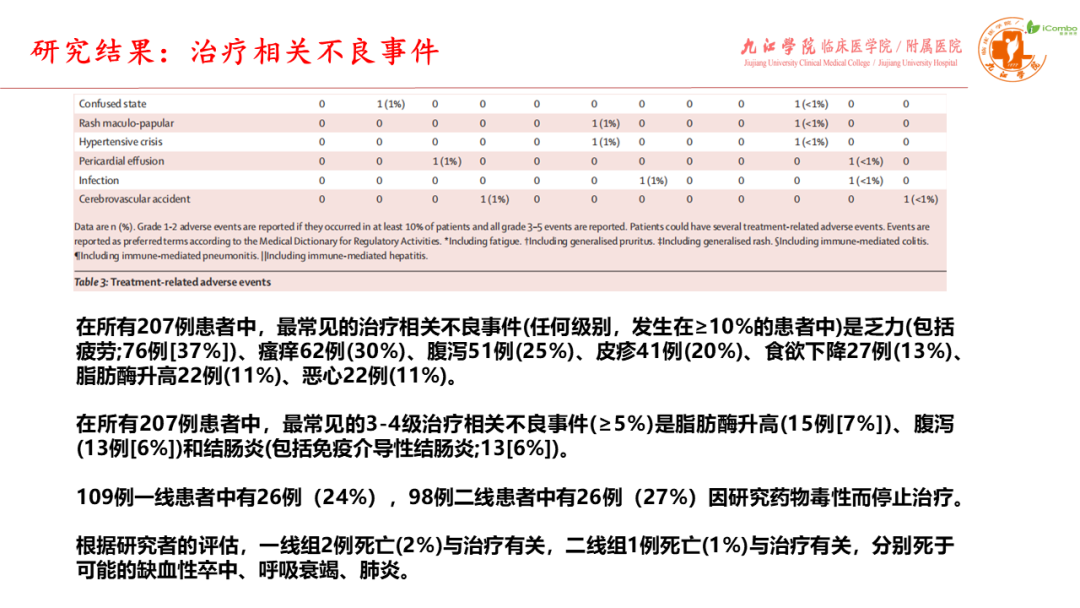
研究入组207例中危或高危晚期肾透明细胞癌患者,其中一线治疗者109例,既往TKI抑制剂或伊维莫司治疗失败的二线患者98例。 纳武利尤单抗诱导后第8或16周时确认的ORR:一线组28%(2% CR),二线组18% (无CR)。纳武利尤单抗±纳武利尤单抗联合伊匹木单抗治疗后,一线组与二线组的确认ORR分别为36%(7% CR)与32%(6% CR)。一线组的中位PFS为6.0个月,二线组为3.7个月。一线组的中位OS为36.1个月,二线组为33.7个月。
结论:与纳武利尤单抗联合伊匹木单抗一线治疗的CheckMate-214方案相比,TITAN-RCC研究客观缓解率和完全缓解率略低,但中位无进展生存期几乎减半,中位总生存期更短。
与二线纳武利尤单药(CheckMate-025)相比,TITAN-RCC方案的疗效有所改善,客观缓解率为32% vs 23%,完全缓解率为6% vs 1%,中位总生存期为33.7个月vs 25.8个月。最常见的3-4级治疗相关不良事件(≥5%)是脂肪酶升高、结肠炎和腹泻。因此,与已批准的纳武利尤单抗联合伊匹单抗相比,总体疗效较差。对于二线治疗,纳武利尤单抗联合伊匹单抗可能是已批准的纳武利尤单抗单药治疗进展的挽救策略( Lancet Oncol. 2023 Nov;24(11):1252-1265. doi: 10.1016/S1470-2045(23)00449-7)。












本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#纳武利尤单抗# #伊匹木单抗# #转移性肾癌#
49