美国批准罗氏公司旗下新型全肿瘤液体活检测试平台
2020-08-30 Allan MedSci原创
美国监管机构已批准罗氏针对实体瘤患者进行的新型全肿瘤液体活检测试平台(FoundationOne Liquid CDx),这将为无法进行组织活检的患者提供替代选择。
美国监管机构已批准罗氏针对实体瘤患者进行的新型全肿瘤液体活检测试平台(FoundationOne Liquid CDx),这将为无法进行组织活检的患者提供替代选择。FoundationOne Liquid CDx是一种基因组分析(CGP)测试,可分析300多个与癌症相关的基因和多个基因组特征,以识别肿瘤内的基因突变并优化患者护理。
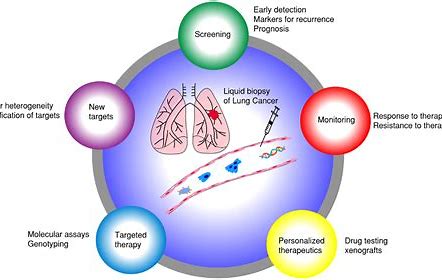
FoundationOne Liquid CDx能够分析患者血液样本中循环的无细胞DNA,并使用大规模并行测序来检测四大类基因组改变。监管机构还批准了该测试用以识别可能受益于某些前列腺癌和肺癌疗法的患者,包括Rubraca(rucaparib)和三种一线酪氨酸激酶(TKI)抑制剂。
罗氏执行副总裁,首席医学官Levi Garraway表示:“许多癌症患者无法进行组织活检。FoundationOne Liquid CDx可能为原本可能无法从全面基因组分析中受益的患者提供微创治疗方案。检测血液样本的便利性还可以使治疗决策更加迅速,从而使患者放心,减少时间的浪费,为高效治疗争取时间”。
原始出处:
http://www.pharmatimes.com/news/us_approves_roches_new_pan-tumour_liquid_biopsy_test_1347425
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#美国批准#
100
#活检#
97
好的
0