细胞的N种死亡方法----因为死亡才有重生!
2016-02-10 老狼 癌图腾
生存还是死亡,我们身体中的细胞每天都在做着这样的选择——不仅是选择是否死去,还选择了如何死去。它们可以选择安静地死亡,或是大掀风浪。细胞死亡是生命现象不可逆停止及生命的结束,正常的组织中经常发生细胞死亡,是维持组织机能和形态所必须的,主要细胞死亡方式汇总如下: 自杀——为了身体整体的利益 生物体发育过程中普遍存在着由宿主决定的细胞自觉有序的死亡现象,当细胞遇到内、外环境因子刺激
生存还是死亡,我们身体中的细胞每天都在做着这样的选择——不仅是选择是否死去,还选择了如何死去。它们可以选择安静地死亡,或是大掀风浪。细胞死亡是生命现象不可逆停止及生命的结束,正常的组织中经常发生细胞死亡,是维持组织机能和形态所必须的,主要细胞死亡方式汇总如下:
自杀——为了身体整体的利益
生物体发育过程中普遍存在着由宿主决定的细胞自觉有序的死亡现象,当细胞遇到内、外环境因子刺激时,主动启动基因调控的自杀保护措施,通过这种方式去除体内非必需细胞或即将发生特化的细胞。细胞自杀无炎症反应,不遗留瘢痕。死亡的细胞碎片很快被巨噬细胞或邻近细胞回收再利用或清除,不影响其他细胞的正常功能。在正常情况下,我们身体内细胞的死亡大都是程序性死亡,这可以让新生的细胞取代衰老的细胞,让我们的身体保持健康。
细胞凋亡(apoptosis):这种死亡是细胞的一种生理性、主动性的“自觉自杀行为”。 生物体内细胞在特定的内源和外源信号诱导下,其死亡途径被激活,并在有关基因的调控下发生的程序性死亡过程。意指细胞的死亡犹如秋天的树叶或花瓣的凋落的死亡方式, 1973 年 Kerr 和 Wyllin 最先提出这一概念。细胞凋亡的过程大致可分为以下几个阶段:接受凋亡信号→凋亡调控分子间的相互作用→蛋白水解酶的活化(Caspase)→进入连续反应过程;
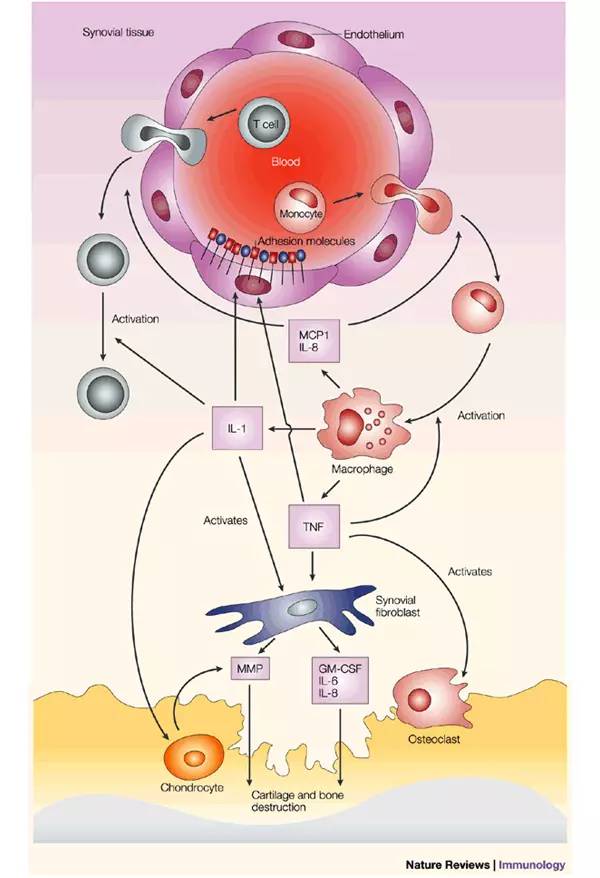
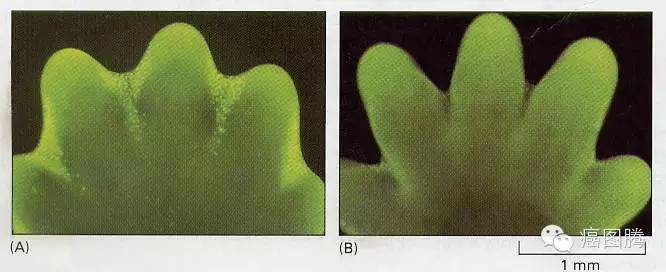
手指或脚趾的发育及青蛙尾巴的退化都是细胞凋亡的结果
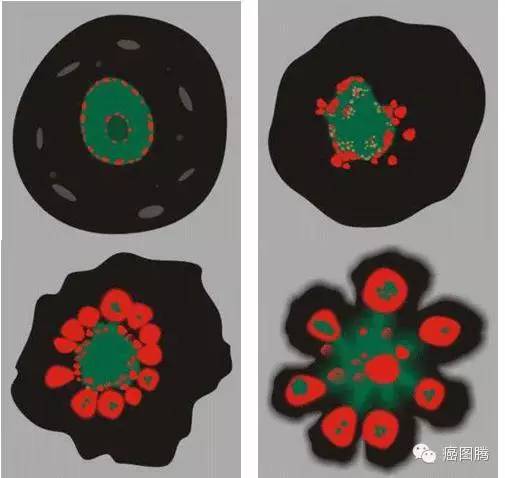
细胞凋亡动态图
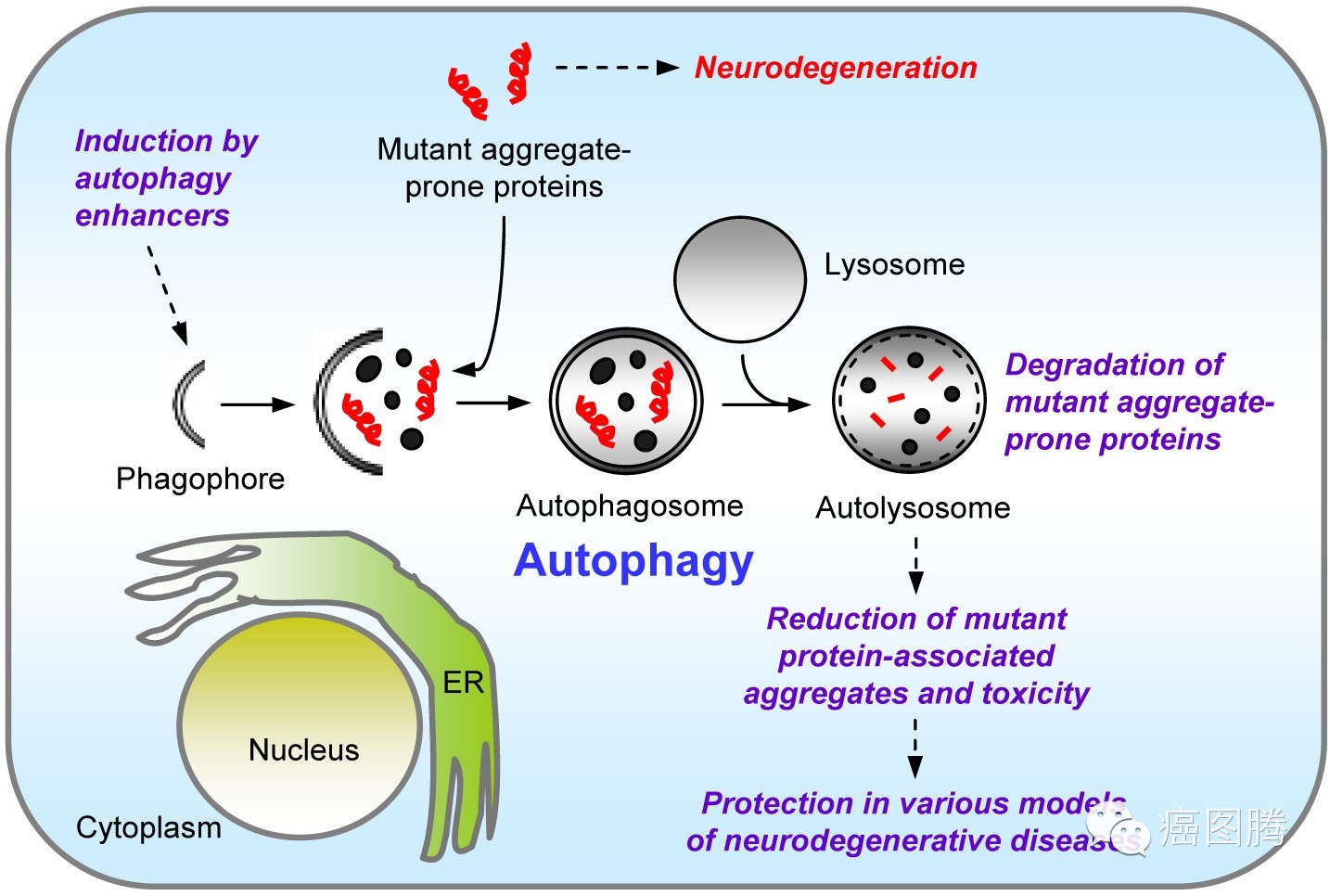
细胞自噬(Autophagy)一些损坏的蛋白或细胞器被双层膜结构的自噬小泡包裹后,送入溶酶体(动物)或液泡(酵母和植物 )中进行降解并得以循环利用。1966年Duve和Wattiaux在发现溶酶体的同时发现了细胞的自吞噬现象,1977年Mortimore和Schworer发现肝细胞在处于饥饿状态时,自吞噬对其维持自身的稳态发挥着至关重要的作用;
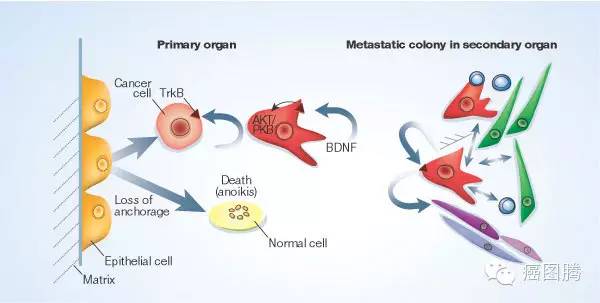
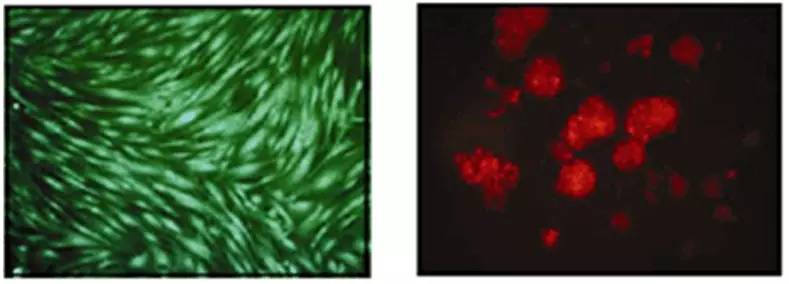
失巢凋亡(anoikis: suspension-induced apoptosis):正常的贴壁细胞如果长时间处于悬浮状态就会因“无家可归”而死亡。这是一种形式的细胞程序死亡,由与细胞外基质和其他细胞脱离接触而诱发的;这种细胞死亡形式在1994年被首次命名为失巢凋亡。失巢凋亡对维持机体组织稳定状态是不可缺少的,它的主要作用是防止细胞异常生长或细胞黏附到异常的细胞外基质上。抵抗失巢凋亡是肿瘤转移的一个特点,能使肿瘤细胞通过循环系统扩散到远处的其他器官.肿瘤细胞在脱离细胞外基质的黏附和细胞间的接触后,通过旁自分泌以及旁分泌机制抵抗凋亡得以存活,并重新获得附着能力得以扩散、转移和侵袭。
{nextpage}
他杀——君要臣死臣不得不死
免疫系统发现并清除异物、外来病原微生物、处死病变细胞等引起内环境波动的因素,粒细胞、巨噬细胞、淋巴细胞等通过多种方式来处死一些细胞来维持系统内环境稳定。但免疫功能的亢进会对自身器官或组织产生伤害,造成自身免疫性疾病。
吞噬死亡(phagocytosis):在哺乳动物体内中性颗粒白细胞和巨噬细胞担任机体中的保护防御任务。免疫细胞既可以吞噬感染的病毒、细菌或其它一些颗粒,也可以对衰老的、进入编程死亡的细胞的吞噬。如占成人细胞总数1/4的红细胞仅能成活120天, 因此人体每天必须清除大量衰老的红细胞,这主要是靠吞噬作用即溶酶体酶的消化作用来完成。
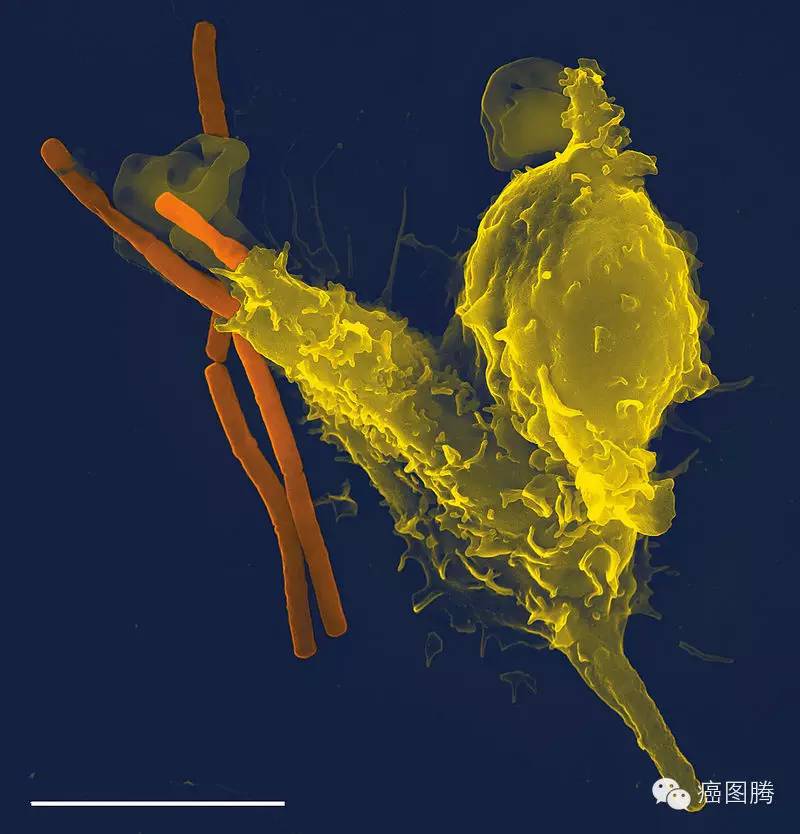
白细胞吞噬细菌
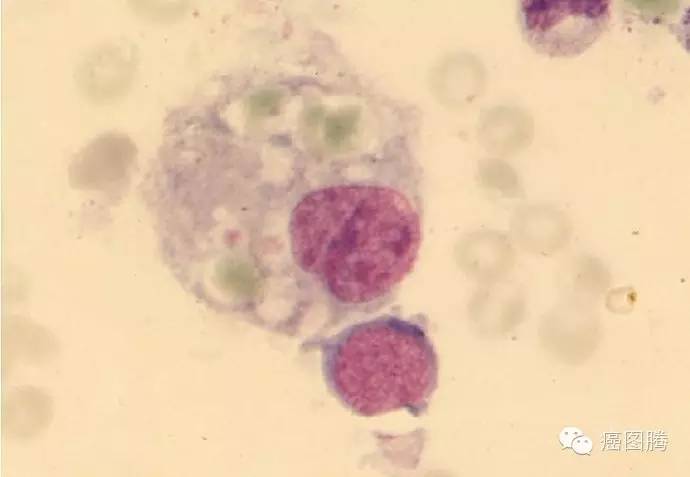
红细胞被吞噬
免疫杀伤( immune killing):T细胞、B细胞和NK细胞等淋巴细胞可介导机体的细胞免疫、体液免疫和对肿瘤细胞和病毒感染细胞的杀伤作用等免疫学功能。

抗原呈递
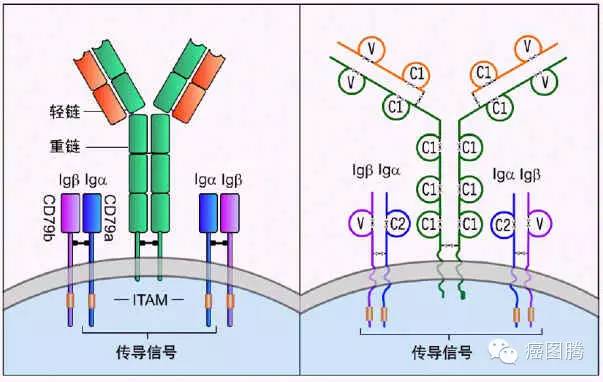
B细胞表面分子
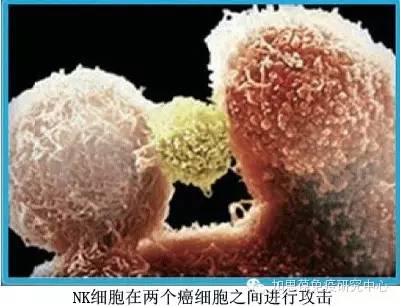
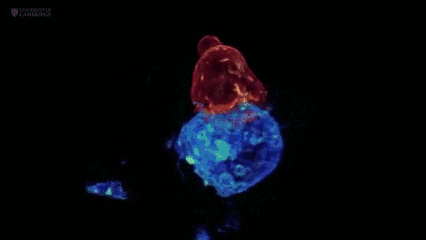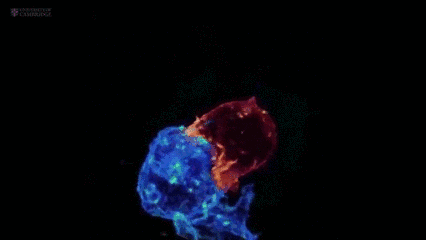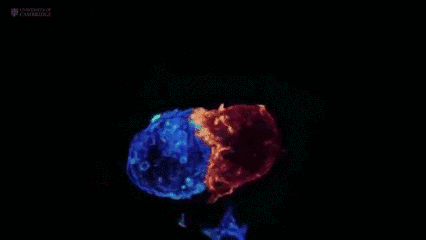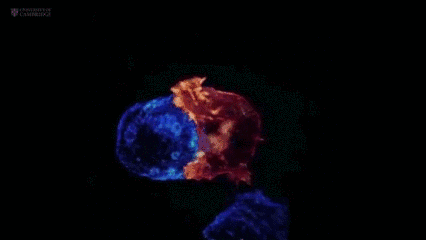
毒性T-细胞攻击肿瘤细胞
{nextpage}
意外事件死亡
细胞遭遇到异常的物理、化学及生物因素影响,有的细胞会当即毙命,有的会选择一些奇葩的死法,细胞意外死亡会带来炎症反应和机体功能障碍。
细胞坏死(Necrosis:accidental cell death/cell lysis)是活体内范围不等的局部细胞死亡,死亡细胞的质膜(细胞膜、细胞器膜等)崩解、组织自溶(坏死细胞被自身的溶酶体消化),并引发急性炎症反应。细胞受到化学因素(如强酸、强碱、有毒物质)、物理因素(如热、辐射)和生物因素(如病原体)等环境因素的伤害,引起细胞死亡的现象;
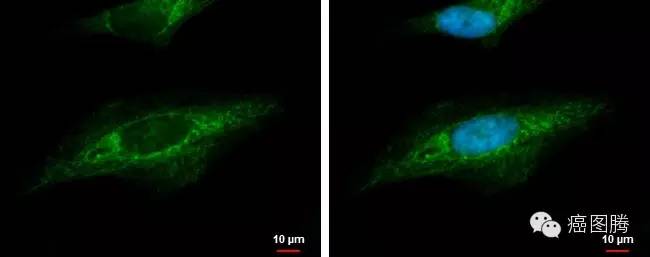
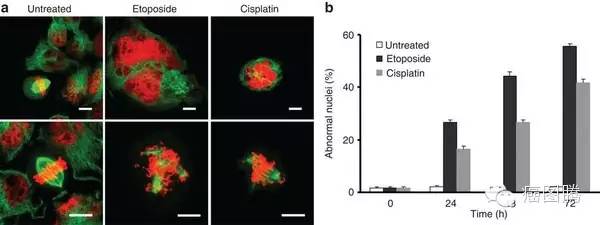
有丝分裂的灾难(Mitotic catastrophe)在DNA发生损害时,细胞无法进行完全的分裂从而导致四倍体或多倍体的现象。1989年,Lisa Molz等发现在酵母的一种对热敏感的突变株中,细胞分裂时染色体分离发生异常;
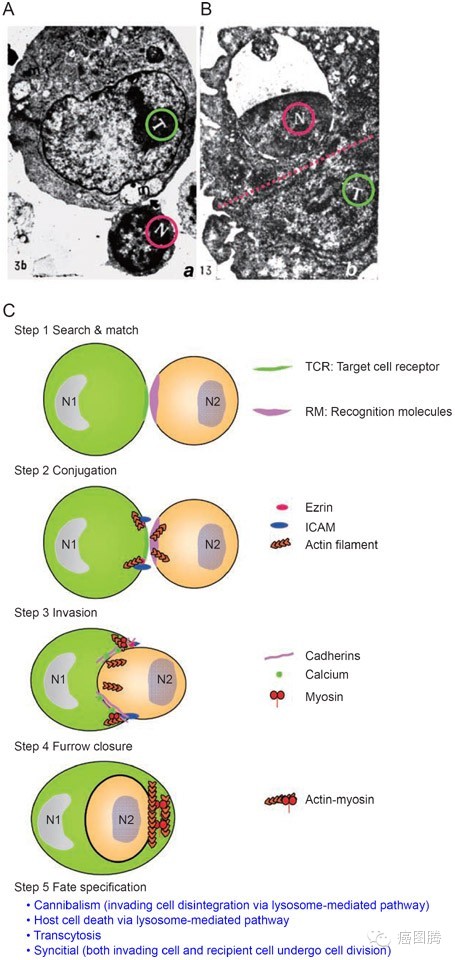
并入死亡(entosis),即有些细胞会进入到其它细胞中,然后死亡。科学家称,这种新形式有可能成为一种抑制肿瘤的新方法。相关论文2007年11月30日发表于《细胞》(Cell)上;
兴奋性中毒(Excitotoxicity)谷氨酸酯及其类似物质等神经递质的过度刺激,使神经细胞受损及死忘的病理过程;
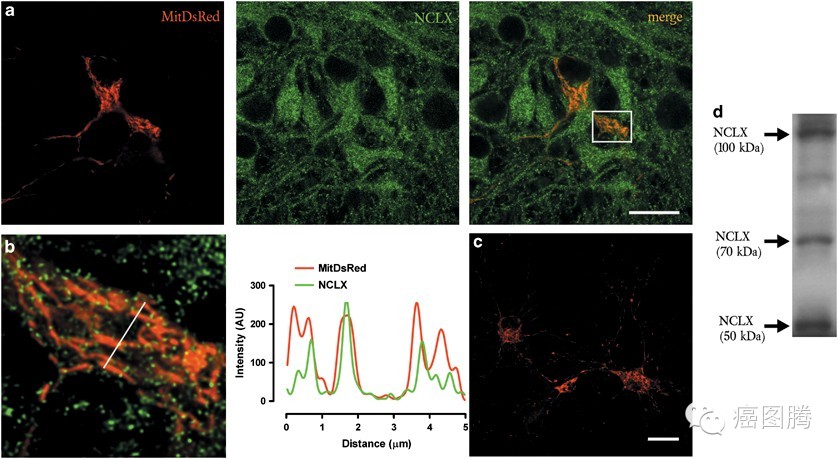
{nextpage}
非典型性细胞死亡
当细胞凋亡不能正常发生而细胞必须死亡时,细胞采用一些不同于典型的凋亡和坏死的细胞死亡方式的“替补”方案,这些死亡方式不依赖半胱氨酸家族蛋白酶路径,可引发炎症反应在内的重要生理功能。
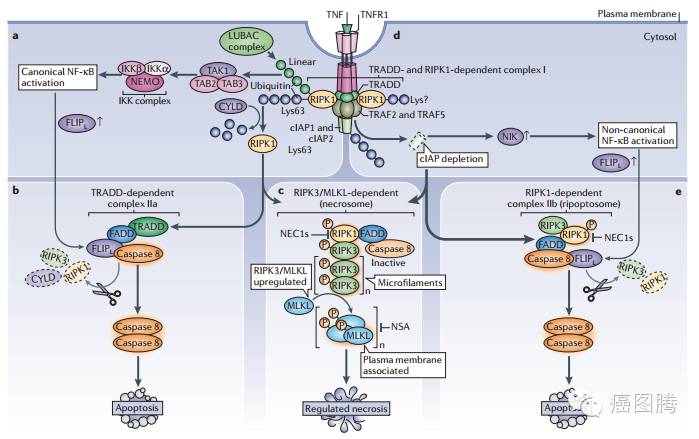
坏死性凋亡(necroptosis):是一种“受控”的死亡类型,不依赖于半胱氨酸家族蛋白酶活化的路径,在这些类型的细胞死亡中,细胞会破裂,细胞内容物被释放。它在向细胞下达死亡指令的同时,刺激了一种炎症反应让免疫系统知道出现了一些问题。然而,当这一细胞死亡信号通路开始出现失控时,它可以导致炎症性疾病。坏死性凋亡还牵涉到神经退行性疾病、失血引起的脑损伤,克隆氏病、多发性硬化症、急性心衰,以及某些病毒感染。
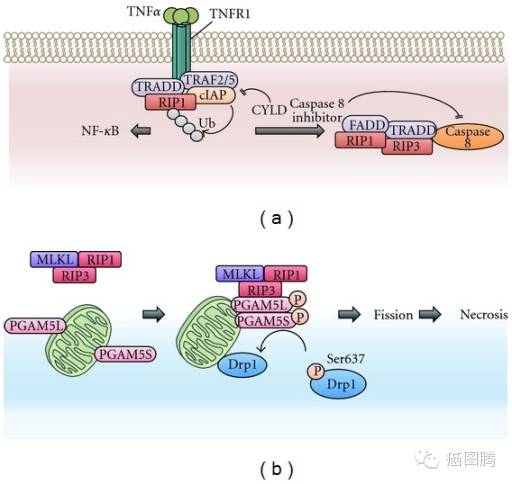

细胞焦亡(Pyroptosis )一种微生物感染等引起的程序性细胞死亡方式,其特征为依赖于半胱天冬酶-1,并伴有大量促炎症因子的释放.细胞焦亡的形态学特征、发生及调控机制等均不同于凋亡、坏死等其他细胞死亡方式。细胞焦亡广泛参与感染性疾病、神经系统相关疾病和动脉粥样硬化性疾病等的发生发展。
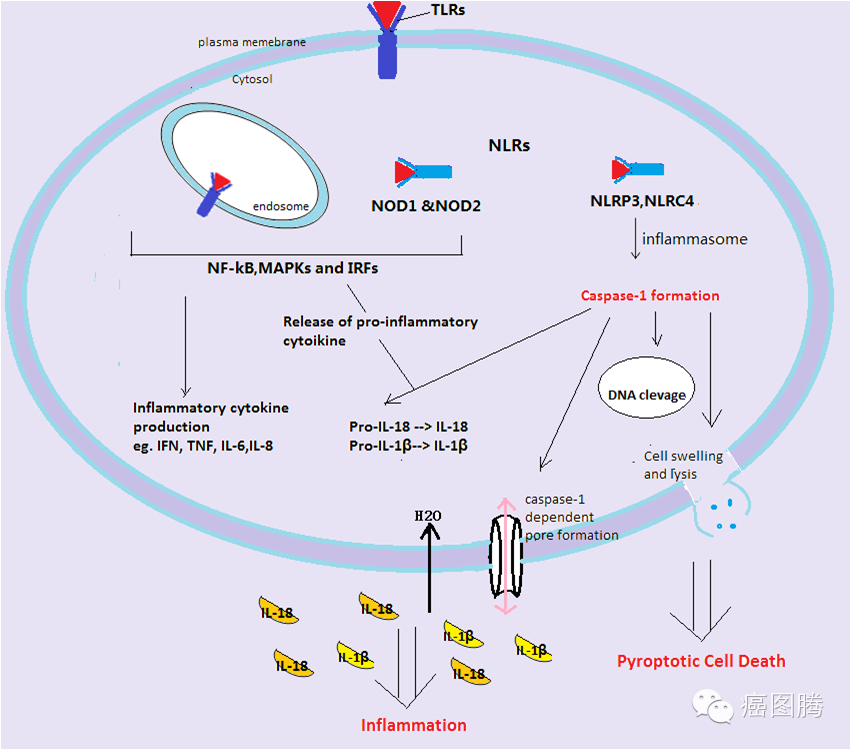
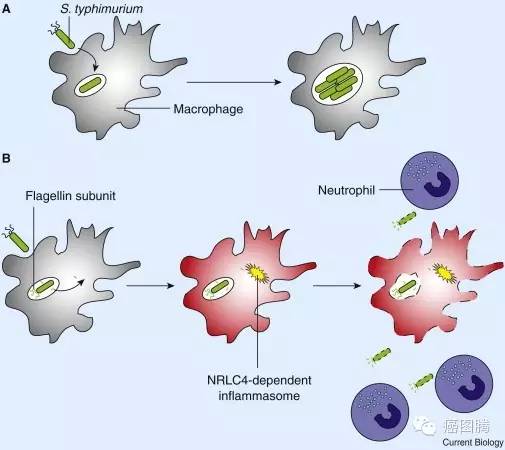
巨噬细胞通过自杀暴露隐层的入侵者
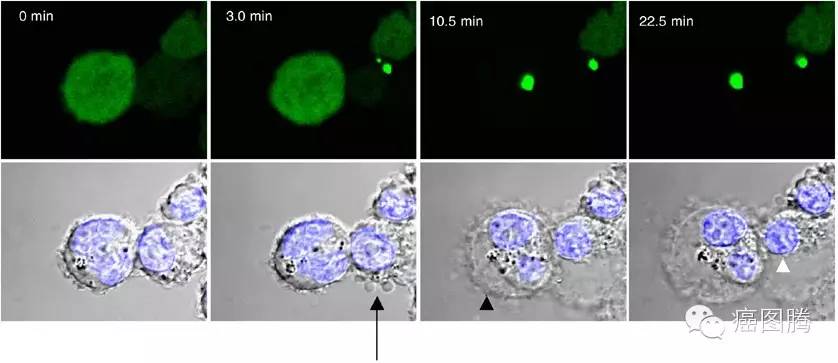
细胞胀亡(Oncosis)细胞肿胀,体积增大,胞浆空泡化,肿胀波及细胞核、内质网、线粒体等胞内结构,胞膜起泡,细胞膜完整性破坏。胀亡细胞周围有明显炎症反应。1910年, von Reckling-hausen在骨软化病中发现由于缺血而肿胀坏死的骨细胞,他把这种肿胀坏死叫做Oncosis。1995年Majno和Joris为与凋亡相区别,重新引入了Oncosis的概念,把具有明显肿胀特点的细胞死亡命名为Oncosis;
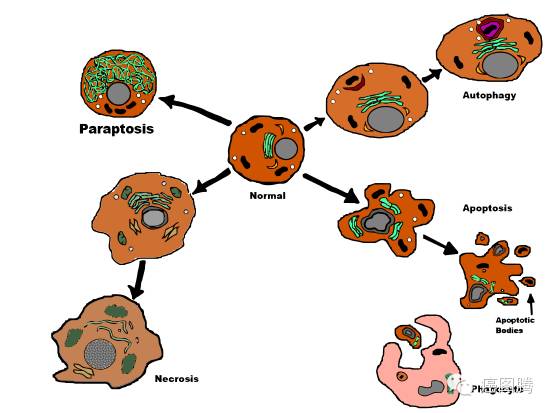
副凋亡(Paraptosis ):一种非凋亡性细胞程序死亡,细胞浆空泡化,线粒体和内质网肿胀,但没有核固缩现象。2000年Sperandio等在293T细胞系中超表达胰岛素样生长因子1受体(IGFIR)时发现一种与经典凋亡不同的死亡表型,并定义为Paraptosis 。
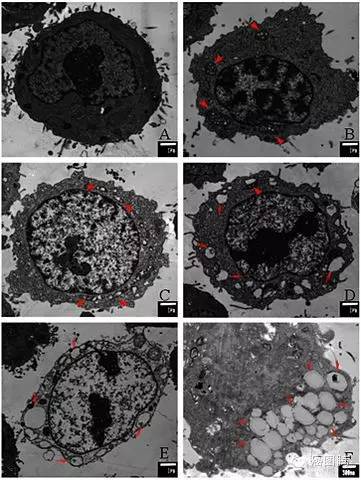
流产凋亡(aborted apoptosis:Necrosis-like programmed cell death):正常的程序性死亡启动后,半胱氨酸家族蛋白酶活化的路径被封堵,从而终止程序性死亡转向坏死,最后的细胞选择选择非胱解酶依赖凋亡路径终止生命;
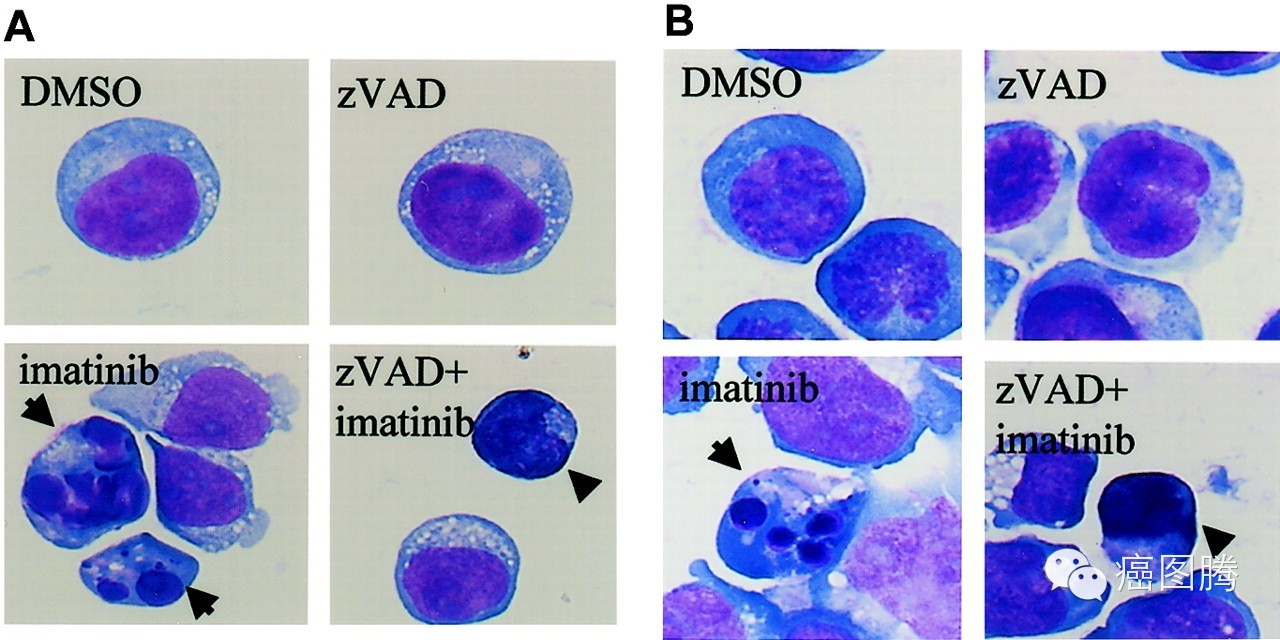
{nextpage}
衰老性细胞死亡
细胞在执行生命活动过程中,随着时间的推移,细胞增殖与分化能力和生理功能逐渐发生衰退。衰老死亡的细胞被机体的免疫系统清除,同时新生的细胞也不断从相应的组织器官生成,若衰老死亡的细胞不能被及时清除或被新生细胞替代会造成一些退行性疾病。
细胞僵尸(Senescense,"cell zombie"),生物学老化引起的现象,一般指体外倍增50次以后由于DNA双链受损、细胞中毒等引起细胞失去分裂能力;
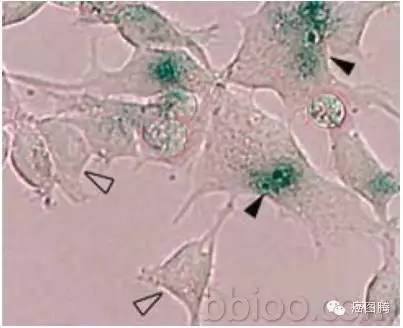
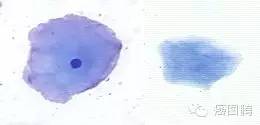
细胞角质化(Cornification)表皮细胞会依基底细胞→棘层细胞→颗粒层细胞→角质层细胞的顺序形态集资转变,并向表层逐渐移动,最后变成角质细胞。这种表皮细胞的分化过程叫做“角质化”;

normal
Cornification
沃勒变性(Wallerian degeneration)切断神经纤维后,在与神经细胞失去联系的一侧(末梢侧)神经纤维,在几天内所发生的变性。是英国生理学家沃勒(A.V.Waller 1816—1870)所研究的现象,但细胞侧的纤维部分则没有多大变化,称此为沃勒(变性)定律;
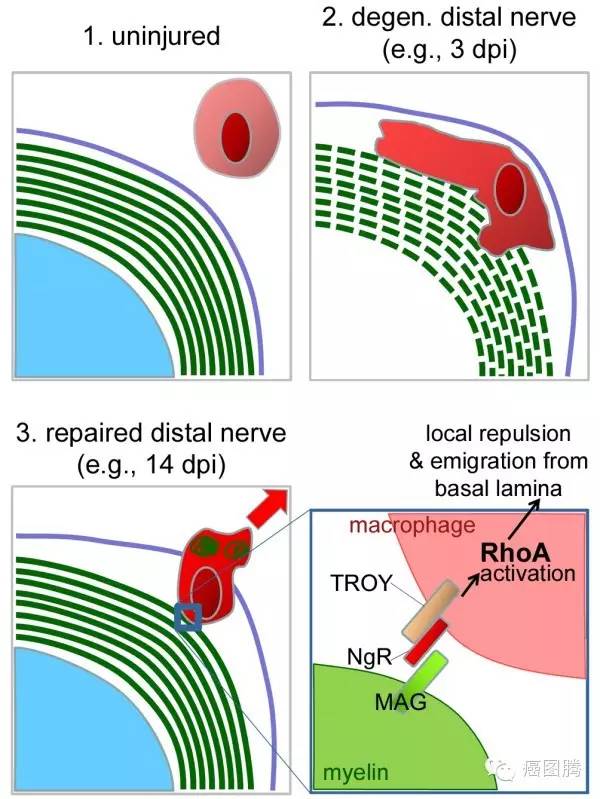
向死去的细胞致敬
多数情况下因为一些细胞死了我们才能更健康,而意外或衰老造成的细胞死亡会却影响机体功能正常运行,研究细胞坏死的信号、机理和调控以及它们对人体功能和疾病的影响,研究细胞坏死的方式有助于找到造成死亡的原因和解决办法。因此,我们要向为了机体全体细胞的利益而壮烈牺牲的细胞致敬!
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











死去活来!
199
当知识记不错,整理的真好
213
学习!
150
长知识了!
152
总结的真好!
70
总结的太好了
107
奋斗
56