一文读懂:肝纤维化的发生机制
2023-01-11 消化界 消化界 发表于上海
在我国肝纤维化和肝硬化的最常见病因为慢性病毒性肝炎特别是乙肝和丙肝,近年非酒精性脂肪性 肝病(NAFLD)和自身免疫性肝病引起的纤维化也逐渐增加。
概述
肝纤维化是多种病因导致的慢性肝脏疾病。其主要特征是肝脏内弥漫性的、过量的细胞外基质(特别是胶原)沉积。近期研究表明,如果能给予有效的病因治疗,或能直接抑制细胞外基质的合成和/或促进其降解,已经形成的肝纤维化甚至是可以逆转的,但是当病变继续进展产生肝硬化及肝细胞肝癌 (HCC)时,肝脏结构和功能会发生不可逆损害,威胁患者生命。
在我国肝纤维化和肝硬化的最常见病因为慢性病毒性肝炎特别是乙肝和丙肝,近年非酒精性脂肪性 肝病(NAFLD)和自身免疫性肝病引起的纤维化也逐渐增加。
肝纤维化的病因
1.感染性:慢性乙型肝炎、慢性丙型肝炎、慢性丁型肝炎和血吸虫病;
2.脂肪代谢性:非酒精性脂肪性肝炎;
3.化学毒物性:酒精性肝病、药物性肝损害和其它化学毒物所致的肝损害;
4.自身免疫性:自身免疫性肝炎;
5.胆汁淤积性:原发性胆汁性肝硬化(胆管炎)、原发性硬化性胆管炎、先天性胆道闭锁和进行性肝内胆汁淤积;
6.遗传代谢性:肝豆状核变性(WiIson病)、血色病和α-1抗胰蛋白酶缺乏症。

肝纤维化的临床表现
肝纤维化从严格意义上来说是无症状的,但是由于疾病的进展,导致肝脏进一步受损,患者出现如:疲乏无力、食欲减退、大便异常、肝区不适、睡眠障碍等一系列症状。若不及时进行有效的控制,肝纤维化可能进一步发展为肝硬化, 甚至肝硬化失代偿,出现:腹水、食管胃底静脉曲张等症状。肝纤维化的原因有多种,有时同一患者身上存在多种原因,伴有原发慢性肝病的其他临床特征。
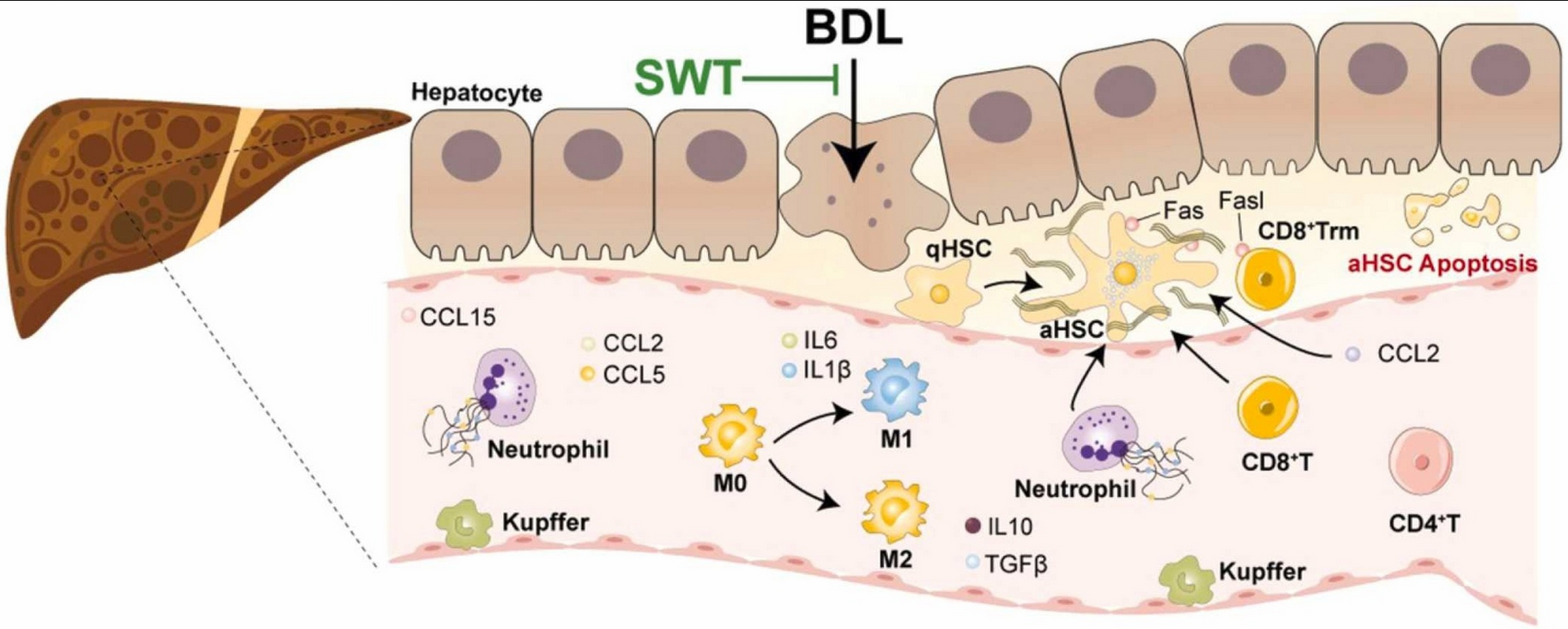
肝纤维化的机制
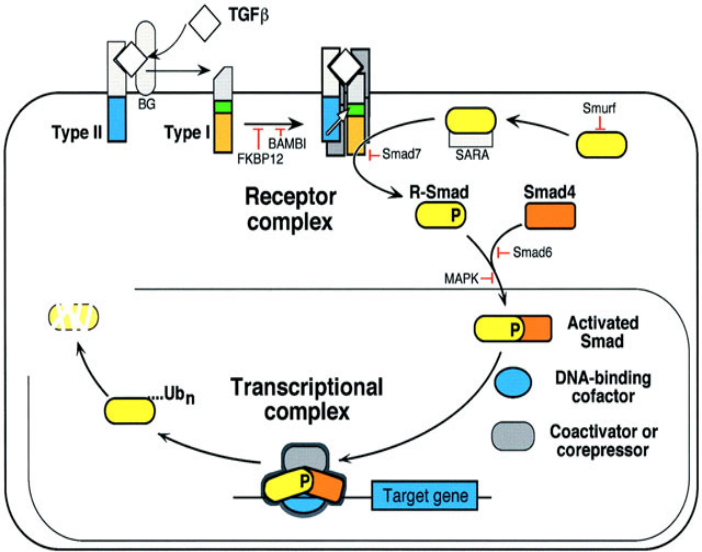
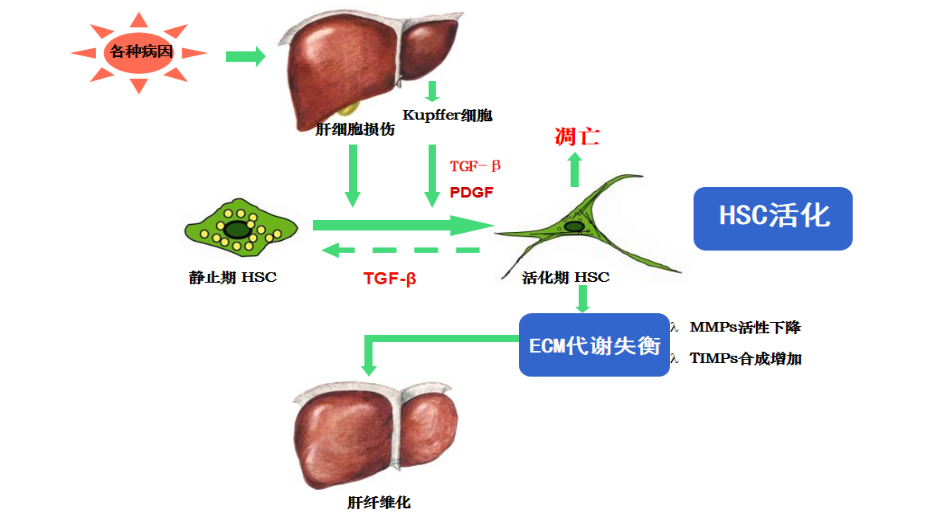
肝纤维化是肝脏在受到外界刺激后发生的自我修复和伤口 愈合,这是一个复杂的多细胞反应的结果。国内肝病多数是由于大量饮酒和慢性乙型、丙型病毒性肝炎感染引起的,但不管是何种病因,肝纤维化的形成过程非常相似,主要包括长期慢性实质损伤,持续激活炎症反应和氧化应激,细胞外基质大量沉积,纤维瘢痕形成等,共同破坏肝脏的正常结构和功能纤维化的发生始于效应细胞的激活。肝脏受到损伤后,肝内细胞的死亡以及免疫细胞的浸润引起炎症和纤维化信号的级联反应激活。细胞损伤会释放危险相关分子模式(damageassociated molecularpatterns,DAMPs),是一种细胞内异质分子,如游离 DNA、ATP、核因子(high mobility group protein B1,HMGB1),热休克蛋白等,或许还有病原体相关分子模式(pathogen-ssociated molecular patterns, PAMPS), 如 酒 精 ,革兰氏阴性菌脂多糖(LPS)等,这些相关模式刺激并激活一些炎症细胞如巨噬细胞、T 细胞、自然杀伤细胞(natural killer Tcell, NKT)、 库 普 弗 细 胞 等 , 分 泌 如 白 介 素 (interleukin,IL)-1β、-18、-13, 干 扰 素 γ, 肿 瘤 坏 死 因 子-α(tumornecrosis factor-α, TNF-α) 等 促 炎 因 子 和 CCL2(C-C motifchemokineligand 2)等趋化因子,进一步诱导淋巴细胞,单核细胞等在损伤处的募集和激活。
在炎症微环境下,肌成纤维细胞活化和增殖,并在趋化因子的作用下迁徙,肌成纤维细胞是产生细胞外基质(extracellular matrix,ECM)的主力来源。肌成纤维细胞的来源可根据病因的不同,大致分为4种,以静息期的肝星状细胞(hepatic stellate cells,HSC)激活分化为主,α-平滑肌肌动蛋白(actin alpha 2,α-SMA)和I型胶原的表达增加是活化的肝星状细胞(activated hepatic stellate cells,aHSCs)的特征标志;还有内源性门静脉成纤维细胞、骨髓来源细胞和肝实质细胞来源,可经过上皮间充质转换(epithelial-mesenchymaltransition,EMT)产生肌成纤维细胞,通过分泌细胞外基质蛋白等对肝纤维化进展产生重要作用。在进展性肝慢性损伤中,ECM的生成降解平衡状态被打破而大量沉积是肝纤维化的重要特征。活化的巨噬细胞、肝星状细胞,以及其他肌成纤维细胞可以释放肿瘤生长因子-β1(transforming growth factor beta 1,TGF-β1),TGF-β1 是诱导纤维胶原(主要是I型和III型)、α-SMA、层黏连蛋白和纤维连接蛋白产生的最有效的细胞因子,同时该因子也会促进肌成纤维细胞存活和增殖。肝星状细胞可以分泌基底膜蛋白酶、基质金 属 蛋 白 酶 (matrixmetalloproteinase, MMP) 包 括 MMP-2、MMP-3和MMP-9和间质胶原酶MMP-13,aHSCs可以分泌金属蛋白酶组织抑制剂(tissue inhibitor of metalloproteases,TIMP)1和2。MMPs是一种钙依赖性酶,能特异性降解胶原和非胶原性 ECM底物,而在肝损伤期间金属蛋白酶组织抑制剂的持续产生可以抑制基质金属蛋白酶的活性,使得金属蛋白酶对多余的纤维胶原去除效率降低,打破基质降解合成的平衡,从而促进细胞外基质的沉积。在肝纤维化的典型特征中,除了ECM的大量沉积,还会发 生窦道毛细血管化,这主要是由于HSC激活后,合成和释放血管生成介质,如 VEGFA(vascular endothelialgrowth factor A),PDGF(platelet derived growth factor)等,同时分泌纤维胶原I和III在剥离间隙中取代IV型胶原引起的;胆管反应,在慢性肝损伤的情况下,持续的炎症和氧化应激使得肝细胞增殖和肝干细胞分化被抑制,短暂扩增的肝祖细胞被迫主要分化为激活和应激抵抗的胆管样细胞或反应性胆管细胞。

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言