CAR-T之父最新Nature论文!无需放化疗,新型T细胞疗法成功治愈超半数难治型实体瘤小鼠
2022-08-18 上海细胞治疗工程技术研究中心 金瑞斯生物
研究人员在两种难治型癌症模型(胰腺癌和黑色素瘤)中测试了一种新型的 T 细胞疗法。
当前,肿瘤的基因与细胞治疗已成为国内外研究的热点问题。近几年,尤其是在 T 细胞免疫治疗研究方面,已经取得了很大成效,有多款 T 细胞治疗产品获批上市。这些产品大多利用基因编辑和细胞培养等技术强化 T 细胞的治疗能力,从而达到攻克癌症的目的。
然而,在病人接受针对癌症肿瘤的 T 细胞治疗之前,必须先用化疗或放疗来摧毁病人的免疫系统,否则输入病人体内的 T 细胞会受到原先的免疫系统影响而无法正常发挥治疗作用 [1]。众所周知,接受化疗或放疗的患者往往会经受很多副作用的摧残,包括恶心、脱发和极度疲劳等等。
近日,CAR-T 之父 Carl June 和来自斯坦福的 Kenan Garcia、来自加州大学洛杉矶分校(UCLA)的 Antoni Ribas 等团队合作,共同在 Nature 上发文,证明了使用一种人工合成的白细胞介素 IL-9 受体即可让抗癌 T 细胞(CAR-T 和 TCR-T)在不需要化疗或放疗的情况下正常工作[2]。当 T 细胞通过合成的 IL-9 受体发出信号时,它们获得了新的功能,这不仅能让它们战胜现有的免疫系统,还能更有效地杀死癌细胞。这一研究成果有望使得 T 细胞输送变得像普通输血那样容易 [3]。

本研究中所使用的 cDNA 由金斯瑞助力合成
细胞因子 IL-9
常见的 γ 链细胞因子家族( IL-2,IL-4,IL-7,IL-9,IL-15 和 IL-21)在 T 细胞分化、增殖和体内平衡等方面起到了关键作用。早在 2018 年,Antoni Ribas 等人就已报道,一种关键的 T 细胞生长细胞因子白细胞介素 - 2(IL-2)可以用来刺激携带有相应合成受体的 T 细胞。通过这种方式,即使 T 细胞已经被注射到病人体内,也可以利用人工合成的细胞因子来操纵 T 细胞,而且这些细胞因子不会影响体内其他细胞。在这项工作的启发下,研究人员开始对细胞因子的合成受体进行改良,这些改良的受体也可以传递来自 γ 链家族的其他细胞因子信号:IL-4、IL-7、IL-9 和 IL-21。其中,IL-9 十分具有研究价值。
IL-9 最初被描述为参与辅助型 T 细胞应答的 T 细胞生长因子。但是最近的研究表明,产生 IL-9 的 T 细胞(Th9 / Tc9)可引起组织炎症,通过激活肥大细胞(Mast Cell)或间接吸引非成熟的树突细胞和 CD8 T 细胞来抑制肿瘤生长。与其他常见的 γ 链细胞因子不同,由于 IL-9 受体(IL-9R)表达的缺失,IL-9 信号传导在天然存在的 T 细胞中并不活跃。合成的 IL-9R 信号可以使 T 细胞呈现出一种独特的类似干细胞和杀伤细胞的混合特性,这让它们在对抗肿瘤时会变得更加强大。
信号模拟实验:锁定 o9R
研究人员首先对各种野生型 IL 受体信号进行了模拟,模拟信号被称为 o2R、o4R、o7R、o9R 和 o21R。他们观察到,通过 o9R 或 o21R 信号传递,T 细胞表面标志物 CD62L、CD95 和 Sca-1 的表达量均会升高。这与干细胞记忆 T 细胞(TSCM)表型相一致,这一类 T 细胞以其在过继细胞治疗中优越的抗肿瘤活性而闻名。
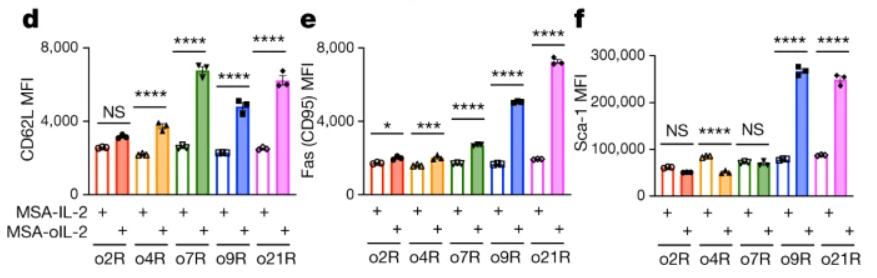
嵌合受体 T 细胞表面标志物的表达水平
结合各种 IL 受体信号的研究史和其他特性,研究人员最终决定对 IL-9R 的模拟信号 o9R 进行深入研究。他们选择使用以细胞疗法治疗实体肿瘤的小鼠模型在体内研究 o9R 信号传导的影响。
体内实验:疗效显著
研究人员首先对 pmel 小鼠 T 细胞进行改造,使其得以表达对 gp100 具有特异性的 T 细胞受体(TCR)。这是一种在 B16 黑色素瘤中过度表达的黑色素细胞抗原。然后用 o2R 或 o9R 转导 T 细胞,再将其输入 B16 黑色素瘤小鼠体内。实验结果表明,T 细胞过继 7 天后,o9R pmel T 细胞在不经过放化疗(未清除淋巴细胞)的情况下,也能实现大量扩增,而且其抗肿瘤作用和存活期都要优于 o2R 转导的 T 细胞。

实验流程 (a) 及过继 7 天后 T 细胞数量比较 (b)
为了探索 o9R 信号在 CAR-T 疗法中的作用,研究人员使用了表达间皮素的胰腺癌免疫治疗耐药模型。他们利用含有 IL 受体模拟信号的 CAR 来转导小鼠原代 T 细胞,从而得到了 CAR-o2R 和 CAR-o9R T 细胞。结果显示 CAR-o9R T 细胞在体外对间皮素阳性的胰腺导管腺癌 (PDA) 细胞系(PDA7940b)显示了优越的抗肿瘤疗效。
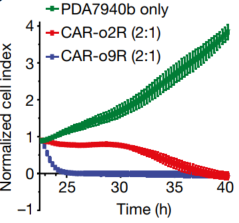
体外 CAR-o9R T 细胞杀灭间皮素阳性胰腺导管腺癌细胞系 PDA7940b
走向临床应用
为了探索 o9R 信号的应用潜能,研究人员首先利用编码人类 o2R(ho2R)或人类 o9R(ho9R)的逆转录病毒和编码 TCR(靶向癌症抗原 NY-ESO-1)的载体来转导人类 T 细胞。NY-ESO-1 在滑膜肉瘤、黏液性脂肪肉瘤、黑色素瘤等肿瘤中都会过表达。结果表明,ho9R 信号使得 TSCM 细胞和中央记忆性 T 细胞(TCM)大量扩增富集。
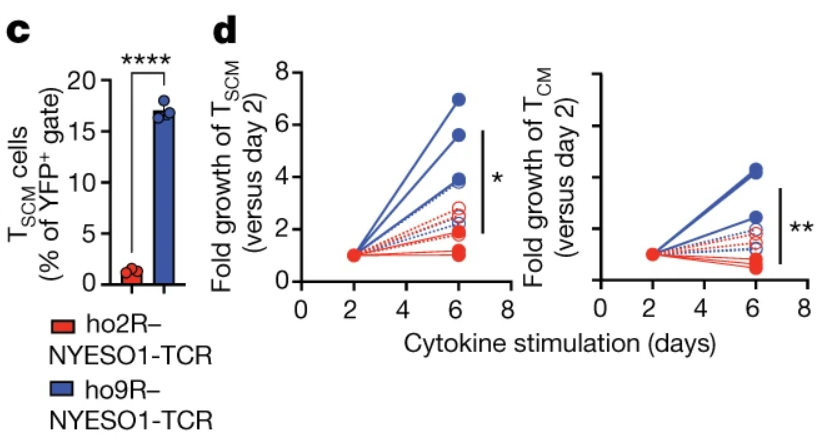
ho2R 和 ho9R 对 TSCM 和 TCM 的影响
随后,他们改用编码 ho2R/ho9R 和 CAR 的载体来转导人类 T 细胞,以期治疗小鼠胰腺癌,并获得了与 TCR 实验中类似的结论:即 ho9R 信号能够使得 T 细胞获得更优越的肿瘤细胞杀伤能力。
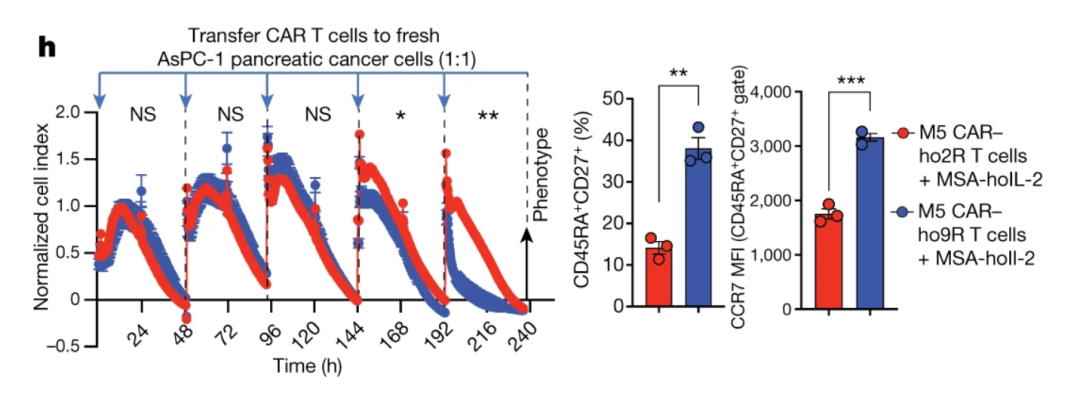
CAR-T 细胞输入后小鼠肿瘤活力及 T 细胞表面标志物表征
值得一提的是,本文的第一作者 Anusha Kalbasi 在接受采访时说到,他们利用合成 IL-9 受体 T 细胞,已经成功在一个肿瘤实验中治愈了超过半数的患病小鼠 [3]。
总而言之,研究人员在两种难治型癌症模型(胰腺癌和黑色素瘤)中测试了一种新型的 T 细胞疗法。他们通过靶向天然的 T 细胞受体(TCR)或嵌合抗原受体(CAR)的 T 细胞来攻击小鼠癌细胞,并利用合成的细胞因子信号来强化 T 细胞。
无论研究人员将细胞因子注入整只小鼠还是直接注入小鼠肿瘤中,这种疗法都被证明具有显著疗效。在所有的实验中,用合成 IL-9 受体信号传导设计的 T 细胞都具有更好的肿瘤杀伤能力,治愈了很多原本无法治愈的肿瘤小鼠。
参考资料:
[1] Dudley, Mark E., et al. "Adoptive cell therapy for patients with metastatic melanoma: evaluation of intensive myeloablative chemoradiation preparative regimens." Journal of Clinical Oncology 26.32 (2008): 5233.
[2] Kalbasi, A., Siurala, M., Su, L.L. et al. Potentiating adoptive cell therapy using synthetic IL-9 receptors. Nature (2022). https://doi.org/10.1038/s41586-022-04801-2
[3] News Medical Life Sciences. “Synthetic IL-9 receptor allows T cells to fight cancer without the need for chemo or radiation”. Retrieved Jun 10, 2022 from https://www.news-medical.net/new
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#CAR-#
100
#Nat#
84
#最新#
65
#放化疗#
104
#T细胞疗法#
95