【肝霖特写】丁肝当前最佳疗法:基于干扰素α治疗!
2024-03-11 雨露肝霖 雨露肝霖 发表于上海
现有证据表明,基于干扰素α治疗仍是丁肝最佳疗法。肝霖君整理了丁肝治疗的相关证据。
编者按
目前,美国食品药品监督管理局(FDA)尚未批准任何丁型肝炎治疗药物。在过去的几十年里,聚乙二醇干扰素α被广泛用作丁肝治疗的标准疗法。备受瞩目的Bulevirtide于2020年获得了欧盟(EU)的有条件上市许可。现有证据表明,基于干扰素α治疗仍是丁肝最佳疗法。肝霖君整理了丁肝治疗的相关证据。
丁型肝炎病毒 (HDV) 感染与乙型肝炎病毒 (HBV) 感染相关,在普通人群中丁型肝炎总体患病率为0.16% - 0.98%,在HBsAg携带者中为4.5% - 14.57%,影响全球约 1200 万至 7200 万人[1-3]。慢性丁型肝炎(CHD)是最严重的慢性病毒性肝炎,与单纯的乙型肝炎病毒相比,丁型肝炎病毒导致更快的肝脏疾病进展,发生肝硬化、失代偿性肝病和肝细胞癌 (HCC)的风险更高。
01 丁肝治疗指征及治疗终点
所有慢性丁型肝炎患者(HDV-RNA阳性且伴有丙氨酸转氨酶水平升高或肝纤维化)在有安全有效的治疗方法时均应考虑进行抗病毒治疗。丁肝治疗的目标是通过预防疾病进展(尤其是肝硬化、失代偿性肝病、肝癌和肝脏相关死亡)提高患者生存率。丁肝治疗的理想终点是乙型肝炎表面抗原 (HBsAg)血清学转换,这与改善临床结局相关且HBsAg是丁型肝炎病毒生命周期所必需的。2022年AASLD-EASL关于HBV-HDV治疗终点会议[4]提出在评估治疗持续时间有限研究(II/III期)时HBsAg清除是慢性丁型肝炎的首选终点,停药24周后HDV RNA <LLOQ是适宜的替代终点。评估持续治疗研究时主要终点为治疗第48周HDV RNA <LLOQ,替代终点是HDV RNA降低≥2 log10 IU/mL,同时丙氨酸转氨酶水平恢复正常。
慢性丁型肝炎治疗性研究的主要和次要终点
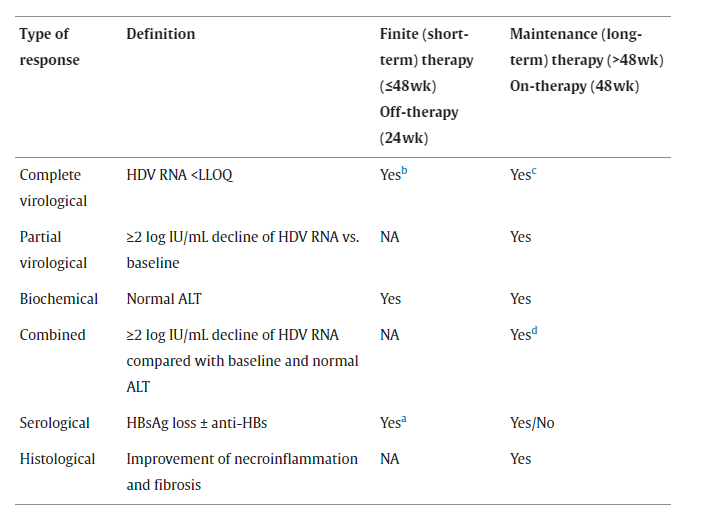
a治疗持续时间有限研究的主要终点;b治疗持续时间有限研究的次要终点;c持续治疗研究的主要终点;d持续治疗研究的次要终点
02 聚乙二醇干扰素α是大多数国家目前唯一认可的丁肝治疗策略
目前,聚乙二醇干扰素α是大多数国家唯一认可超说明书使用的丁肝治疗药物。有丁肝病毒血症伴有肝纤维化且无失代偿和禁忌证的患者应使用聚乙二醇干扰素α治疗。在一些欧洲国家可选择Bulevirtide,但其最佳剂量和持续时间仍不明确[5]。
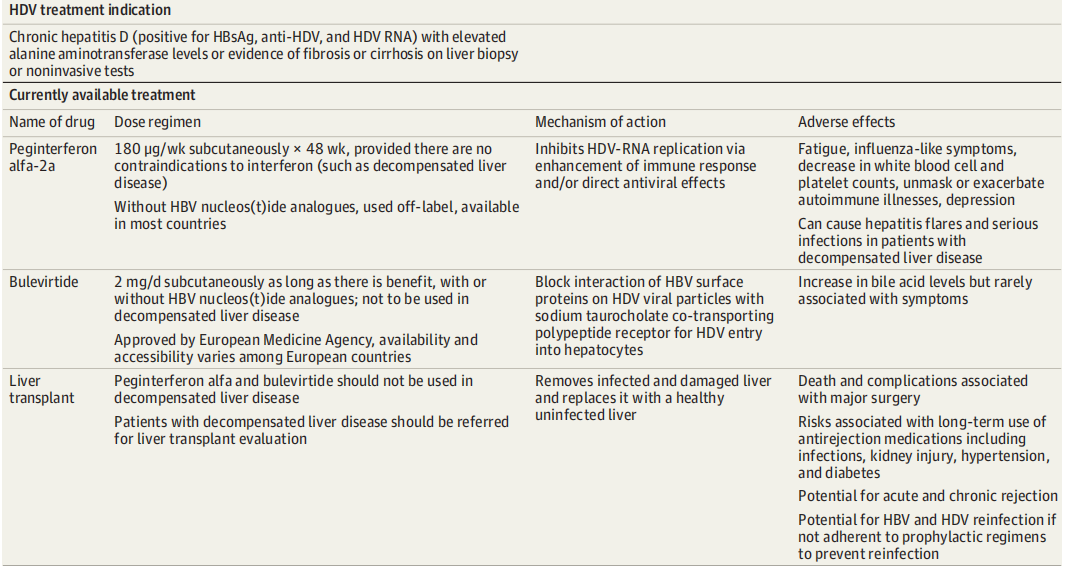
一项随机对照试验的系统综述和网状荟萃分析[6]通过比较七种干预措施对慢性丁型肝炎的疗效发现:干扰素α、聚乙二醇干扰素α联合Bulevirtide 和干扰素α联合核苷(酸)类似物可有效清除 HDV RNA 和使丙氨酸转氨酶水平正常化;在慢性丁型肝炎的干扰素α治疗中加入核苷(酸)类似物没有额外的获益;然而,聚乙二醇干扰素α联合Bulevirtide显著提高了短期HDV RNA清除率,显示出较强的协同作用。因此,聚乙二醇干扰素α联合Bulevirtide最有可能作为改善长期预后甚至治愈慢性丁型肝炎的疗法。
03 其他正在开发的治疗方案
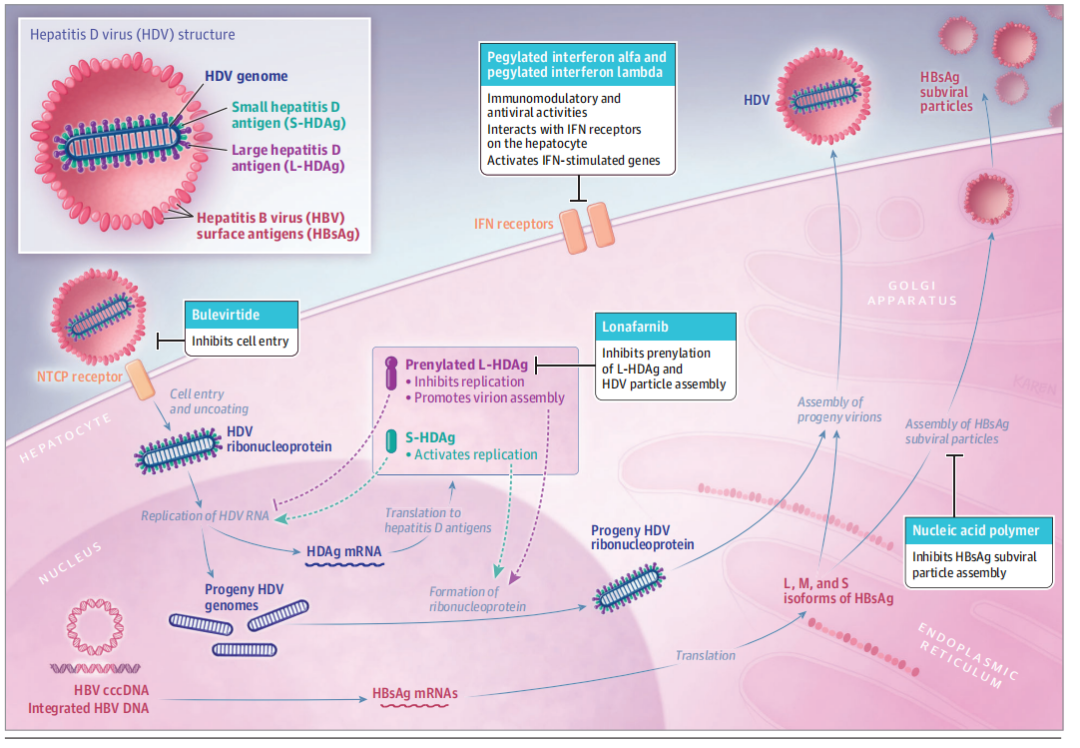
目前,聚乙二醇干扰素λ、Lonafarnib、REP-2139(核酸聚合物)作为治疗丁肝的新型药物已进入临床试验阶段。在Lonafarnib的 3 期随机对照研究中,Lonafarnib、聚乙二醇干扰素α与tonavir的三联组合的第48周复合应答率(HDV RNA下降≥2 log10 IU/mL和丙氨酸转氨酶正常化)为19.2%高于Lonafarnib与tonavir联合组合的10.1%[7]。REP 2139-Ca联合PEG IFNα治疗HBV/HDV共感染患者实现了高 HDV RNA和乙型肝炎表面抗原清除/血清学转换率,且在随访3.5年期间持久性良好[8]。
肝霖君有话说
慢性丁型肝炎是最严重的慢性病毒性肝炎。与单纯乙肝病毒感染相比可导致更快的肝脏疾病进展,因此应积极开展抗病毒治疗。基于丁肝病毒依赖于乙肝病毒的特征,建议丁肝治疗药物可与聚乙二醇干扰素α联合使用以达到HBsAg清除的理想终点。
参考文献:
[1] Chen HY, Shen DT, Ji DZ, et al. Prevalence and burden of hepatitis D virus infection in the global population: a systematic review and meta-analysis[J]. Gut, 2019, 68(3): 512-521.
[2] Miao Z, Zhang S, Ou X, et al. Estimating the Global Prevalence, Disease Progression, and Clinical Outcome of Hepatitis Delta Virus Infection[J]. J Infect Dis, 2020, 221(10): 1677-1687.
[3] Stockdale AJ, Kreuels B, Henrion MYR, et al. The global prevalence of hepatitis D virus infection: Systematic review and meta-analysis[J]. J Hepatol, 2020, 73(3): 523-532.
[4] Ghany MG, Buti M, Lampertico P, et al. Guidance on treatment endpoints and study design for clinical trials aiming to achieve cure in chronic hepatitis B and D: Report from the 2022 AASLD-EASL HBV-HDV Treatment Endpoints Conference[J]. J Hepatol, 2023, 79(5): 1254-1269.
[5] Negro F, Lok AS. Hepatitis D: A Review[J]. Jama, 2023, 330(24): 2376-2387.
[6] Rong Y, Ju X, Sun P, Wang Y, et al. Comparative effectiveness of seven interventions for chronic hepatitis D: a systematic review and network meta-analysis of randomized controlled trials[J]. BMC Infect Dis, 2023, 23(1): 726.
[7] Etzion O, Hamid SS, Asselah T, et al. Week 48 results of the phase 3 D-LIVR study, a randomized double-blind, placebo-controlled trial evaluating the safety and efficacy of Lonafarnib-boosted with Ritonavir with or without Peginterferon Alfa in patients with chronic hepatitis delta[J]. Journal of Hepatology, 2023, 78: S10-S10.
[8] Bazinet M, Pântea V, Cebotarescu V, et al. Persistent Control of Hepatitis B Virus and Hepatitis Delta Virus Infection Following REP 2139-Ca and Pegylated Interferon Therapy in Chronic Hepatitis B Virus/Hepatitis Delta Virus Coinfection[J]. Hepatol Commun, 2021, 5(2): 189-202.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#干扰素α# #丁肝#
113