JCO:多基因风险评分帮助预测儿童肿瘤幸存者继发癌症风险
2023-09-28 儿童肿瘤前沿 儿童肿瘤前沿 发表于上海
研究评估了一个在成人肿瘤幸存者患者中验证过的PRS评分系统,对于儿科肿瘤幸存者(确诊后存活超5年者)的继发恶性肿瘤风险的预测价值。
儿童肿瘤幸存者罹患继发恶性肿瘤(Subsequent malignant neoplasm,SMN)的风险较高,其肿瘤发病率是一般人群的5倍。既往研究已经表明,接受放疗是继发恶性肿瘤明确的风险因素,并且呈现剂量相关性;因此,在现代的儿童肿瘤治疗方案中,已经尽量减少放疗的使用。化疗药物的应用也与特定的继发恶性肿瘤有关,如继发白血病与烷化剂、鬼臼毒素暴露有关;继发肉瘤与蒽环类药物、烷化剂暴露有关,等等。
遗传易感性是另一个重要因素。对于少数患者,罕见的高致病性种系突变引起家族癌症综合征,增加继发肿瘤风险。对于一些较常见的突变/基因多样性,采用多基因风险评分(Polygenic Risk Score,PRS)这种方法学可以更好地评价多个微小效应突变的总和效应,因此对于预后分层上更有价值。既往研究已经揭示了PRS在成人肿瘤患者的继发肿瘤风险评估中的价值,但在儿童肿瘤患者队列中尚未明晰。
近日,来自圣裘德儿童医院的 Cindy Im 等人在 Journal of Clinical Oncology 发表题为 Polygenic Risk and Chemotherapy-Related Subsequent Malignancies in Childhood Cancer Survivors: A Childhood Cancer Survivor Study and St Jude Lifetime Cohort Study Report 的文章,评估了一个在成人肿瘤幸存者患者中验证过的PRS评分系统,对于儿科肿瘤幸存者(确诊后存活超5年者)的继发恶性肿瘤风险的预测价值。

本研究应用的PRS评分系统基于179个基因位点,这些基因位点在样本量超过40万人的UK biobank成人肿瘤GWAS研究中被验证。儿科肿瘤幸存者的基线、治疗、基因和预后信息来自于两个北美儿科肿瘤队列:儿科肿瘤幸存者研究(Childhood Cancer Survivor Study,CCSS)和圣裘德终身队列(St Jude Lifetime Cohort,SJLIFE)。
共有 10,613 名儿童期肿瘤幸存者被纳入分析,随访时间达 244,633 人年。其中,9895 名幸存者具有欧洲(EUR)遗传血统,718 名幸存者具有非洲(AFR)遗传血统。与非洲裔幸存者相比,欧洲裔幸存者有更高几率罹患 SMN(15.2%),尤其是继发性基底细胞癌(7.9%);非洲裔幸存者罹患SMN的比例是3.9%,罹患基底细胞癌的比例仅有 0.1%。最常见的原发性癌症诊断为白血病、中枢神经系统肿瘤和霍奇金淋巴瘤。欧洲裔幸存者首次罹患继发恶性肿瘤的中位年龄为36岁(IQR,30-43岁),而非裔幸存者为31岁(IQR,24-42岁)。放疗暴露方面,52.6%的欧洲裔幸存者和44.1%的非洲裔幸存者曾暴露于放疗,在完整病例分析中,共有4322名欧洲裔幸存者(259例SMN)和414名非洲裔幸存者(9例SMN)未接受放射治疗。
首先,放疗使用和SMN发生有关;而对于未接受放疗者,PRS评分最高级Q5与增加的SMN风险有关(HR of Q5, 2.06; P < .001)。未接受放疗者多接受了各种化疗,关于各种化疗药物/PRS与继发肿瘤风险的关联,研究表明,在未接受放疗的欧洲裔癌症幸存者中,如果按照PRS风险分层,将基因决定的癌症风险分为五个等级,则风险等级最高者相比于风险等级最低者,在接受烷化剂(HR of Q5, 2.46 [95% CI, 1.41 to 4.30]; P < .01),蒽环类(HR of Q5, 2.86 [95% CI, 1.60 to 5.09]; P < .001),依托泊苷(HR of Q5, 12.20 [95% CI, 2.94 to 50.68]; P < .001)和铂类(HR of Q5, 8.58 [95% CI, 1.89 to 38.98]; P < .01)治疗后,发生SMN的风险升高。(图1)
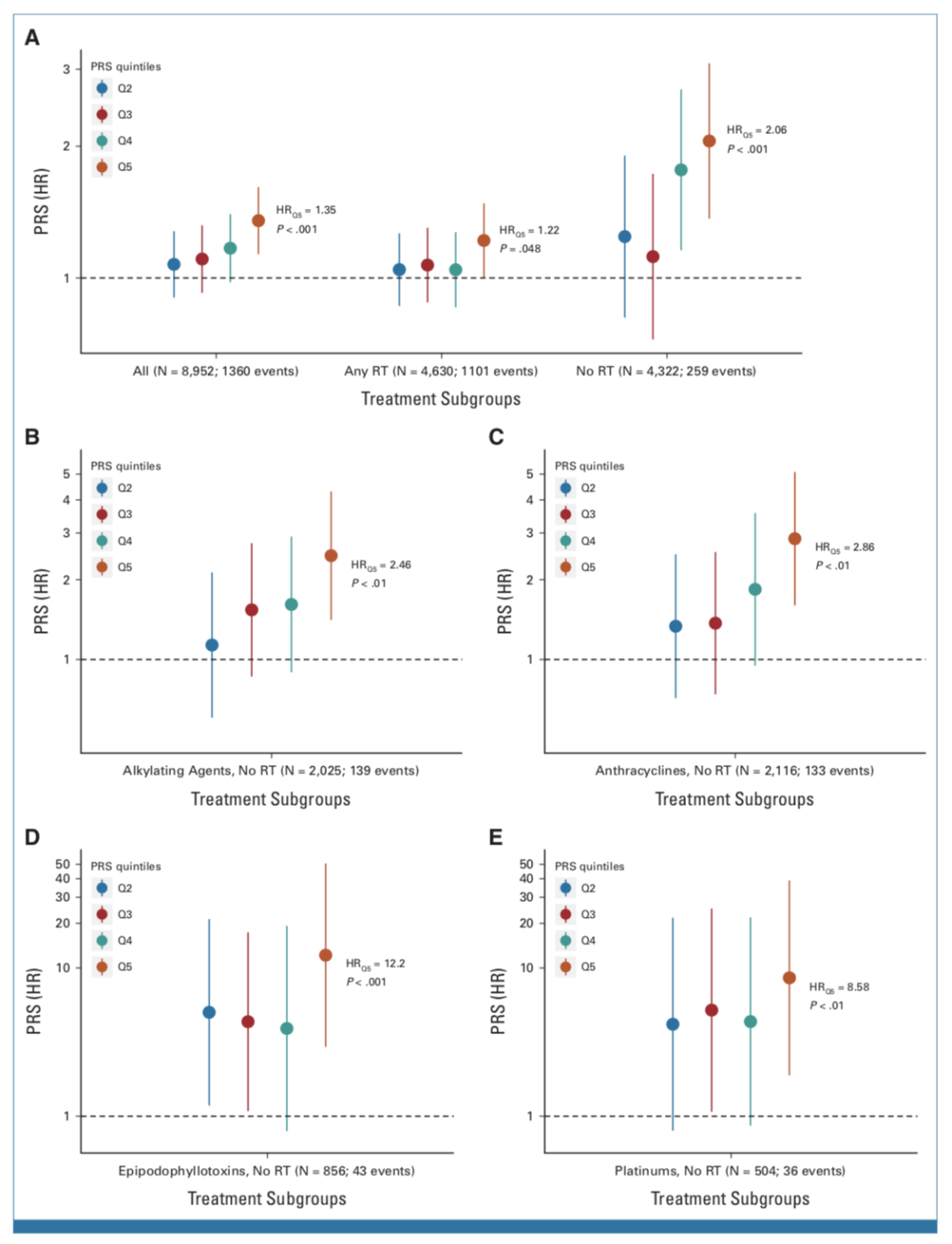
图1 PRS和SMN风险的关联,按照是否接受过放疗,以及具体化疗药物种类分组
生存分析来看,对于仅接受放疗,或者其他种类化疗的患儿,PRS最低风险和PRS最高风险者发生SMN的累积发病曲线没有统计学显著差异。但是对于烷化剂、蒽环类、依托泊苷和铂类化疗药物,PRS Q1和PRS Q5的幸存者,其生存曲线呈现统计学显著的差异。(图2)
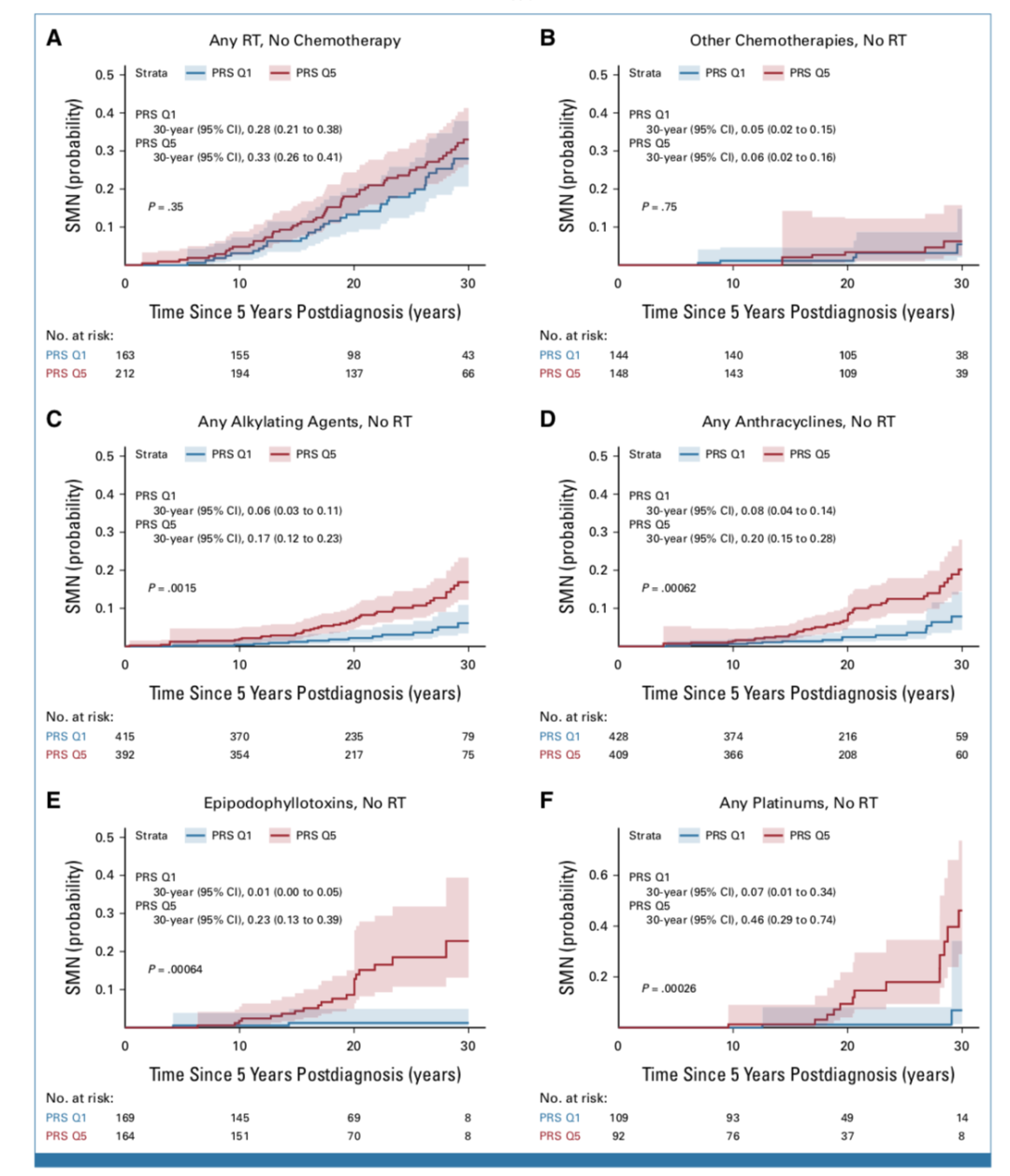
图2 SMN发生率的生存分析,PRS最高风险 v PRS最低风险,按照放化疗暴露情况分组
常见的继发癌症类型包括乳癌、甲状腺癌和其他实体瘤,占59%-73%,而非黑色素瘤的上皮细胞癌是仅接受了放疗的幸存者中最常见的肿瘤类型,占76%。(图3)
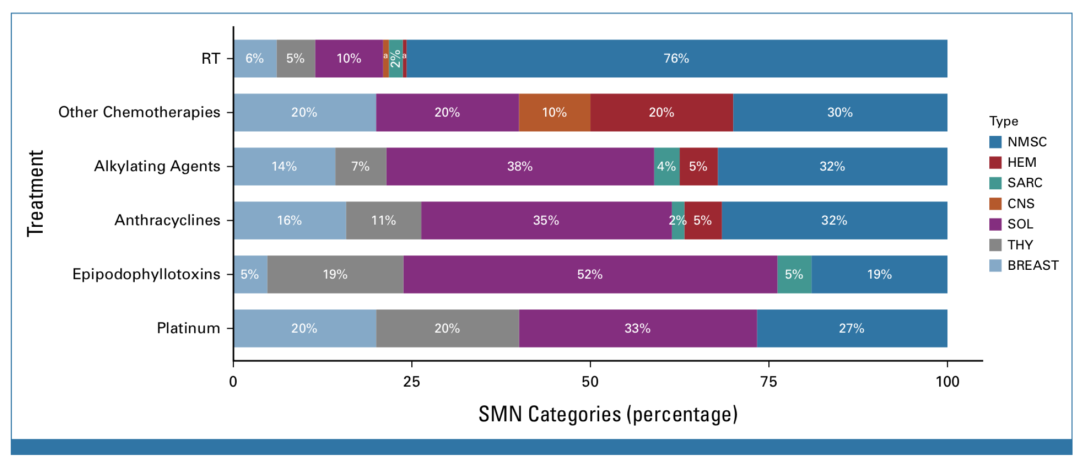
图3 SMN中各肿瘤诊断占的比例,按照放化疗暴露分组
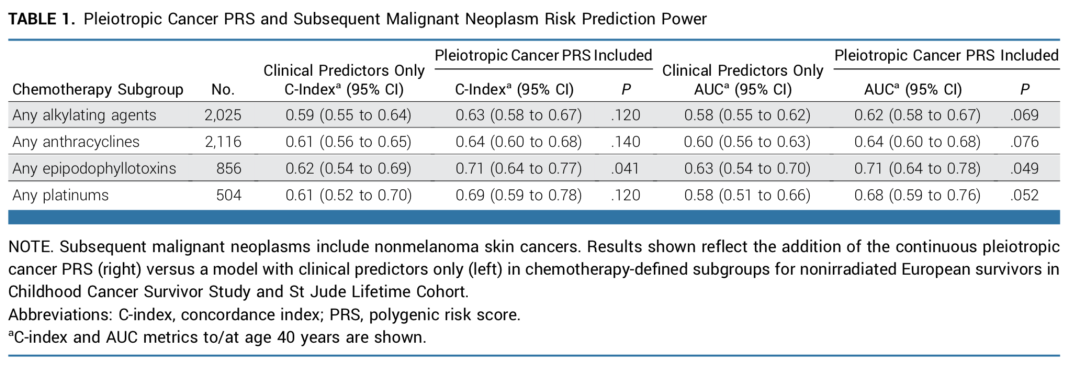
作者探讨了PRS评分对于继发肿瘤的预测效能。相比于传统的临床风险模型,加入PRS评分后,模型预测效能大大提高。(表1)
表1 在模型中加入PRS评分将提高对模型SMN发生的预测效能
本文的研究表明,尽管放疗在儿童肿瘤治疗的使用不断减少,但与普通人群相比,仅接受化疗的儿童肿瘤幸存者患 SMN 的风险仍几乎增加了三倍。利用来自 10,613 名儿童肿瘤长期幸存者的表型和基因型数据,发现利用经外部验证的成人肿瘤患者中验证过的多基因评分PRS对肿瘤患儿进行风险分层 ,如果原发性癌症接受特定化疗类药物治疗,PRS 最高风险组患儿后续患 SMN 的风险显著增高。在临床模型中纳入PRS评分,可以提高模型对于未来SMN发生的预测效能。该研究的结果提示我们,在对儿童肿瘤幸存者SMN风险的管理中,除了临床的暴露因素以外,先天性因素如基于基因多态性的PRS评分也应该被纳入考虑,或可更好地识别未来有较高SMN风险的患儿,从而改善随访的临床路径,改善患儿预后。
DOI: 10.1200/JCO.23.00428
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言