Hemasphere:Polatuzumab治疗复发/难治DLBCL的真实世界报道
2022-11-20 聊聊血液 聊聊血液
复发/难治性 (R/R) 弥漫性大 B 细胞淋巴瘤 (DLBCL) 的二线及以上治疗尚无明确的标准治疗,尤其是对于不适合移植的患者。
Polatuzumab
复发/难治性 (R/R) 弥漫性大 B 细胞淋巴瘤 (DLBCL) 的二线及以上治疗尚无明确的标准治疗,尤其是对于不适合移植的患者。最近在欧美获批的治疗药物包括polatuzumab vedotin 联合苯达莫司汀和利妥昔单抗 (PolaBR)、抗 CD19 单抗tafasitamab 联合来那度胺、CD19 CAR T 细胞治疗药物axicabtagene ciloleucel、tislecagenleucel,以及塞利尼索和loncastuximab tesirine,它们均具有特殊的缓解率和毒性特征。
Pola 是一种抗 CD79b 抗体-药物偶联物,其单药治疗和联合利妥昔单抗治疗 R/R DLBCL疗效均佳,且联合 BR 的完全缓解 (CR) 率为40.0%,中位无进展生存期 (PFS) 为9.5个月。FDA已批准 PolaBR 用于既往≥2线治疗的 DLBCL 患者。
关于 PolaBR 使用的真实世界报道仍然很少,尤其是关于该药物的潜在额外用途(例如桥接 CAR-T 或 CAR-T 后的挽救治疗),而对照临床试验之外接受 PolaBR 治疗的患者的数据可以提供关于该方案在 R/R DLBCL 患者中的临床使用、治疗持续时间、有效性和毒性的额外信息。
意大利Pier Luigi Zinzani教授牵头进行了一项观察性、回顾性、多中心意大利研究,重点关注PolaR(±B)在R/R DLBCL成人患者中的有效性和安全性(是否添加苯达莫司汀由医生自行决定)。研究结果近日发表于EHA官方期刊《Hemasphere》。

研究方法
本研究分析了在2019年6月至2020年2月期间,在指定患者项目(Named Patient Program ,NPP)中接受至少一剂PolaR(±B)的R/R DLBCL成人患者中的有效性和安全性。
研究的主要终点是总缓解率 (ORR),次要研究终点为最佳ORR、总生存期 (OS)、无病生存期 (DFS) 和PFS,以及从治疗开始至末次输注后30天发生的任何不良事件 (AE) 的类型、发生率、严重程度及其与研究药物的可能关系。探索性终点是两组治疗(即 PolaR 和PolaBR)之间的结局和安全性差异。
研究结果
患者特征
共入组55例患者,其中女性26例 (47.3%),男性29例,所有患者均接受R-CHOP或 CHOP 样方案作为一线治疗。32例患者为原发性难治,45例 (81.8%) 为末次治疗难治。Pola 前接受的中位治疗次数为3次。基线时(即 Pola 治疗前)大多数患者为 III/IV 期 (80.0%),大多数(78.2%)的ECOG PS 评分为0-1。Pola治疗方面,36例患者接受PolaBR,19例患者接受PolaR。除骨髓受累外,两组的基线特征无差异(表1)。

疗效和结局
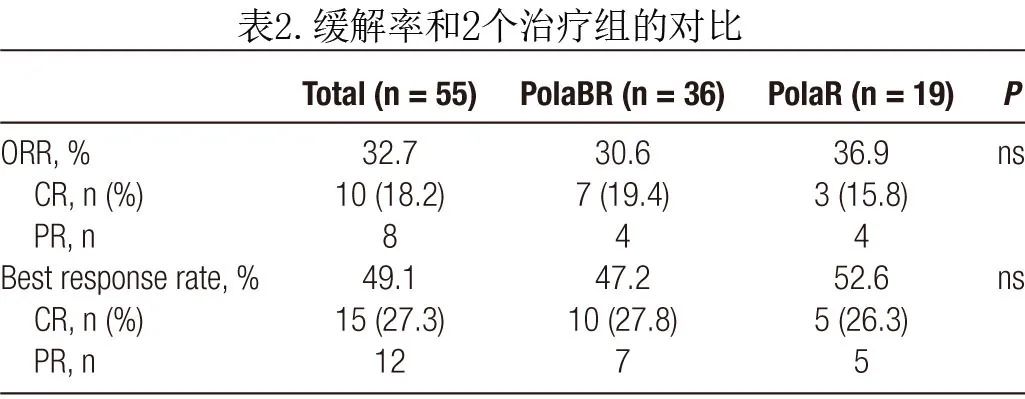
中位治疗4个周期后,最终 ORR 为32.7%(18.2% CR),最佳缓解率为49.1%(表2)。PolaBR 和 PolaR 的最佳 CR 率分别为27.8%(中位4个周期后达到)和26.3%(中位6个周期后达到)。PolaBR 组21例患者提前中止治疗:主因PD (N= 18) ,此外2例患者接受移植,1例患者因药物耐受性差而拒绝继续治疗;PolaR 组9例提前停药:7例因PD,2例因AE(肺炎和药物相关中毒性皮病)。
中位 DFS 为12.0个月,中位 PFS 为4.9个月(1年时为26.4%),中位 OS 为9.0个月(1年时为48.7%)(图1)。

33例患者在 Pola 后接受进一步治疗,特别是其中4例使用 Pola 作为干细胞输注(2例行自体和1例异基因移植)或 CAR-T 治疗(1例)的桥接治疗,分析时4例患者持续缓解,其中2例在 Pola 结束后19.5个月和16.2个月持续CR而无任何实变。
中位随访11个月后发生35例死亡,除5例死亡外均是由淋巴瘤引起(1例由胃肠出血、2例新冠肺炎感染、1例未指明的感染和1例其他原因;全部与研究药物不相关)。
关于两个治疗组之间的比较,PolaBR组的中位 PFS 为5.5个月,估计29.4%的患者在12个月时无复发,而 PolaR 组为5.1个月,估计21.1%的患者在1年时无复发(HR=0.8826,P= 0.7452)。PolaBR 组的中位 DFS 为12.7个月,PolaR组为9.6个月 (HR= 0.9142,P= 0.7940)。2组治疗在缓解率和生存期方面均无差异。
安全性
31例患者在治疗期间发生88起AE,其中22起≥3级;共发生20起血液学事件,其中16起≥3级,包括1起白细胞减少、11起中性粒细胞减少、3起血小板减少和1起贫血,其余4起事件为2起2级血小板减少和2起2级贫血。PolaBR 组仅发生1起3级发热性中性粒细胞减少(与研究药物相关)。

所有患者共发生5起严重AE,即1起肺炎(与研究药物无关)、1起Stevens-Johnson 综合征(与 polatuzumab 相关)、2起因治疗相关血液学 AE 住院和1起胃肠道出血导致的死亡(无关)。共发生8起神经病变,均为1-2级,与 polatuzumab 相关;此外共发生4起感染,均在 PolaBR 组。
在 PolaBR 组中,20例患者发生至少1起毒性,其中18起血液学事件(13起≥3级)和20起非血液学事件(5起≥3级)。在 PolaR 组中,11例患者发生至少1起AE:包括同一患者发生的2起血液学毒性(4级白细胞减少和中性粒细胞减少,均在粒细胞集落刺激因子支持后消退)和25起非血液学AE(2例≥3级)。两组在 AE 发生方面存在统计学显著差异:PolaBR组血液学 AE 和≥3级AE更多,而 PolaR 组神经疾病更多(表3)。
讨论
本研究证实了 Pola(B)R 方案在真实世界中治疗 R/R DLBCL 的可行性和安全性:在既往接受过多线治疗且末次治疗难治的患者比例较高 (81.8%)的患者中,ORR为32.7%,最佳 ORR 为49.1%(CR率27.3%)。本研究与Pola为基础方案治疗R/R DLBCL的其他真实世界研究疗效结果无差异(表4),尤其是中位 PFS 和中位 OS 以及 ORR 和 CR 率相似。

作者还分析了接受苯达莫司汀治疗的患者和未接受苯达莫司汀治疗的患者之间的差异,结果未发现2个治疗组在缓解率或生存期方面的差异,但在 AE 发生率方面有所差异,尤其是和PolaBR 组的≥3级血液学毒性更高。这表明PolaBR和PolaR的疗效相同,但至少有3个原因使首选 PolaR 方案成为首选:患者的毒性较小、从联合方案移除一种药物可节约成本、医生可在后续治疗线中使用苯达莫司汀作为复发后的挽救治疗。
虽然PolaR 组中神经病变的发生率显著较高(中位6个周期 vs 4 个周期),这可能是由于患者接受的治疗周期更多,但两组中因 AE 而停止治疗的患者百分比均非常低 (3.6%),从而证实了该方案的安全性可控。
Polatuzumab 也可能是 CAR-T 细胞治疗或移植的有效桥接治疗,或可视为 CAR-T 细胞治疗失败后的挽救治疗。但本研究未解决这个问题,仅3例患者使用 polatuzumab 作为移植的桥接。
参考文献
Lisa Argnani,et al.Real-world Outcomes of Relapsed/Refractory Diffuse Large B-cell Lymphoma Treated With Polatuzumab Vedotin-based Therapy.Hemasphere . 2022 Nov 11;6(12):e798. doi: 10.1097/HS9.0000000000000798.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言