病例分享 | 肺细支气管腺瘤(BA)与浸润性黏液腺癌诊断及鉴别诊断
2024-06-27 上海阿克曼病理 上海阿克曼病理 发表于上海
介绍细支气管腺瘤与浸润性黏液腺癌的病例,包括临床表现、影像学特征、病理特点、鉴别诊断等,强调两者在临床病理诊断中的鉴别要点。
细支气管腺瘤与浸润性黏液腺癌均为肺部伴有突出的黏液特征的肿瘤,两者组织学相似,均具有沿肺泡壁生长的模式,大量细胞外黏液和黏液细胞,可以出现不连续的跳跃式生长方式,并且二者的细胞均表现出温和的状态,异型性较小,因此是临床病理诊断工作中的重要鉴别诊断,最为关键的诊断鉴别要点是准确识别是否存在连续的基底细胞和腔面的纤毛细胞。
例1:
患者,男,65岁,发现右肺下叶结节3年,期间患者偶有咳嗽、咳痰,为黏液样浓痰,无痰中带血、无胸闷、气促及呼吸困难等症状。无吸烟史,既往有“2型糖尿病”病史,其余无特殊。
01 辅助检查:
CT示:右肺下叶基底段的部分实性结节,大小1.8cmx1.4cm,平均CT值约-252.1HU,纵隔内未见明显肿大的淋巴结。
02 大体检查:
右肺下叶肿物:楔形切除肺组织一块,大小6.2cmx3.5cmx1.2cm,胸膜下肺实质内可见一大小1.5cmx1.5cmx0.8cm的灰白色结节,无胸膜牵拉,肿瘤无明显包膜,界限尚清,切面呈灰白色,实性,有黏液感。
03 镜下所见:
肿瘤与周围肺组织分界清楚,但无明显包膜,排列成大小不一,形状不规则的腺管状结构,局部可见乳头状结构,腔内可见黏液分泌,局部可见厚壁血管穿行。肿瘤性腺管具有双层细胞,即腔面细胞及外周的基底细胞,腔面细胞主要为柱状细胞及黏液细胞,细胞核位于细胞基底部,腔面可见纤毛,基底细胞呈圆形或椭圆形,形态温和,未见核分裂象及坏死。

CT示:右肺下叶基底段的部分实性结节。
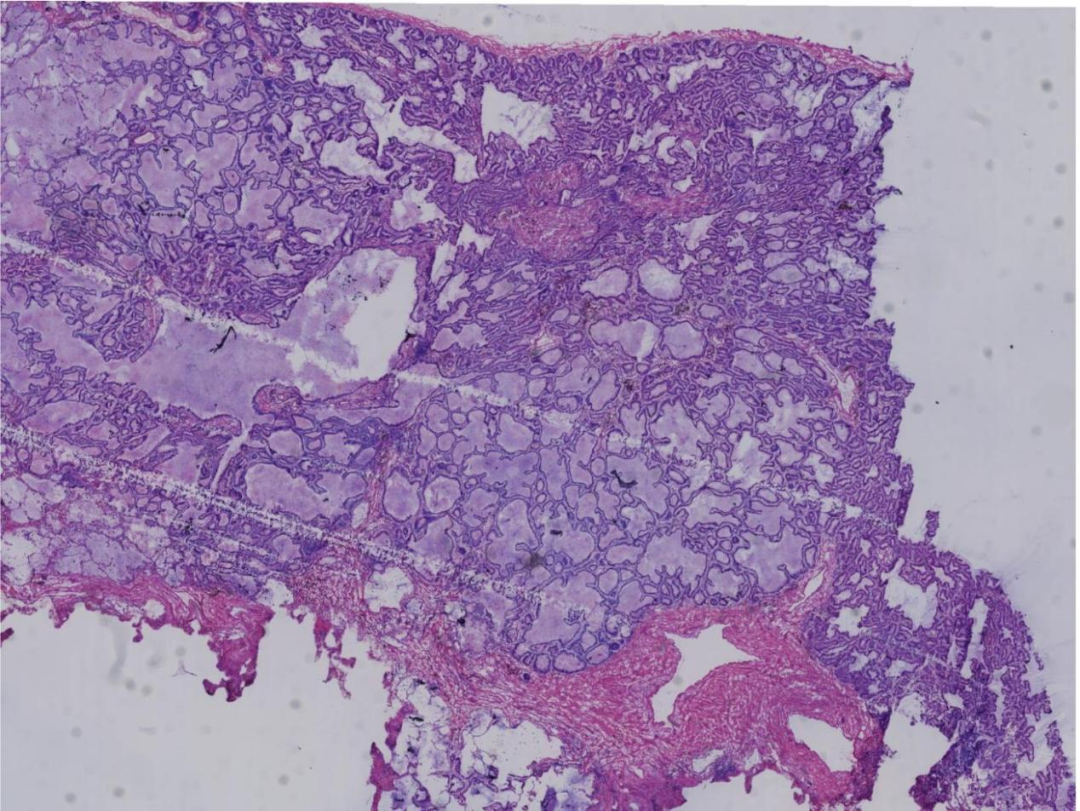
冰冻切片内可见肿瘤组织呈管状及不规则状腺样结构,可见腔内黏液。

肿瘤与周围肺组织分界清楚。

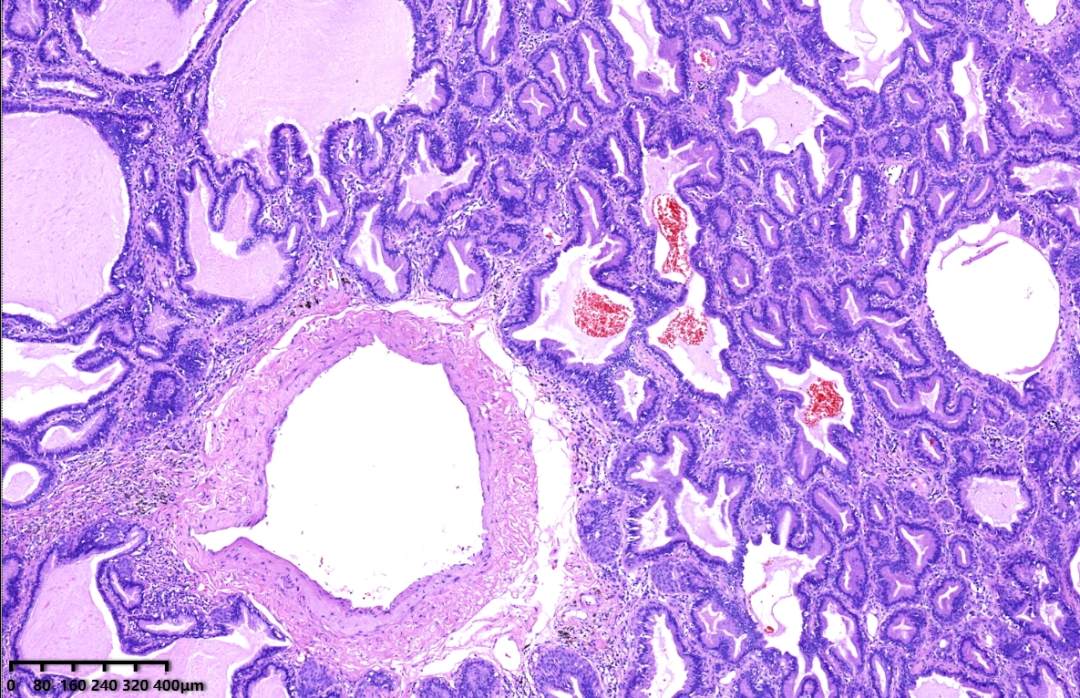
低倍镜,肿瘤呈大小不一,形状不规则的腺管状结构,局部可见乳头状结构,腔内可见黏液,肿瘤内可见厚壁血管穿行
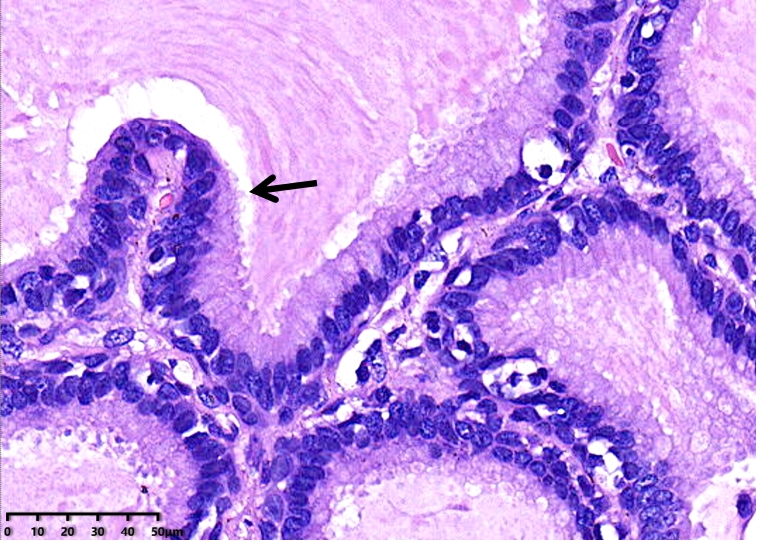

高倍镜,肿瘤性腺体具有双层细胞,内侧的腔面细胞,可见纤毛(黑色箭头)及外周的基底细胞(红色箭头),2种细胞形态异型性均较小。

CK5/6 基底细胞(+)
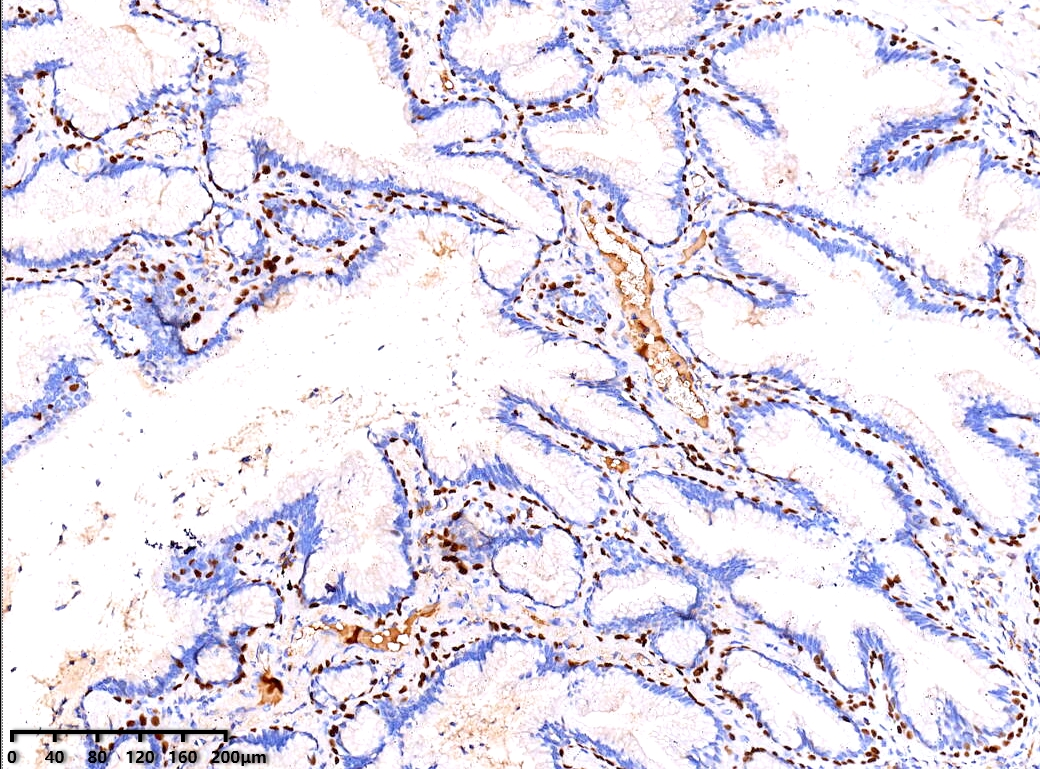
P40 基底细胞(+)

Ki67约1%
04 病理诊断:
细支气管腺瘤,近端型。
例2:
患者,男,53岁,CT检查发现左肺上叶结节,无痰中带血、无胸闷、气促及呼吸困难等症状。有吸烟史16年,既往有阑尾炎手术史。
01 辅助检查:
CT示:左肺上叶前段可见部分实性结节,大小约1.4cmx1.1cm,平均CT值约-156.1HU,边缘见少许支气管影及上叶舌段血管贴边现象。
02 大体检查:
左肺上叶肿块:楔形切除肺组织一块,大小2.5cmx1.5cmx0.5cm,切开见一大小1.2cm的灰白色实性区。
03 镜下所见:
肿瘤与周围肺组织分界清楚,但无明显包膜,排列成形状不规则的腺管状结构,无乳头状结构,无腔内黏液聚集。腔缘的细胞为立方状或柱状,腔缘细胞可见有顶浆分泌样小突起,无典型的纤毛结构及黏液细胞,腔缘细胞外周存在基底细胞。

CT示:左肺上叶肿块,界限相对清楚。
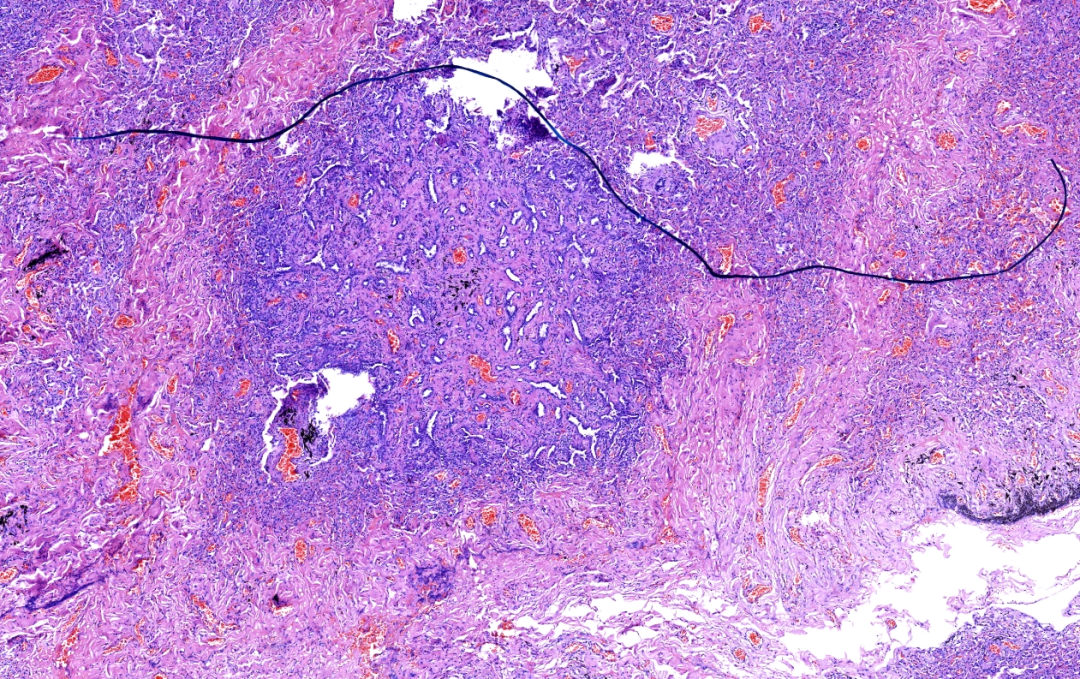
低倍镜,肿瘤与周围肺组织具有清晰的分界。

肿瘤呈腺样或小管状,无乳头状结构及腔内黏液分泌。

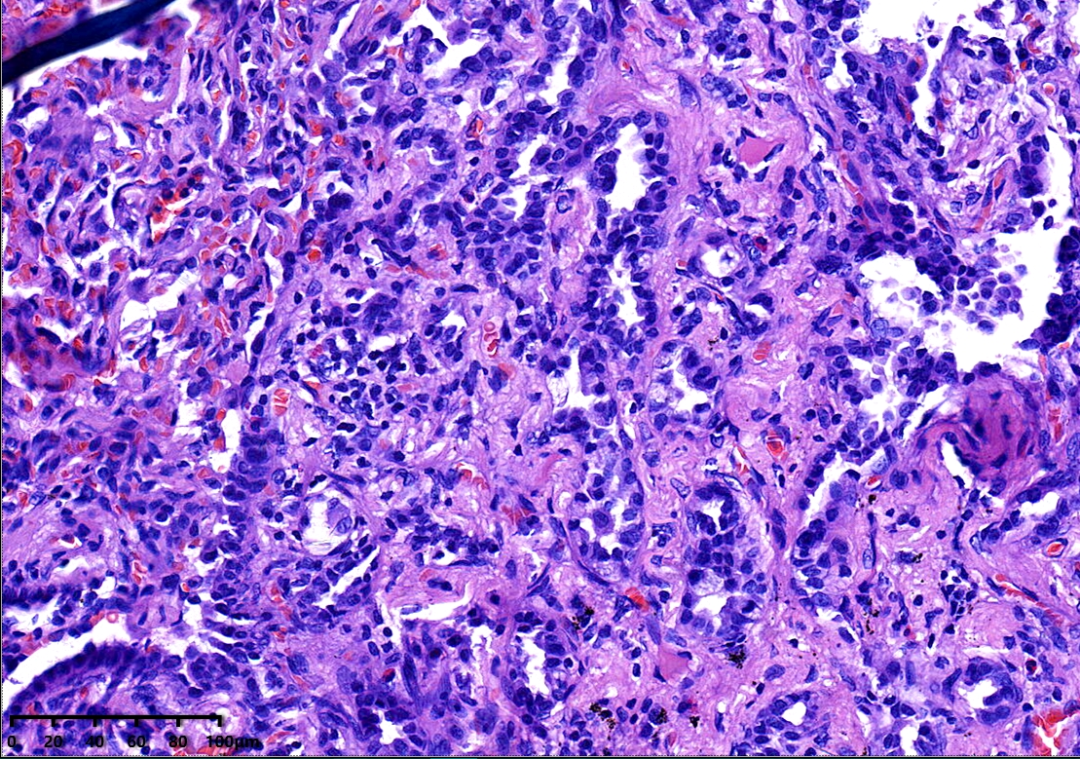

高倍镜,肿瘤细胞大小相对一致的立方状及柱状上皮细胞,无腔面纤毛细胞,细胞异型性小,染色质均一。

P40 基底细胞(+)
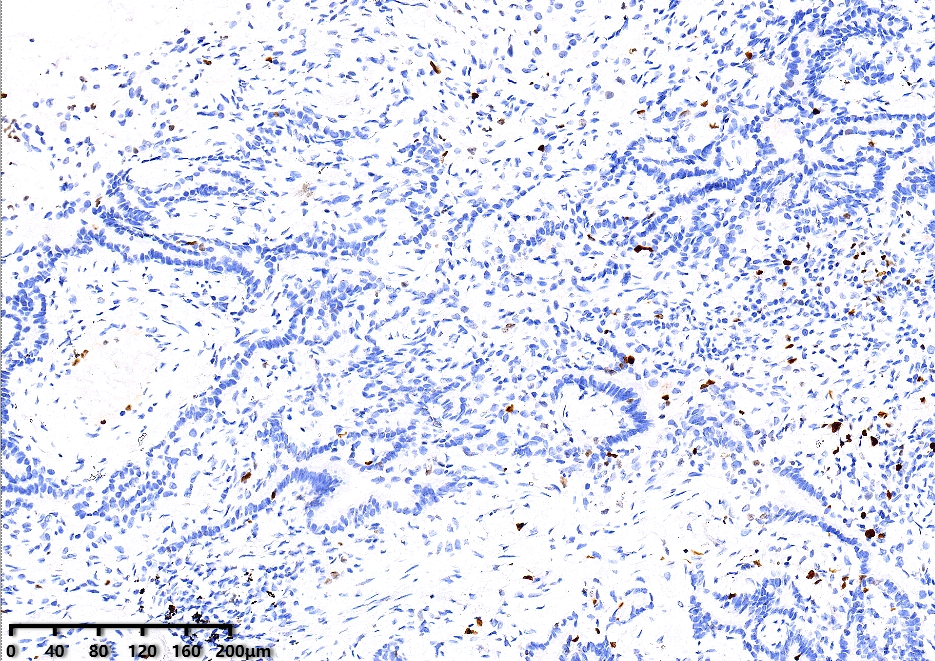
Ki67约1%
04 病理诊断:
细支气管腺瘤,远端型。
例3:
患者,男,70岁,3年前体检发现右肺结节,无痰中带血、无胸闷、气促及呼吸困难等症状。有吸烟史20年,既往有阑尾炎及前列腺手术史。
01 辅助检查:
CT示:右肺下叶后基底段见部分实性结节,大小约1.5cmx1.1cm,可见分叶,毛刺、胸膜凹陷征象,增强扫描轻度均匀强化。
02 大体检查:
右肺下叶结节,楔形切除肺组织一块,大小5.5cmx2.5cmx2.0cm,切开胸膜下见一直径1.2cm的灰白色结节,结节切面胶样,黏液感。
03 镜下所见:
肿瘤与周围肺组织分界不清楚,呈多灶浸润性分布。排列成大小不一,形状不规则的腺管状结构,呈贴壁状生长及跳跃式生长,腔内可见黏液分泌。肿瘤细胞胞质内充满黏液,细胞核卵圆形,位于基底部,核仁明显。
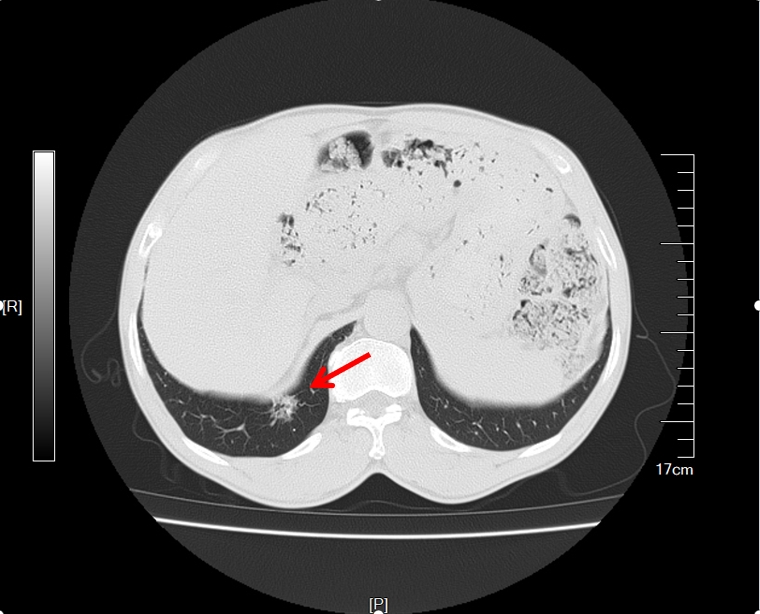
CT示:右肺下叶结节,边缘不规则,分页、毛刺状。
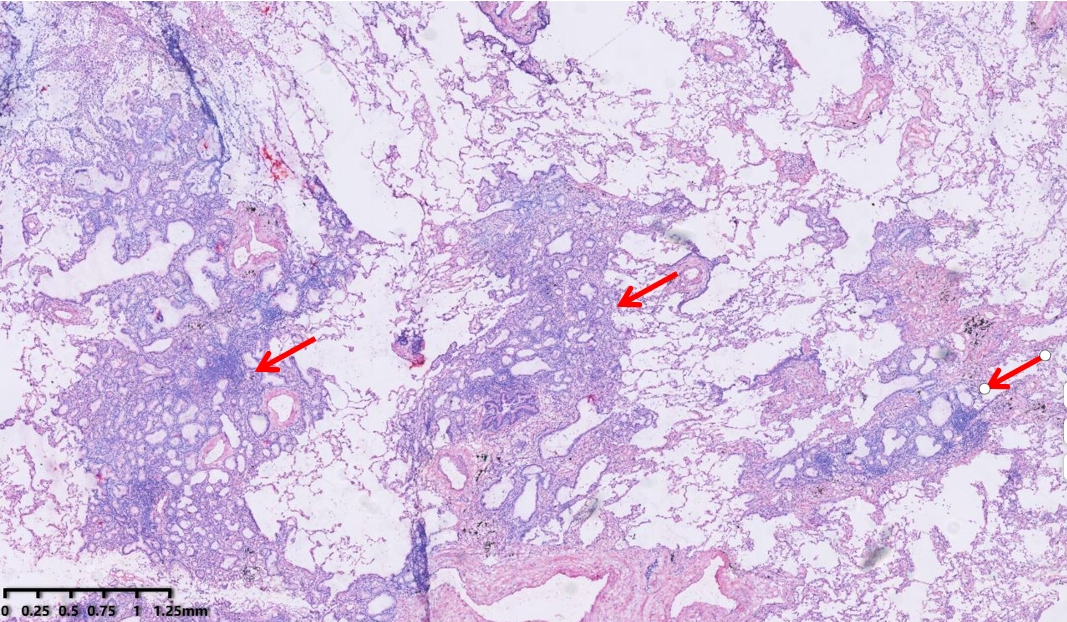
冰冻切片内可见肿瘤呈多灶跳跃分布。

冰冻切片显示肿瘤呈腺样,腺腔内可见黏液,细胞胞质内含黏液,细胞核位于基底部。
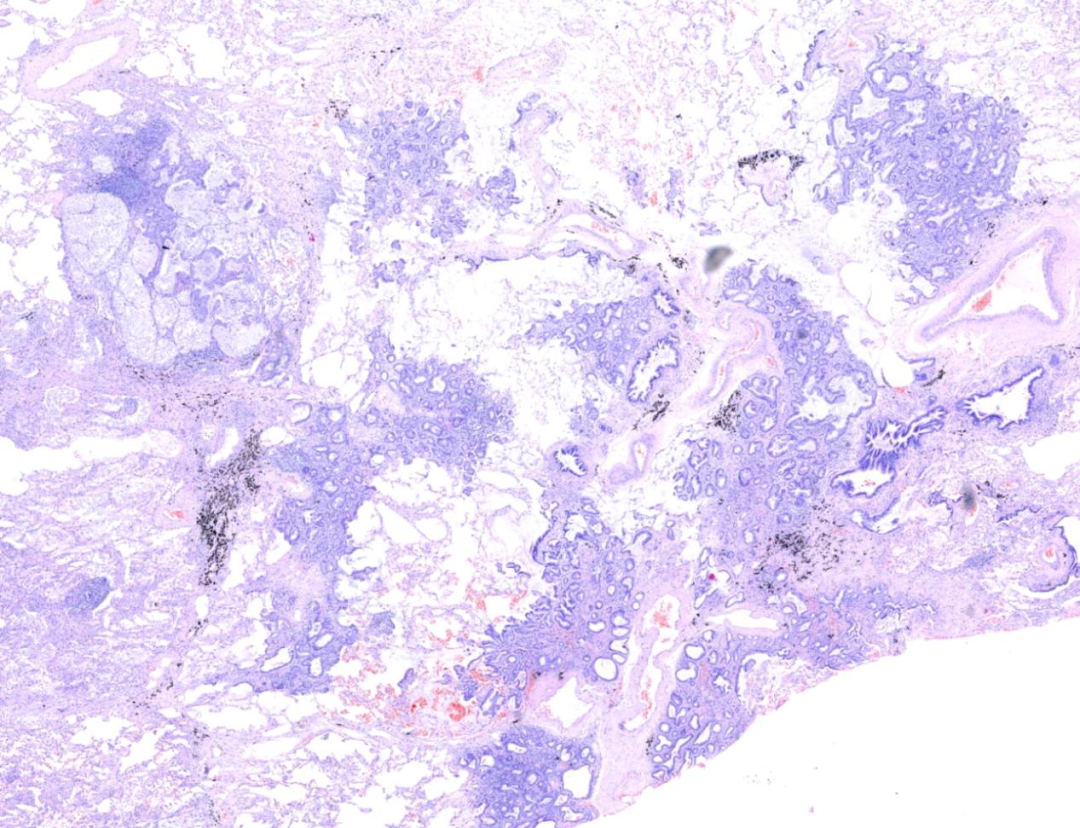
肿瘤不规则分布,无明显界限,与周围肺组织分界不清。


低倍镜,肿瘤呈大小,形态不规则的腺样结构,可见贴壁状生长及不连续的跳跃式生长,腔内充满黏液。


高倍镜,肿瘤主要为黏液细胞,胞质内具有黏液,细胞核位于基底部,可见明显核仁。

CK5/6(-)

P40(-)

Ki67增值指数约20%
04 病理诊断:
浸润性黏液腺癌。
讨 论
8253/3 浸润性黏液腺癌
8140/0 细支气管腺瘤
临床特征:
细支气管腺瘤好发于老年人,发病年龄55-83岁,中位年龄72岁,无明显性别差异,肿瘤的发生与吸烟无明显相关性,肿瘤一般较小,临床症状一般不明显,大部分患者为体检时发现。
影像学表现: 与早期肺的腺癌具有相似之处,主要表现为外周肺组织内磨玻璃样结节或部分实性结节。
细支气管腺瘤为良性肿瘤,术后极少复发或转移,预后较好。
浸润性肺黏液腺癌占肺腺癌的2%~5%,可与非黏液腺癌混合存在,对于非黏液腺癌成分占比大于10%的可定义为混合型黏液腺癌。黏液腺癌多见于中老年人,尤其是60岁以上的人群。临床表现不特异,包括咳嗽、咳痰、咳血、胸痛、气促等其他类型的肺癌的相关临床表现。
黏液腺癌以分泌黏液为特点,因此CT上以单发或多发磨玻璃病变、大片渗出、肺实变、空洞、支气管征为主要表现,但纵隔淋巴结肿大少见。预后较非黏液性腺癌差,更容易发生淋巴结转移。
病理学特征:
01 大体特点
细支气管腺瘤:肿瘤一般位于周围肺组织内,大体为灰白、灰褐色的实性结节,切面实性,伴有黏液感,部分可有囊性变,肿瘤边界清楚但无明显包膜,肿瘤一般较小,最大径0.4-2.5 cm(平均1.0 cm)。
浸润性黏液腺癌:肿瘤通常表现为边界不清的病灶,常常累及胸膜,出现胸膜牵拉现象,无包膜,外观柔软,切面呈胶状、黏液状。肿瘤大小0.7-8.5cm(平均1.7cm)。
02 镜下表现
细支气管腺瘤:组织学多样,不同的排列方式,常见的为管状,不规则腺样,乳头状及微乳头状结构,腔内可见多少不等的黏液,根据组织学结构不同分为近端型及远端型,两者均有连续的基底层细胞存在。近端型呈现典型的纤毛黏液结节性乳头状肿瘤形态,以乳头样和腺腔样结构为主,肿瘤常伴随细支气管动脉束或中型动脉穿过。具有双层细胞结构,即腔面上皮细胞和外围连续存在的基底细胞(HE形态有时很难辨认基底细胞)。腔面上皮细胞包括黏液细胞 、柱状细胞,腔缘可见顶浆分泌小突起及纤毛。远端型组织学以腺管状结构为主,乳头状结构,纤毛细胞和粘液较少或无,腔面上皮细胞主要为立方或柱状的II型肺泡上皮细胞。细胞形态温和,缺乏非典型性,无明显核分裂及坏死。
浸润性黏液腺癌:常呈现附壁型为主的生长方式,包括腺泡、乳头状、微乳头状、实性或筛状生长模式,肿瘤细胞呈杯状细胞/柱状细胞形态,含丰富的细胞内黏液,肿瘤细胞核小,被推挤至细胞一侧或基底,肿瘤周围肺泡腔常充满黏液,可见肿瘤细胞沿肺泡腔播散。细胞异型性小,无明显核分裂象。如果黏液和非黏液成分混合,肿瘤中每种成分的含量均≥10%,则应将其分类为混合性浸润性黏液和非黏液腺癌。无明确分级规定,但建议病理报告将附壁型腺泡型等生长方式列出并计算各种成分的肿瘤占比。
03 免疫表型
细支气管腺瘤:腔面细胞CK7、TTF1、NapsinA阳性,PAS黏液阳性,CK20、Villin、CDX2阴性,基底细胞p40、p63、CK5/6阳性,Ki-67增殖指数低(<5%)。
浸润性黏液腺癌:CK7、HNF4α阳性,CK20及CDX2部分阳性,TTF1,NapsinA大部分阴性,SATB-2阴性。
分子遗传学
细支气管腺瘤:最常见的遗传学改变是BRAF突变,大部分发生在第15号外显
子的V600E内,少部分病例可伴有EGFR、ALK、RAS突变。
浸润性肺黏液腺癌:最常见的分子改变是KRAS突变(约占76%),最常见的
2个KRAS突变点是p.G12D和p.G12V。其次是NRG1融合(7%)、ERBB2改变(6%)。
预后:
细支气管腺瘤:是一组良性病变或恶性潜能未定型肿瘤,临床可按肺部良性肿瘤
处理,手术完整切除预后良好,罕见复发及远处转移。
浸润性肺黏液腺癌:整体预后较其他亚型肺腺癌差,可能的原因是有更高的转移
率,包括肺内转移、血行转移和淋巴转移等,主要包括手术切除、化疗、放疗等。
早期手术切除被认为是主要的治疗方式,标准手术方式是肺叶切除术+ 系统性淋巴结清扫术。
鉴别诊断:
1. 细支气管腺瘤与浸润性黏液腺癌鉴别:两者容易混淆,尤其是在术中冰冻切片内,鉴别诊断较困难。鉴别重点在于辨别基底细胞。浸润性黏液腺癌无基底细胞存在,腔面细胞无纤毛,借助免疫组化p40、p63及CK5/6等可以明确诊断;此外,浸润性肺黏液腺癌常累及胸膜出现胸膜牵拉现象。
2. 细支气管腺瘤与浸润性非黏液腺癌(腺泡型)鉴别:远端型细支气管腺瘤以管状结构或平坦型腺样结构为主,易与腺泡型腺癌混淆。腺泡型腺癌细胞异型性大,核浆比高,核仁明显,腺体结构周围可见促纤维反应,腺体外周无基底细胞存在,免疫组化p40、p63及CK5/6阴性。
3. 浸润性黏液腺癌与转移性腺癌鉴别:转移性腺癌包括来源于胰胆系统、胃肠道和卵巢的黏液腺癌。乳腺黏液癌通常表达GATA3和ER。SATB2、CK20和CDX2阳性支持黏液型结直肠型腺癌,黏液型结直肠型腺癌有时也表达TTF1。
*本文(包括图片)均为作者投稿, 仅供行业交流学习用,不作为医疗诊断依据。
参考文献
[1] Liu X, Xu Y, Wang G, et al. Bronchiolar adenoma/ciliated muconodular papillary tumour: advancing clinical, pathological, and imaging insights for future perspectives. Clin Radiol. 2024;79(2):85-93.
[2] Chen Z, Li M, Ma K, et al. Analysis of the clinicopathological characteristics, genetic phenotypes, and prognostic of pure mucinous adenocarcinoma. Cancer Med. 2020 Jan;9(2):517-529.
[3] 刘加豪,许竞泽,帅立雄等.细支气管腺瘤的临床病理学特征[J].诊断病理学杂志,2023,30(09):899-900+906.
[4] Kriegsmann M, Harms A, Longuespée R, Muley T, et al. Role of conventional immunomarkers, HNF4-α and SATB2, in the differential diagnosis of pulmonary and colorectal adenocarcinomas. Histopathology. 2018 May;72(6):997-1006.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#细支气管腺瘤# #浸润性黏液腺癌#
49