Nature:兴奋性神经元调节睡眠质量和深度
2022-12-26 brainnew神内神外 brainnew神内神外 发表于安徽省
兴奋性神经元中的 SIK3 通路会改变时间常数,以减缓S过程或睡眠需求的动态。大脑皮层兴奋性神经元中的 SIK3和HDAC4 参与调节NREMS delta功率或睡眠深度。
2022年世界杯决赛正在进行中,无数球迷正在熬夜看球。
目前,我们对睡眠和觉醒在神经回路层面调节的研究取得了不错的进展。然而,调节睡眠的细胞内信号通路和这些细胞内机制起作用的神经元群在很大程度上仍然未知。
近日,Hiromasa Funato团队在小鼠中使用正向遗传学(forward genetics)方法,鉴定出组蛋白脱乙酰酶4(HDAC4)为睡眠调节分子,发现盐诱导激酶3(SIK3)的底物Hdac4的单倍不足会增加睡眠。他们的成果发表在Nature杂志上,名为“Kinase signalling in excitatory neurons regulates sleep quantity and depth”。
 相关阅读:
相关阅读:
Nature:睡多久谁说了算?刘清华团队揭示调控睡眠时间的关键分子通路
Nat Commun:复旦黄志力/杨素荣揭示睡眠时相转换的新环路机制
Nat N+Nat C:中科院神经所刘丹倩组和徐敏组在快速动眼睡眠研究领域取得突破
睡眠具有稳态调节的性质,最新的报道称,有几个神经元群参与睡眠稳态。然而,目前尚不清楚哪些细胞内事件通过特定细胞群调节睡眠的时间和深度。此前,本文作者通过EEG和EMG的随机诱变小鼠筛选,将 SIK3 确定为睡眠稳态的关键组成部分。Sik3 中的剪接突变,即 Sleepy (Slp) 等位基因,导致 NREMS(non-rapid eye movement sleep) 期间 NREMS 时间和 EEG delta 功率增加,这是睡眠需求和睡眠深度的指标。神经元中 SIK3(SLP) 的表达增加了 NREMS期间的睡眠时间和 EEG delta 功率。
本研究,作者使用无偏见的正向遗传学方法,结合小鼠靶向遗传分析,来阐明 SIK3 信号传导的上游和下游分子通路,并确定这些通路在大脑中的哪个位置,以及在哪些类型的神经元中调节睡眠。
Hdac4和Hdac5的减少
会增加 NREMS
通过对随机诱变的 C57B/6J 雄性小鼠进行显性筛选,建立了一个长睡眠谱系 Sleepy2 (Slp2)。N2后代表现出减少总清醒时间的显性特征(图1a)。分析表明,Slp2 谱系的 12 只长睡眠小鼠中有 10 只在剪接位点具有 Hdac4 突变。
纯合 Hdac4 SA 小鼠具有异常的 Hdac4 转录物,缺乏 HDAC4 蛋白产生(图1c)并且表现出严重的生长迟缓。相比之下,杂合子 Hdac4 SA小鼠健康且可育。与 Hdac4 +/+小鼠相比,Hdac4 SA/+小鼠的苏醒时间更短,NREMS 时间增加(图1d),并且在基线和睡眠剥夺后的 NREMS 期间 EEG delta 功率更高(图1e,f)。因此,Hdac4 的遗传或药理学抑制会促进 NREMS。
纯合子 Hdac5SA 小鼠可育的且没有表现出明显的异常。Hdac5SA小鼠表现出增加的 NREMS 时间和深度(图1g-i)。Hdac4 SA/+ 和 Hdac5 SA/+的双杂合性小鼠的总 NREMS 时间具有累加效应(图1j)。
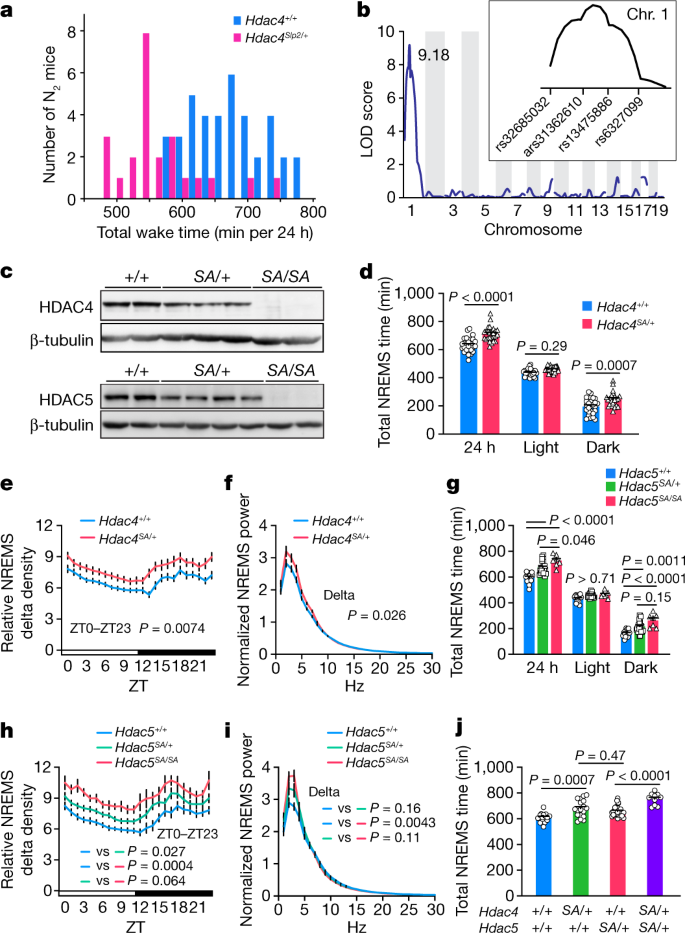
图1. Hdac4 和 Hdac5 的功能缺失突变会增加 NREMS。
SIK3通过HDAC4增强NREMS
在大脑皮层中,HDAC4 核免疫反应的强度在ZT12.5时比在 ZT6 时更高(图2a、b)。睡眠剥夺后,皮质中核部分中的 HDAC4 低于自由睡眠(图2c)。这些发现表明,当睡眠需求高时,HDAC4核水平会降低,这与杂合子 Hdac4 功能不全的 NREMS 增加一致。
与野生型 SIK3 相比,SIK3(S551A) 进一步抑制了 HDAC4 对MEF2C 依赖性转录的反式抑制(图2e)。SIK3 和 SIK3(S551A) 的这种抑制被 HDAC4(S245A) 消除(图2f)。与野生型小鼠相比,Sik3Slp/+小鼠在脑匀浆中表现出 S245 处 HDAC4 磷酸化增加(图2g),并且在 ZT12.5 处HDAC4 核减少(图2d)。这些结果表明, S245 磷酸化影响SIK3(S551A) 和 SIK3(SLP) 对 HDAC4 功能的增益特性。
在 Sik3Slp 小鼠中表达 HDAC4(S245A) 消除了睡眠时间和 EEG delta 功率方面的嗜睡表型(图2l-o)。因此,抗磷酸化 HDAC4 的存在导致睡眠表型与 Hdac4 单倍量不足时相反,这掩盖了 Sik3Slp 突变的影响。

图2. SIK3–HDAC4 对睡眠和觉醒的相互作用。
SIK3激酶在NREM调控中的活性
LKB1 缺乏或 SIK3 的 T221 被丙氨酸取代可能会降低 NREMS。将他莫昔芬施用于 Syn1creERT;Lkb1flox/flox小鼠,以在神经元中诱导 LKB1 缺陷。这些小鼠表现出NREMS 时间减少和 NREMS delta 功率以及对睡眠剥夺的抑制反应(图3a-c)。
尽管纯合 Sik3T221A 小鼠表现出与 Sik3 缺陷小鼠相似的严重生长迟缓和过早死亡,但杂合 Sik3T221A小鼠是健康的并且表现出轻度降低的 NREMS delta 功率,且NREMS 时间没有变化(图3d-f)。
杂合 Sik3Slp;T221A 小鼠表现出更长的总清醒时间、更短的总 NREMS 时间和更短的 NREMS 发作持续时间(图3j-l)。这些结果进一步支持 Sik3Slp小鼠中增加的 NREMS 时间和增量密度取决于完整的激酶活性。
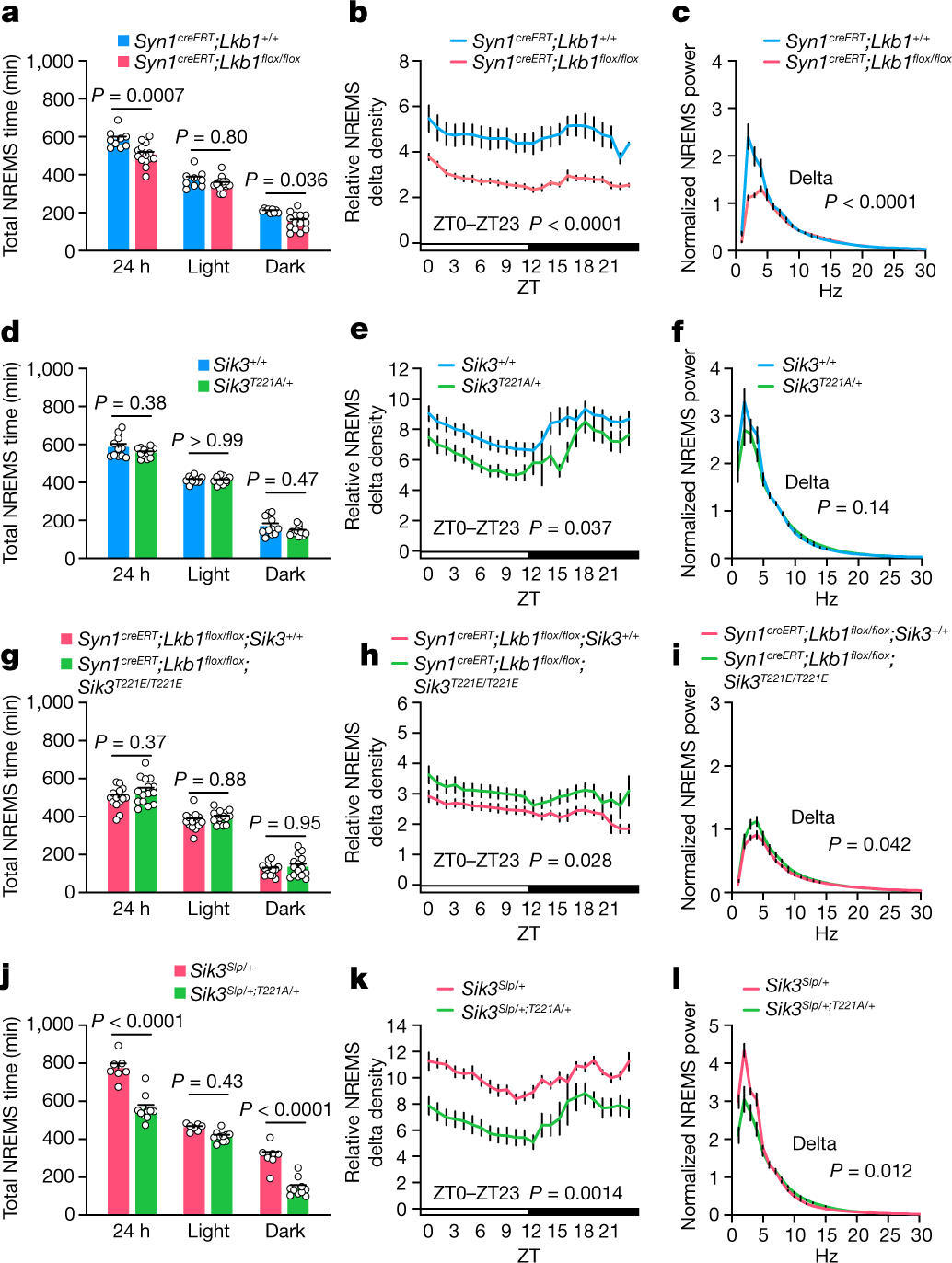
图3.神经 LKB1 缺陷和 SIK3 激酶活性修饰小鼠的睡眠-觉醒
睡眠需求的转录变化
来自接受 AAV-Sik3Slp 的皮质样本在谷氨酸能神经元中有 133 个上调基因和 32 个下调基因(图4a、c、d、f、g)。睡眠剥夺主要影响谷氨酸能神经元中的基因表达,但其他细胞类型也受到影响(图4b、c)。当将睡眠剥夺小鼠的大脑皮层与自由睡眠小鼠的大脑皮层进行比较时,谷氨酸能神经元中分别有 2,685 个基因上调和 394 个基因下调(图4e-g)。
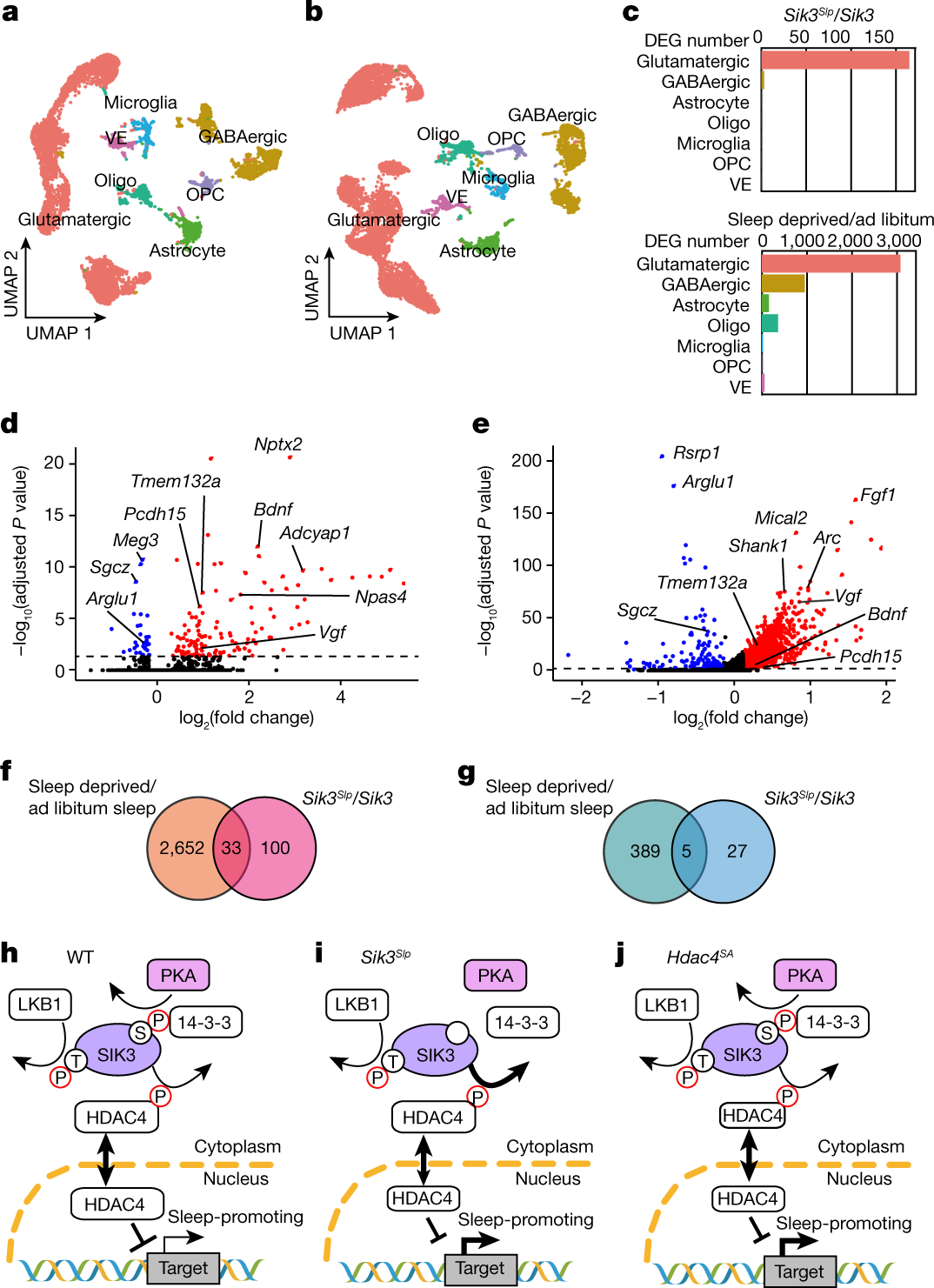
图4. 单核转录组变化和与睡眠需求相关的分子通路。
结 论
作者在Sik3Slp小鼠中证明了,兴奋性神经元中的 SIK3 通路会改变时间常数,以减缓S过程或睡眠需求的动态。大脑皮层兴奋性神经元中的 SIK3和HDAC4 参与调节NREMS delta功率或睡眠深度。
此外,下丘脑兴奋性神经元中的 SIK3和HDAC4 参与 NREMS 时间或睡眠量的调节。阐明调节睡眠时间和深度的细胞内信号机制,最终将使我们能够理解人们为什么睡觉,也能了解睡眠障碍的病理生理学并制定治疗干预措施。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#Lancet#学习了
78
不错!!!学习了
67