Lancet Oncol:IMWG关于多发性骨髓瘤相关肾损害的管理建议
2023-07-11 聊聊血液 聊聊血液 发表于上海
肾损害(Renal impa。irment,RI)是多发性骨髓瘤(MM)的主要特征之一。
多发性骨髓瘤肾损害
肾损害(Renal impairment,RI)是多发性骨髓瘤(MM)的主要特征之一,高达50%的MM患者在诊断时存在肾损害(定义为估计的肾小球滤过率 [eGFR] <60 mL/min/1.73 m²),且2-4%的患者需要透析。不过各研究中报告的肾损害发生率存在差异,可能部分归因于定义的不同,包括血清肌酐浓度高于2mg/dL 或高于正常值上限,eGFR低于60 mL/min/1.73m²或低于40 mL/min/1.73m²。
肾损害可导致MM患者的总生存期缩短和早期死亡风险增加,相对于不伴肾损害的MM患者,伴肾损害的新诊断患者发生骨髓瘤进展或死亡的相对风险为1.07,而复发性或难治性患者为1.20。新疗法(如蛋白酶体抑制剂、免疫调节剂和单克隆抗体)显著改善了总生存期和肾功能,尽管肾功能改善与生存期延长相关,但在MM诊断时存在肾损害患者的总生存期仍低于无肾损害患者。
引入新的抗骨髓瘤药物增强了诊断时和复发或难治性MM患者的治疗选择,但必须对肾损害患者进行特殊考虑。基于此,国际骨髓瘤工作组 (IMWG) 审查了截至2022年12月31日发表的数据,更新了2016年关于多发性骨髓瘤患者肾损害的管理建议,近日发表于《The Lancet Oncology》。
多发性骨髓瘤患者肾损害的病理生理学
MM患者的肾损害主要归咎于单克隆游离轻链 (FLC) 对肾小球和肾小管的毒性作用。在生理条件下,FLC可通过肾小球自由滤过,通过megalin—cubulin受体复合物被近曲小管细胞内吞,并分解代谢。而在多发性骨髓瘤患者中,单克隆 FLC的过度生成可超过近曲小管细胞的吸收和分解代谢能力,近端小管中残留的FLC可激活凋亡分子级联反应并诱导炎症,从而导致纤维化。到达远端肾单位的未吸收FLC可与 Tamm-Horsfall 蛋白相互作用并形成聚集体,沉淀并导致管型形成,随后出现肾小管梗阻和炎症。这些是导致轻链管型肾病的主要病理生理机制,在大多数多发性骨髓瘤患者中发现,可导致急性肾损伤。当浆细胞疾病背景下发生轻链管型肾病时,称为骨髓瘤管型肾病。
可能共存且与整个单克隆免疫球蛋白或其片段沉积或沉淀相关的其他肾脏疾病包括免疫球蛋白相关淀粉样变性(immunoglobulinrelated amyloidosis)、单克隆免疫球蛋白沉积病(monoclonal immunoglobulin deposition disease)、轻链近端小管病(light-chain proximal tubulopathy)、范可尼综合征(Fanconi syndrome)、冷球蛋白血症性肾小球肾炎(cryoglobulinaemic glomerulonephritis,I型和 II 型)、伴有单克隆免疫球蛋白沉积的增生性肾小球肾炎(proliferative glomerulonephritis with monoclonal immunoglobulin deposits)、冷冻晶体球蛋白血症或结晶球蛋白诱导的肾病(cryocrystalglobulinaemia or crystalglobulin-induced nephropathy)、结晶贮存组织细胞增多症(crystalstoring histiocytosis)、免疫触须样肾小球肾炎(immunotactoid glomerulonephritis)和伴单克隆丙种球蛋白病的 C3 肾小球病(C3 glomerulopathy with monoclonal gammopathy)。在不存在其他症状性MM的情况下,至少存在一种与肾毒性单克隆免疫球蛋白生成相关的实体,则属于具有肾脏意义的单克隆丙种球蛋白病(MGRS)。
非免疫球蛋白相关因素也可能导致MM患者出现肾损害,包括脱水、高钙血症、感染、肿瘤溶解综合征、肾毒性药物(如非甾体抗炎药、造影剂、抗生素、利尿剂和肾素-血管紧张素-醛固酮系统阻滞剂)和抗骨髓瘤治疗,包括双膦酸盐和可能的卡非佐米。考虑到多发性骨髓瘤诊断时的中位年龄约为70岁,正常年龄相关的肾功能下降和存在合并症(如糖尿病、动脉粥样硬化性血管疾病和心力衰竭)可能导致患者易患肾损害。
MM患者肾损害的诊断和分期
所有MM和肾损害患者均应在诊断和疾病评估时进行血清肌酐、eGFR、电解质和FLC测量以及24h尿液采集样本的总蛋白、尿电泳和免疫固定电泳(A级推荐)。如果检测到非选择性蛋白尿(主要是白蛋白尿)或受累血清FLC值低于500mg/L,且无其他已知的肾损害加重诱因(如肾毒性药物、高钙血症、感染和脱水),则应进行肾活检以确定肾损害的原因,尤其是在皮下脂肪或其他组织中不存在淀粉样物质的情况下(B级推荐)。
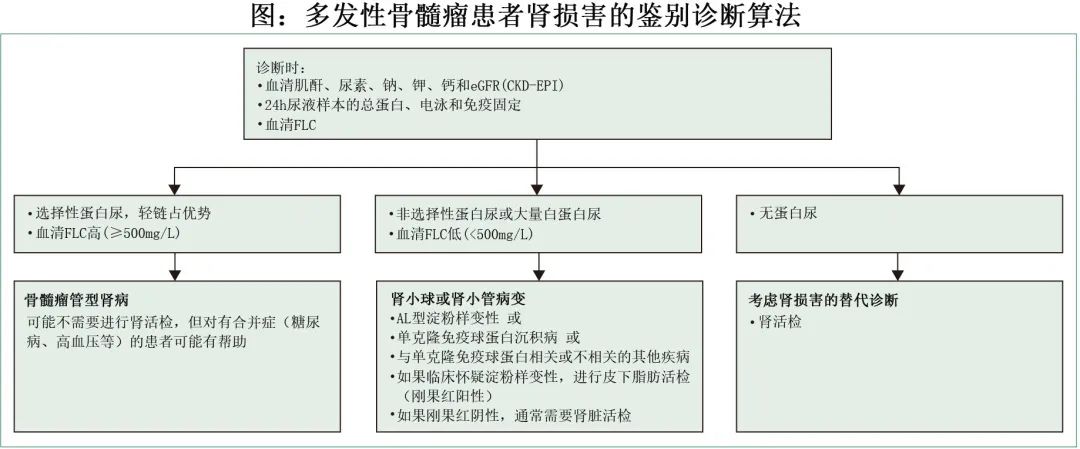
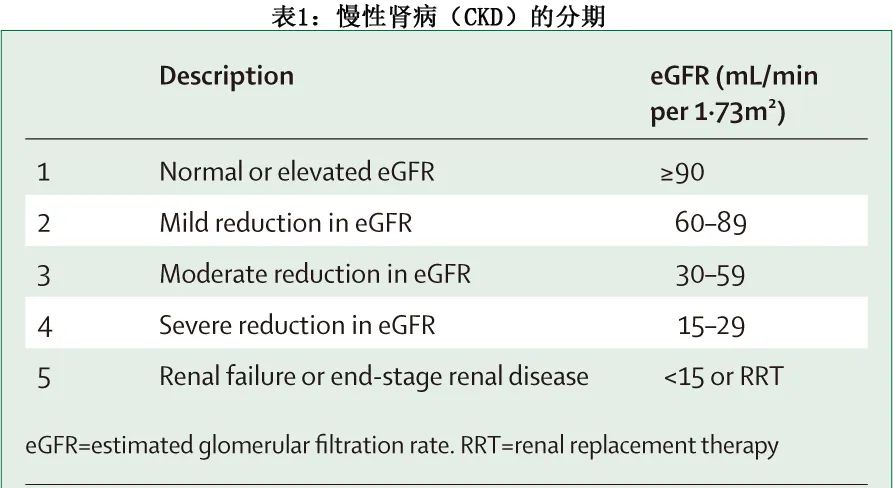
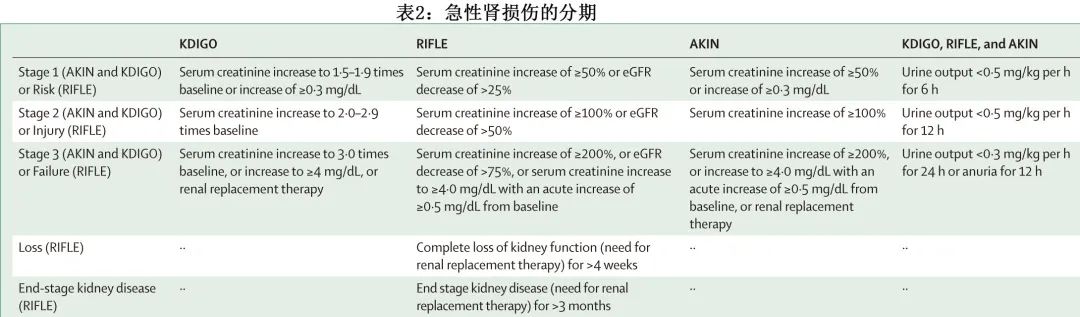
应使用CKD-EPI (Chronic Kidney Disease Epidemiology Collaboration)公式评价肾功能,应使用 CKD 分期对血清肌酐浓度稳定的MM患者进行分类(表1;B级推荐)。如果可用,加入胱抑素 C 作为变量可改善 CKD-EPI 计算(包括肾损害检测的灵敏度和总生存期的预后价值)(B级推荐)。应该测量所有MM患者的基线β2-微球蛋白浓度(A级推荐)。对于急性肾损伤患者,应使用KDIGO、RIFLE和 AKIN 标准(表2;C级推荐)。
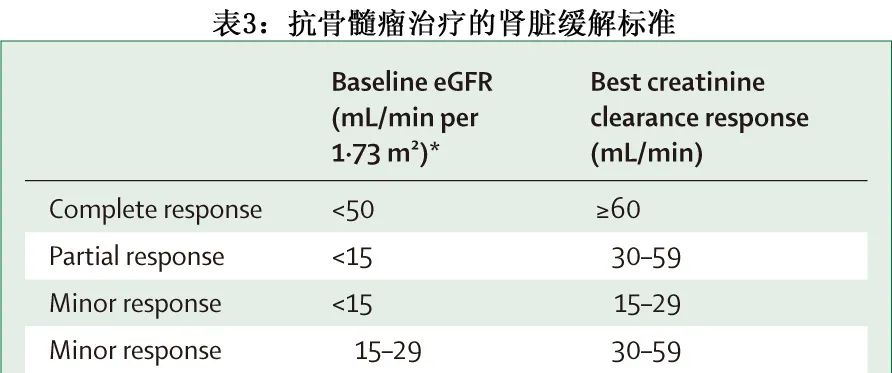
肾脏缓解标准
临床试验和日常临床实践中均应使用IMWG标准定义肾脏缓解(表3;B级推荐)。
支持性治疗
应在抗骨髓瘤治疗的同时开始高液体输注(至少≥3L/天或2L/m²/天)(B级推荐)。在逆转MM患者的肾损害方面,尿液碱化似乎没有提供优势(B级推荐)。双膦酸盐类可降低高钙血症患者的钙浓度,但帕米膦酸盐和唑来膦酸均不应用于MM伴重度肾损害患者(肌酐清除率<30 mL/min;A级推荐)。在接受慢性透析的患者中,如果无法将GFR率逆转至超过30 mL/min/1.73m²,可使用双膦酸盐治疗骨髓瘤相关骨病(D级推荐)。地舒单抗可能对高钙血症和肾损害患者有用,但应密切监测钙和磷酸盐浓度(B级推荐)。MM伴肾损害患者强烈建议避免使用肾毒性药物,如氨基糖苷类抗生素、肾素-血管紧张素-醛固酮系统阻滞剂、呋塞米、非甾体抗炎药和造影剂(A级推荐)。
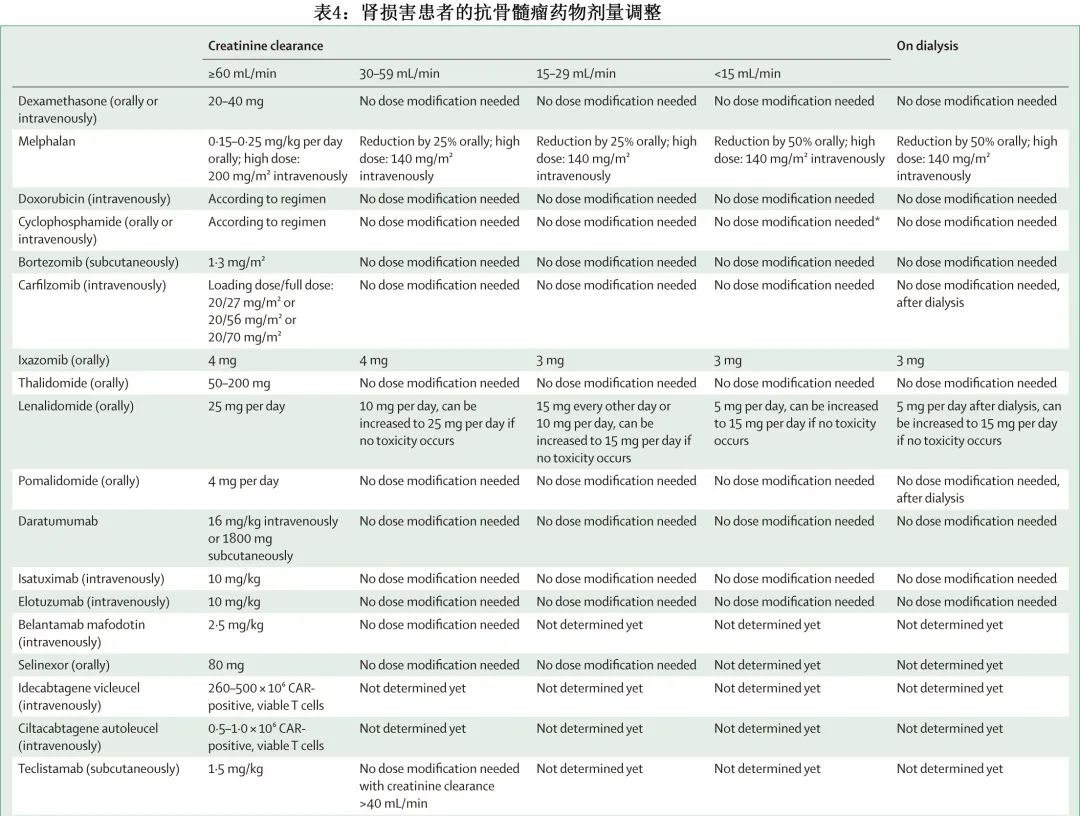
此外,多重用药在MM患者中很常见,尤其是存在合并症时,因此应特别注意抗骨髓瘤药物(表4)和合并用药的剂量调整。
机械方法
由于单克隆管型肾病,即使在MM伴急性肾损伤AKI患者中,单纯机械方法也无法改善总生存期或血液透析依赖(B级推荐)。机械方法联合抗骨髓瘤治疗可提高摆脱透析率(C级推荐)。3个月时,高截留量血液透析和传统高通量血液透析之间的摆脱透析率没有差异(C级推荐)。
抗骨髓瘤治疗
多发性骨髓瘤患者的肾损害(尤其是前期肾损害)是一种可能可逆的疾病,应立即治疗。新诊断MM伴肾损害患者改善的几率较高,而复发或难治性MM伴肾损害患者的管理更具挑战性。
大剂量类固醇为基础的治疗方案
大剂量地塞米松(口服或静脉给药)的推荐剂量为40mg/天(年龄≥75岁的患者为20mg),在治疗的第一个周期内进行3次脉冲给药,给药4天,停药4天,然后根据治疗方案进行给药(B级推荐)。
蛋白酶体抑制剂为基础的治疗方案
基于硼替佐米的治疗方案仍是骨髓瘤相关肾损害管理的基石(A级推荐)。硼替佐米应在3周/周期的第1、4、8和11天以1.3mg/m²的标准剂量开始给药(a级推荐),且应至少在治疗的第一个月给予大剂量地塞米松(B级推荐)。硼替佐米皮下给药的疗效与静脉给药相似(A级推荐)。硼替佐米为基础的三联治疗可能改善部分患者的肾脏结局,以确保疗效和毒性之间的最佳平衡(C级推荐)。卡非佐米在复发或难治性MM伴肾损害患者中安全有效(肌酐清除率≥15mL/min的患者中 A 级推荐;肌酐清除率<15mL/min的患者中 B 级推荐),且无需调整剂量。密切监测对于早期识别和及时管理卡非佐米相关肾脏并发症非常重要。对于肌酐清除率≥30mL/min的复发或难治性多发性骨髓瘤患者,伊沙佐米可以安全地与来那度胺和地塞米松联合给药(A级推荐);对于肌酐清除率低于30mL/min的患者,适用较低的起始剂量3mg(B级推荐)。
免疫调节剂为基础的治疗方案
沙利度胺对MM伴肾损害患者有效(B级推荐),应在不调整剂量的情况下给药(A级推荐)。来那度胺联合地塞米松对MM伴肾损害患者有效且安全(B级推荐)。来那度胺应根据肌酐清除率进行剂量调整(B级推荐);肌酐清除率低于 30mL/min 的患者,无论是否接受透析,每日最多可接受15mg(B级推荐)。泊马度胺联合地塞米松在复发或难治性MM伴肾损害患者中安全有效,包括接受透析的患者(肌酐清除率≥45mL/min的患者中为 A 级推荐;肌酐清除率<30mL/min为 B 级推荐)。
蛋白酶体抑制剂+免疫调节剂为基础的治疗方案
在肌酐清除率低于 50mL/min 的患者中,包括蛋白酶体抑制剂、免疫调节剂和类固醇的三药方案在一线和首次复发时均可改善肾脏完全缓解率和生存结局(B级推荐)。对于肌酐清除率为 30-59mL/min 的复发或难治性MM患者,与两药方案(例如硼替佐米-地塞米松和来那度胺-地塞米松)相比,三药方案(例如泊马度胺-硼替佐米-地塞米松和卡非佐米-来那度胺-地塞米松)可改善血液学和肾脏缓解率以及生存结局(B级推荐)。
单克隆抗体为基础的治疗方案
达雷妥尤单抗联合地塞米松治疗MM伴肾损害患者安全有效,包括接受透析的患者(B级推荐)。对于肌酐清除率≥40mL/min(达雷妥尤单抗-硼替佐米-美法仑-泼尼松和达雷妥尤单抗-硼替佐米-沙利度胺-地塞米松)或≥30 mL/min(达雷妥尤单抗-来那度胺-地塞米松)的新诊断MM患者,达雷妥尤单抗为基础的治疗方案安全有效(B级推荐)。在复发或难治性MM伴中/重度肾损害(蛋白酶体抑制剂:达雷妥尤单抗-硼替佐米-地塞米松、达雷妥尤单抗-卡非佐米-地塞米松和 isatuximab-卡非佐米-地塞米松)或中度肾损害(免疫调节剂:达雷妥尤单抗-来那度胺-地塞米松,达雷妥尤单抗-泊马度胺-地塞米松和 isatuximab-泊马度胺-地塞米松)患者中,CD38单抗为基础的三药方案安全有效(B级推荐)。Elotuzumab–来那度胺–地塞米松在复发或难治性MM伴肾损害患者中耐受良好且有效(C级推荐)。
自体HSCT
在硼替佐米和达雷妥尤单抗为基础的诱导治疗方案时代,移植的相关死亡率与无肾损害患者相似。自体 HSCT 可能改善高达1/3的患者的肾功能,超过1/4的患者摆脱透析。新药诱导和随后的自体 HSCT 可克服诊断时肾损害的不良预后效应。
大剂量美法仑序贯自体 HSCT 在适合移植的新诊断MM稳定肾损害患者中安全有效(B级推荐)。美法仑可根据肾损害的严重程度降低(100 mg/m²或140 mg/m²)或全剂量 (200 mg/m²)给药(C级推荐)。
抗体药物偶联物
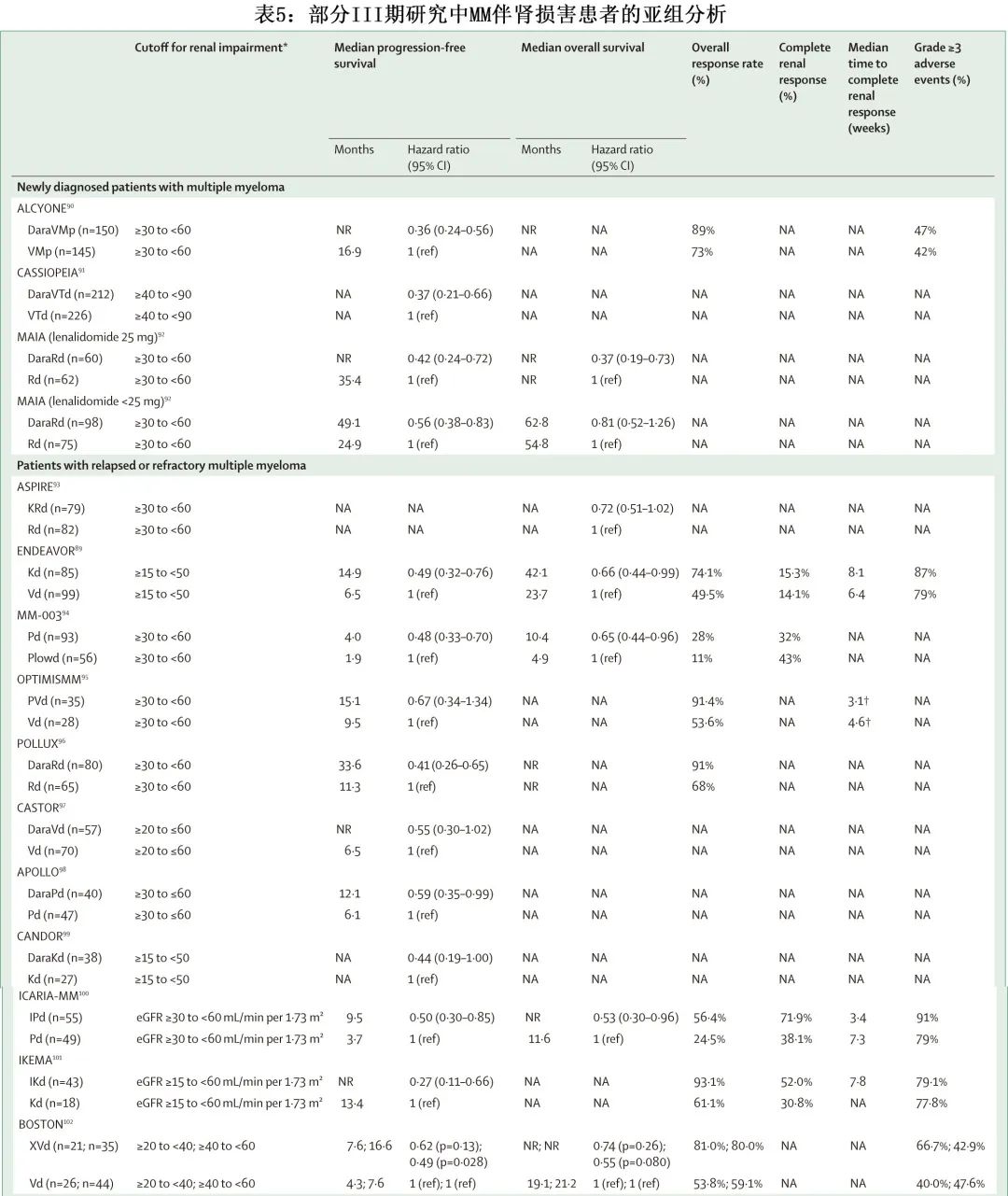
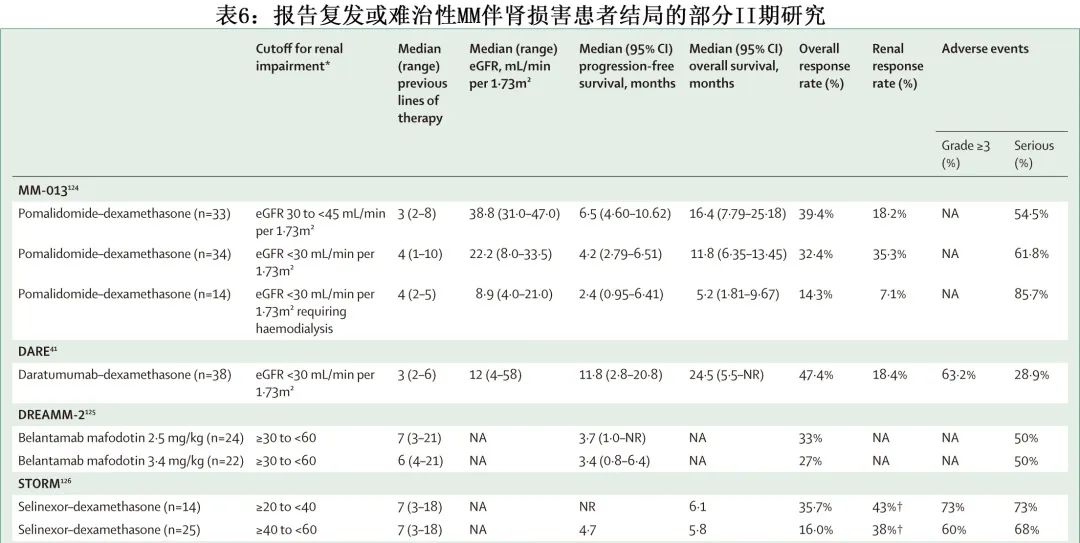
Belantamab mafodotin 是一种靶向 B 细胞成熟抗原 (BCMA) 的抗体偶联药物,在暴露于蛋白酶体抑制剂、免疫调节药物和抗 CD38 单克隆抗体后,对三类难治性患者具有抗骨髓瘤活性。DREAMM-2 研究的事后分析显示,根据肾功能,不同患者组间 belantamab mafodotin 的总缓解率、无进展生存期和毒性相似 (eGFR 90mL/min/1.73m² vs 60-89 mL/min/1.73m² vs 30-59 mL/min/1.73m²)。
XPO1抑制剂
塞利尼索是一种XPO1抑制剂,用于复发或难治性多发性骨髓瘤患者,口服给药。IIb 期 STORM 研究的事后分析显示,在既往多线治疗(五药难治)的复发或难治性MM患者中,无论基线肾功能如何(肌酐清除率为 20 mL/min至<40mL/min、40mL/min至<60 mL/min和≥60mL/min),塞利尼索–地塞米松的总缓解率相似;而高达67%的患者肌酐清除率明显增加。III 期 BOSTON 研究的亚组分析显示,与硼替佐米-地塞米松相比,塞利尼索-硼替佐米-地塞米松可显著改善复发或难治性MM伴不同肾功能水平(肌酐清除率 20mL/min至<40mL/min、40mL/min至<60mL/min、和≥60 mL/min)的总体缓解率。
CAR T细胞疗法
靶向骨髓瘤细胞表面 BCMA 的CAR T 细胞已被批准用于复发或难治性MM,其在既往至少4线治疗后可显著改善三类难治患者的结局。idecabtagene vicleucel (KarMMA) 和 ciltacabtagene autoleucel (CARTITUDE-1) 的注册研究纳入了肾功能良好且肌酐清除率≥45mL/min和≥40mL/min的患者,这主要是由于使用氟达拉滨清淋。对2项不同抗 BCMA CAR T 细胞治疗的 I 期研究的汇总数据进行事后分析,结果显示肾功能不全 (eGFR 30-89 mL/min/1.73m²) 患者的 eGFR 得到改善,但与肾功能正常患者相比,其预后更差。另一报告包括7例复发或难治性MM患者,eGFR为15-29 mL/min/1.73m²,显示总缓解率为100%,肾脏缓解率为100%。对于 eGFR 为30-70 mL/min/1.73 m²的患者,由于肾毒性风险,氟达拉滨应降低至24mg/m²。此外对于eGFR < 30 mL/min/1.73m²的患者,并无给药建议。
双特异性T细胞衔接抗体
双特异性 T 细胞衔接抗体是一种新的有前景的抗骨髓瘤免疫治疗,可在复发或难治性MM患者中产生深度和持久的缓解。Teclistamab 已获批用于复发性或难治性多发性骨髓瘤的治疗,而其他药物(例如 talquetamab[杨森公司,已在中国启动3期临床试验]或elranatamab)则接近获批。目前所有报告的研究均为肌酐清除率高于 40mL/min 且无显著肾毒性的患者,但在中/重度肾损害患者中进行的研究是非常值得期待的。
总的来说,Belantamab mafodotin 在复发或难治性MM伴中度肾损害患者中耐受良好且有效(C级推荐)。复发或难治性MM伴中/重度肾损害患者对塞利尼索为基础的治疗方案耐受良好且有效(C级推荐)。此外还需要更多的研究来确定 CAR T 细胞和双特异性 T 细胞接合器在MM伴中重度肾损害患者中的安全性。Ciltacabtagene autoleucel 和 idecabtagene vicleucel 在肌酐清除率分别≥40mL/min 和 45mL/min 的患者中似乎是安全的,而 teclistamab 在肌酐清除率高于 40 mL/min 的患者中耐受性良好(C级推荐)。
肾移植
在转诊中心,对于适合接受肾移植的终末期肾损害和持续骨髓瘤控制(即MRD阴性2年)的患者,可以考虑进行肾移植(D级推荐)。
参考文献
Dimopoulos MA,et al. Management of multiple myeloma-related renal impairment: recommendations from the International Myeloma Working Group.Lancet Oncol . 2023 Jul;24(7):e293-e311. doi: 10.1016/S1470-2045(23)00223-1.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













