AJH:B 细胞淋巴瘤患者的异源 SARS-CoV-2 疫苗接种
2021-11-26 MedSci原创 MedSci原创
SARS-CoV-2疫苗由于对免疫功能良好的患者疗效显著而被广泛分发。不幸的是,越来越多的文献表明淋巴瘤患者的疗效下降,特别是那些接受b细胞定向治疗的患者,提出了第一个评估异源mRNA/载体/mRNA
SARS-CoV-2疫苗由于对免疫功能良好的患者疗效显著而被广泛分发。不幸的是,越来越多的文献表明淋巴瘤患者的疗效下降,特别是那些接受b细胞定向治疗的患者。鉴于高发病率和死亡率,改进疫苗战略是一个需求未得到满足的关键领域。虽然美国疾病控制和预防中心(CDC)目前建议为免疫功能低下的患者接种第三种mRNA疫苗,但人们对替代方案有相当大的兴趣。
由于担心血栓性不良事件和全球供应限制,一些国家采用了异源疫苗接种策略。欧洲和最近的美国的研究人员已经证明,在健康个体中,病毒载体/mRNA疫苗组合的抗体水平显著增加。然而,对有体液和细胞免疫有缺陷的患者接种异源疫苗的数据有限。在这里,国外一研究团队进行了一项实验。

作为华盛顿大学/弗雷德·哈钦森癌症研究中心进行的一项irb批准的试验的一部分,7例低级别b细胞淋巴瘤患者最初接受了两剂量mRNA疫苗接种,随后获得了强生病毒载体疫苗。根据罗氏Elecsys抗sars-CoV-2S的评估,患者对最初的两剂量mRNA系列缺乏足够的刺突抗体反应,独立寻找异源疫苗接种,这是一种针对刺突蛋白受体结合域的半定量总抗体检测方法。
中位年龄为62岁(范围为41-79岁)。4人是男性,3人是女性。淋巴瘤亚型包括沃尔登斯特罗姆巨球蛋白血症(WM,n=3)、滤泡性淋巴瘤(FL,n=3)和慢性淋巴细胞白血病(CLL,n=1)。罗氏mRNAsys抗SARS-CoV-2S检测完成后,中位峰值抗体水平为<0.4AU/mL(范围<0.4-0.6AU/mL);阴性结果的参考间隔为<0.8AU/mL。第二次注射mRNA疫苗与强生疫苗之间的中位时间为97天(范围为70-173天)。
患者在接受强生疫苗后进行了一次血液样本采集。从强生到收集的中位时间为38天。中位IgG、绝对淋巴细胞计数和正常CD19+b细胞计数分别为597mg/dL、0.97x103/mL和0.6个细胞/mL。所有患者的核衣壳抗体均无反应,表明没有既往感染SARS-CoV-2的证据。使用相同的罗氏检测方法进行半定量抗棘突结合抗体评估,3例患者仍未检测到(<0.4AU/mL),2例患者有适度但阳性的反应(2.6和5.3AU/mL),2例患者经历了更大的血清转化(118和207AU/mL)。(图1)。WM患者接受扎努布替尼患者,CLL患者接受伊布替尼患者,1例利妥昔单抗单药治疗8个月后FL患者,1例伊布替尼+静脉替拉治疗3个月后出现阳性反应。2例接受扎努布鲁替尼治疗的WM患者和1例5个月前完成奥布妥珠单抗和苯达莫司汀治疗的FL患者对J&J缺乏反应。
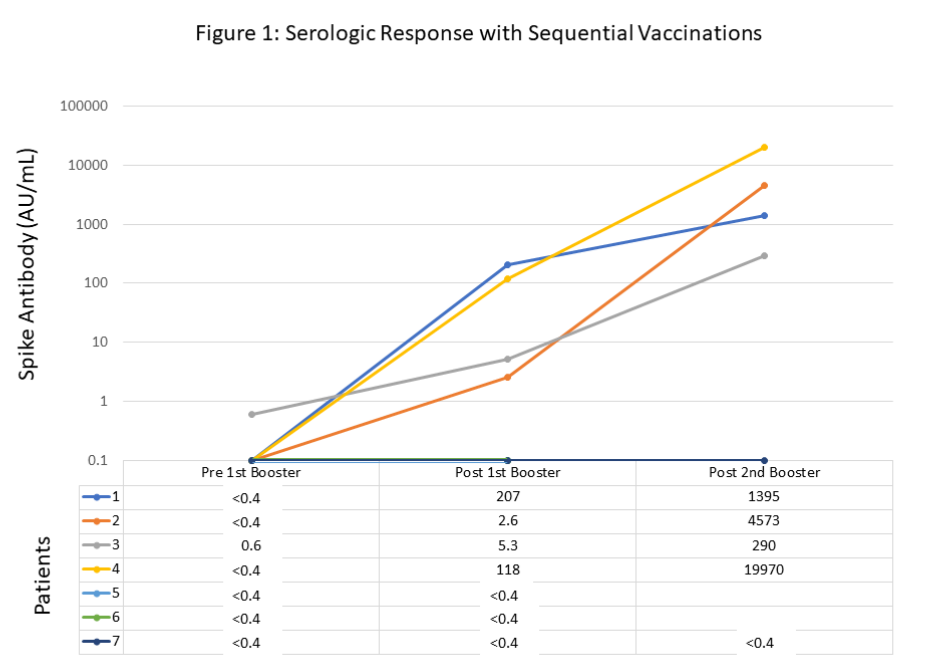
在美国疾病控制与预防中心建议为免疫缺陷患者接种第三种mRNA疫苗后,7名患者中有5名获得了第三种mRNA疫苗和第四种整体SARS-CoV-2疫苗。在这一亚组中,4例有强生的血清转化,1例没有。患者在第四种疫苗接种后平均16天进行了第二次样本收集。4例最初经J&J患者血清转化的患者抗体水平进一步升高。一名未经强血清转化的患者仍未检测到。无一例患者报告有明显的不良事件。
越来越明显的是,SARS-CoV-2疫苗对许多淋巴样恶性肿瘤患者无效,因为它们的先天免疫功能障碍和/或接受了b细胞定向治疗。鉴于并发症风险的增加和大流行病的延长,必须集中努力预测这些人是谁,以及了解其免疫反应的复杂性或缺乏其复杂性。
在这里,研究团队提出了第一个评估异源mRNA/载体/mRNA疫苗接种策略在淋巴瘤患者中的使用的病例系列。仅通过血清学评估,在2剂量mRNA系列后使用病毒载体疫苗就可以成功地诱导应答。结果反映了LLS最近的一份报告,其中在mRNA疫苗接种后,17个血清中有9个转化为J&J;使用相同的罗氏检测,产生的抗体水平在2.3到157AU/mL之间。3例在强生之前血清呈阳性(>2500AU/mL)的反应更强。有趣的是,他们还发现增加第四个剂量可以进一步增加血清学反应
这些发现对于难以理解如何在其环境中存在的脆弱患者很有希望。然而,从这个小队列中不可能确定这一策略将受益。由于缺乏数据,他们通过移植文献来深入了解其他疫苗诱导的免疫变化,认识到免疫抑制机制的差异,即钙调神经磷酸酶抑制剂和抗代谢物。在德国一项针对实体器官受者的研究中,研究人员发现,载体/mRNA疫苗计划导致刺突抗体水平、中和抗体活性和sars-cov-2反应性CD4t细胞的统计学上显著增加,以及CD8t细胞数量增加的趋势。不幸的是,目前分析范围不允许评估细胞免疫反应。
根据这些发现,同时也有新问题的挑战。在同源mRNA疫苗接种失败后,哪些免疫变化使病毒载体/mRNA方法有效?血清学反应的改善是否与实际的临床获益相关?在采用同源方法之前,应该考虑哪一种异源方法?是否有一种疫苗更好地用于启动?这取决于患者的临床特征?最后,我们如何改善一个经常被排除在疫苗试验之外的患者群体的结果?
原始出处:
Ujjani, C., Greninger, A.L., Shadman, M., Hill, J.A., Lynch, R.C., Warren, E.H. and Gopal, A.K. (2021), Heterologous SARS-CoV-2 Vaccinations in Patients with B-cell Lymphoid Malignancies. Am J Hematol. Accepted Author Manuscript. https://doi.org/10.1002/ajh.26418
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#细胞淋巴瘤#
128
#SARS-CoV#
75
#疫苗接种#
66
#SARS#
76