Am J Hematol:VRd或Dara四药方案可改善原发浆细胞白血病的生存
2023-03-10 聊聊血液 网络 发表于上海
回顾性多中心研究评估了未经选择的pPCL人群(包括根据新标准诊断的患者),发现现代抗骨髓瘤治疗(如VRd和达雷妥尤单抗四联方案)安全有效,缓解率高且持久。
原发性浆细胞白血病 (pPCL) 是一种罕见的浆细胞疾病,具有侵袭性的临床病程和较差的结局,占所有PCL的60-70%。PCL的原始诊断标准于1974年由Kyle等提出:循环浆细胞 (cPC) ≥20%且外周血浆细胞绝对计数≥2 × 109/L。2013年国际骨髓瘤工作组 (IMWG) 简化了原始标准,即其中一项足以诊断pPCL。基于最新的研究,2021年IMWG修订了 pPCL 的诊断标准,将cPC≥5%确定为新的临界值。
在自体干细胞移植 (ASCT) 和第一代新型药物,即沙利度胺、来那度胺和硼替佐米可用之前,接受常规化疗的 pPCL 患者的OS不足6个月。在新型药物时代,含硼替佐米的治疗后 ASCT 可改善缓解率并显著延长PFS和OS,但与 MM 相比pPCL的结局仍然较差
目前硼替佐米-来那度胺三联方案 (VRd) 或达雷妥尤单抗为基础的四联方案(daratumumab-based quadruplets ,DBQ) 已纳入 MM 的治疗中,但这些联合方案对 pPCL 患者的疗效数据仍然非常有限,因为pPCL经常被排除在临床试验之外。
考虑到缺乏前瞻性研究和疾病的罕见性,希腊学者开展了一项大型回顾性研究,纳入110例符合新IMWG标准的pPCL 患者(37%的患者cPC为5-19%)并对比不同治疗方案(VRD/DBQ对比含硼替佐米标准治疗/常规化疗)的疗效,以及评估OS的预后因素。研究结果近日发表于《American Journal of Hematology》。


作者回顾性审查了2001年至2021年间在希腊骨髓瘤研究组 (GMSG) 数据库登记的3324例 MM 患者中110例(3%)连续 pPCL 患者的数据。根据新的 IMWG pPCL 诊断标准,原发性 PCL 定义为外周血cPC≥5%。
新型抗骨髓瘤治疗包括:a)达雷妥尤单抗四联治疗 (DBQ),即达雷妥尤单抗联合免疫调节剂 (IMiD,来那度胺或沙利度胺)和地塞米松 (DaraVRd、DaraVDT),或达雷妥尤单抗联合环磷酰胺或蒽环类药物和地塞米松 (DaraVCD、DaraPAD),和b)硼替佐米-来那度胺-地塞米松 (VRd)。
硼替佐米标准联合治疗 (BSC) 包括硼替佐米和地塞米松联合环磷酰胺 (VCd)、沙利度胺 (VDT) 或蒽环类药物 (PAD);VDT联合化疗也视为BSC。常规化疗 (CT) 主要包括长春新碱-多柔比星-地塞米松 (VAD) 或美法仑-泼尼松 (MP) 联合化疗。
作者对比了VRd/DBQ和BSC/CT。

患者特征
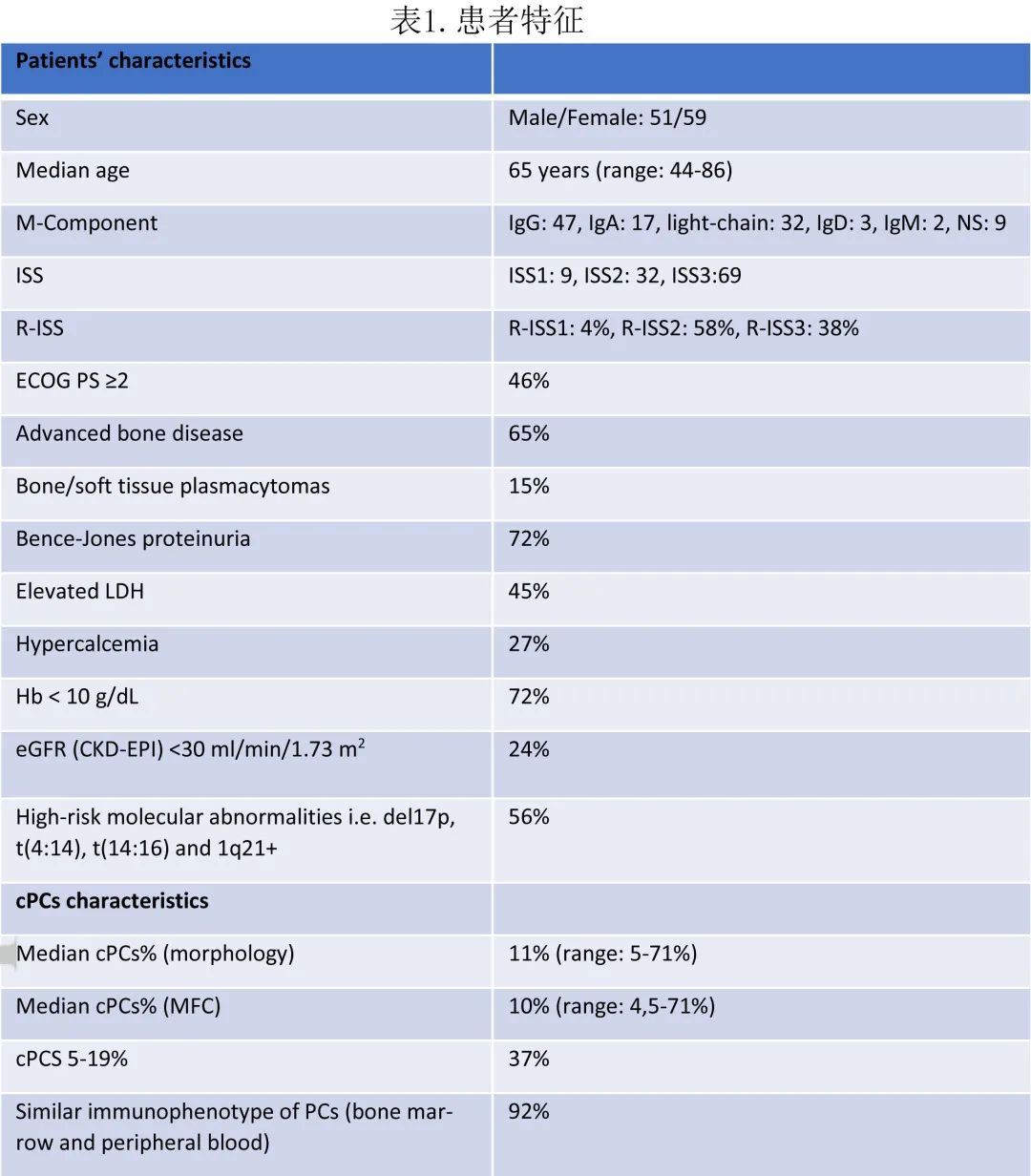
在2001-2021年 GMSG 数据库登记的3324例患者中有110例 (3%) 符合 pPCL 标准,其中41例 (37%)是根据新标准确诊。中位年龄为65岁,男女比例为51:59。69例 (63%) 患者为晚期疾病 (ISS 3);38%的患者为RISS 3;65%的患者患有晚期骨病,15%患有骨/软组织浆细胞瘤。FISH 检测的高危分子学异常即del17p、t(4;14)、t(14;16) 和1q21+ 总体检出率为56%(表1)。具体的分子学异常分布如下:del17p为16%,t(4;14)为9%,t(14;16)为5%,1q21gain或amplification为16%;t(11;14)为30%。常规核型方面,27%的患者为复杂核型,8%为亚二倍体,1%为超二倍体,67%核型正常。总体患者中85%和的 cPC在5-19%之间的患者中90%可获得多参数流式细胞术 (MFC),通过形态学估计的中位 cPC% 与 MFC 结果一致。92%的患者中骨髓和外周血PC免疫表型相似;CD56(-) 和CD27(+) cPC分别占52%和35%。(表1);除cPC≥20%的患者血小板 (PLT) 显著降低外,其他患者特征与cPC无关联。
治疗和反应
89/110例患者 (89%) 在一线治疗时接受硼替佐米为基础的标准方案或新型治疗;其中40例患者 (37%) 接受 DBQ 或VRd(DBQ:21%和VRd:16%)。诱导方案详见表2;35%接受了自体干细胞移植 (ASCT);2例患者进行了串联移植,1例患者接受了串联自体-异基因移植。

83%达到客观缓解 (≥PR);24%达到非常好的部分缓解 (VGPR),26%达到完全缓解 (CR)。中位至缓解时间为1个月。VRd/DBQ 或 ASCT 治疗与较高的 CR 率密切相关(分别为41% vs. 17%,p=0.008;52% vs. 11%,p<0.001)。43/110例患者 (39%) 接受了巩固和/或维持治疗,特别是15例患者 (14%) 接受了巩固治疗(DBQ组12例,KRd组1例,PVd组1例,硼替佐米组1例);41例患者 (37%) 接受了维持治疗(达雷妥尤单抗+/-来那度胺组13例,硼替佐米+来那度胺组10例,来那度胺组15例,伊沙佐米组2例,泊马度胺+地塞米松组1例)。但巩固和/或维持治疗与 OS 无显著相关性 (p>0.05)。
安全性
VRd/DBQ 治疗的患者中12%和接受 BSC/CT 治疗的患者中42%发生了3/4级中性粒细胞减少 (p=0.01);分别有6%和44%的患者发生贫血 (p=0.003);但两组间3/4级血小板减少没有差异。总体而言,接受 VRd/DBQ 治疗的患者中16%和接受 BSC/CT 治疗的患者中42%发生3/4级骨髓抑制(定义为至少一个细胞系的3/4级毒性)(P=0.03)。共19/110例患者 (17%) 发生中性粒细胞减少性感染,其中2例患者在感染发作期间死亡;6例患者发生肺炎,其中4例是由于 CMV 再激活;4例CMV肺炎中3例是接受 DBQ 治疗,1例患者接受 VCd 治疗;无患者死于 CMV 感染。分别有2例和3例患者发生3级肝毒性或神经毒性。此外仅在 BSC/CT 组 (12%) 观察到3/4级胃肠道毒性。
结局
中位随访51个月,共67例患者死亡(因进展:42例,因感染:20例,其他:5例),43例患者仍存活。4/110 (3.6%) 例患者发生早期死亡(≤1个月)。治疗线中位数为1,51例患者 (46%) 接受了二线治疗,42/51例患者 (82%) 在二线治疗中接受了新药联合治疗:9/51例 (17.5%) 接受了含达雷妥尤单抗方案,12/51例 (23.5%) 接受了含 PI方案,17/51例 (33.5%) 接受了含来那度胺方案,4/51例 (7.5%) 接受了含泊马度胺方案,9/51例 (18%) 患者接受 CT 作为二线治疗。pPCL 进展后的中位生存期为8个月。
整个研究人群的中位 PFS 为16个月,中位 OS 为29个月;其中VRd/DBQ治疗患者的 PFS 显著长于 BSC/CT 治疗患者(25个月 vs. 13个月;p=0.03)(图1),前者的中位 OS 也更长(未达到vs. 20个月;p<0.001;HR=0.28);VRd/DBQ组的3年 OS 分别为70%,BSC/CT组为32%(图2)。

作者还评估了cPC对预后的影响:与cPC≥20%的患者相比,cPCs 5-19%患者的中位 PFS 和 OS 显著延长(PFS:29个月vs. 12个月,p=0.004;OS:未达到 vs. 20个月;p=0.009)。
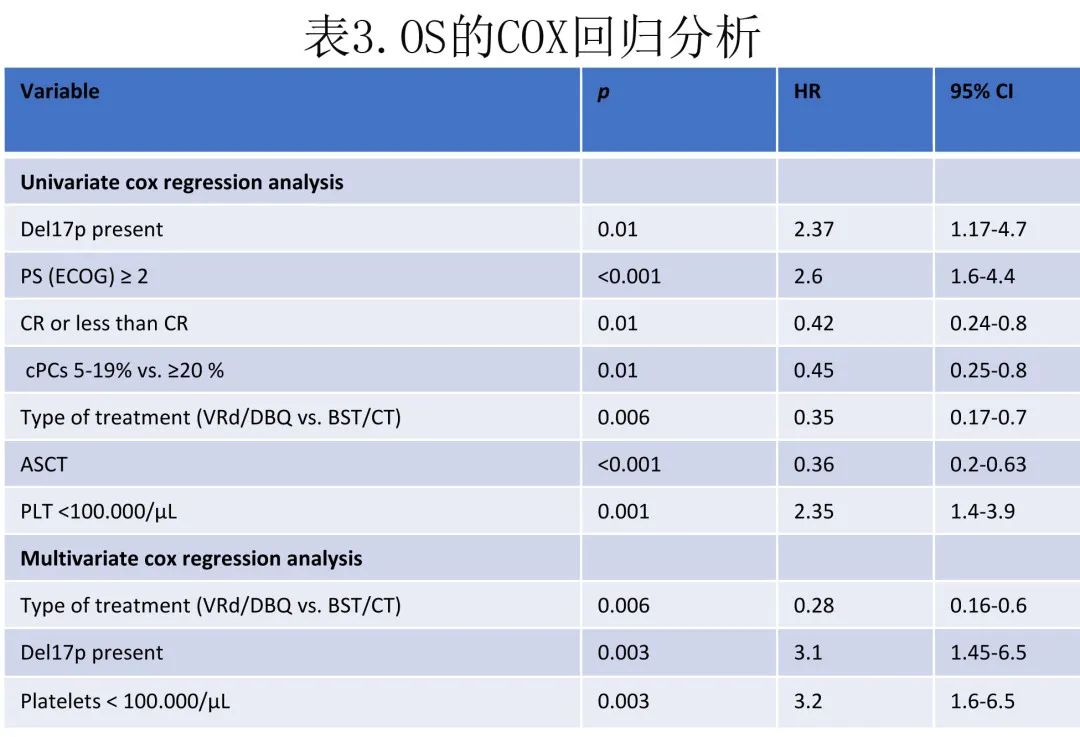
在单变量分析中,ECOG≥2、PLT <10万/μL、cPC≥20%和存在 del17p 是 OS 的负面独立预后因素。此外,VRd/DBQ一线治疗、ASCT和达到 CR 是 OS 的正面预测因素。del17p 患者和无del17p 患者的中位 OS 分别为17个月和48个月 (p=0.01;HR=3.1)。PLT <10万/μL vs.≥10万/μL患者的中位 OS 分别为16个月vs. 46个月(p=0.01;HR=3.2)。在多变量分析中,VRd/DBQ治疗、伴/不伴del17p和PLT计数<10万/μL是 OS 的唯一显著独立预后因素 (p<0.05)(表3)。

本项大型回顾性多中心研究评估了未经选择的pPCL人群(包括根据新标准诊断的患者),发现现代抗骨髓瘤治疗(如VRd和达雷妥尤单抗四联方案)安全有效,缓解率高且持久。并且上述组合证明是OS最强的预测因素,甚至超过了 ASCT 对预后的影响。这表明使用高效治疗方案的年轻和老年患者均可获益,无论是否适合ASCT。最后,重要的是认识到,诊断pPCL的cPC阈值下移至少会使患者数量翻倍,因此需要及时和有效的治疗pPCL。
参考文献
Eirini Katodritou,et al. Improved Survival of Patients with Primary Plasma Cell Leukemia with VRd or Daratumumab-based Quadruplets: A Multicenter Study by the Greek Myeloma Study Group.Am J Hematol . 2023 Mar 4. doi: 10.1002/ajh.26891.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言