Pemigatinib治疗FGFR2融合或重排的晚期胆管癌,CHMP持积极评价
2021-01-31 Allan MedSci原创
人用药品委员会(CHMP)对pemigatinib治疗无法切除的局部晚期或转移性胆管癌持积极意见,建议批准上市。
胆管癌是在胆管中形成的罕见癌症。根据其来源进行分类:肝内胆管癌(iCCA)发生在肝脏内部的胆管中,而肝外胆管癌发生在肝脏外部的胆管中。在欧洲,胆管癌的发病率在6,000-8,000之间。FGFR2融合或重排几乎仅发生在iCCA中,发生率约为10%至16%。
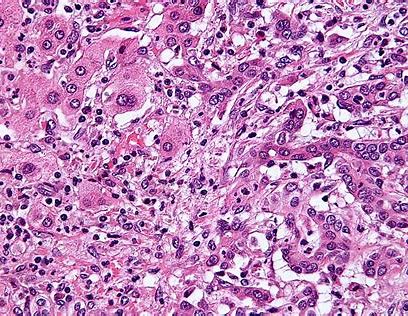
制药公司Incyte近日宣布,欧洲药品管理局(EMA)的人用药品委员会(CHMP)对pemigatinib治疗无法切除的局部晚期或转移性胆管癌持积极意见,建议批准上市。这些患者为成纤维细胞生长因子受体2(FGFR2)融合或重排的复发或难治型患者。
Incyte副总裁Peter Langmuir表示:“对患者而言,CHMP的积极意见是胆管癌的关键里程碑。继FDA批准pemigatinib(Pemazyre®)之后,我们很高兴能在欧洲提供首个针对这些患者的靶向疗法”。
CHMP的意见是基于FIGHT-202研究的数据,该研究评估了pemigatinib在先前已治疗、局部晚期或转移性胆管癌的成年患者中的安全性和有效性。如果获得批准,pemigatinib将成为欧盟第一个针对FGFR2融合或重排的、不可切除的局部晚期或转移性胆管癌患者的首个靶向治疗药物。
原始出处:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言



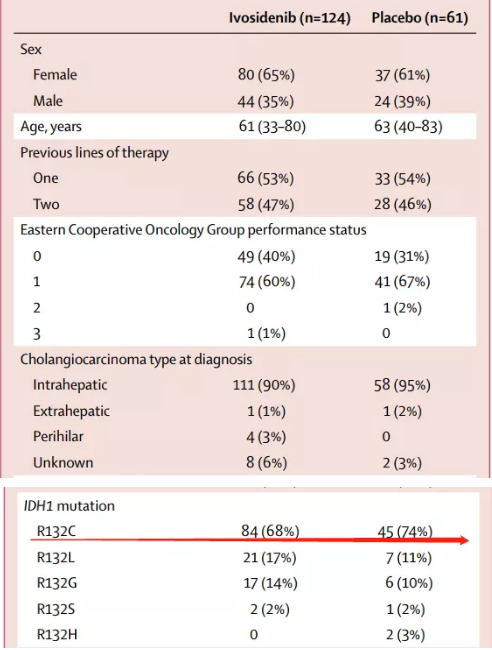
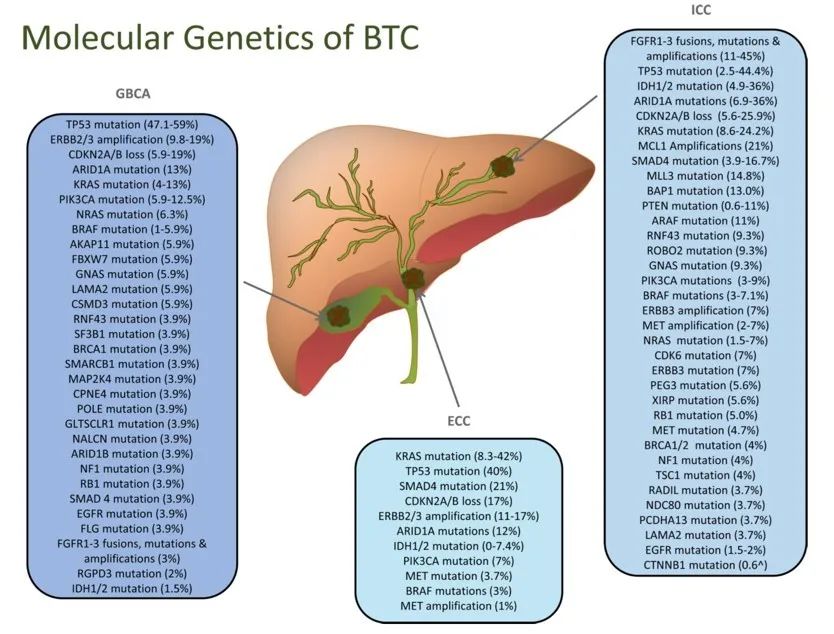











培米替尼针对FGFR2融合或突变的患者有良好疗效,FGFR2融合或重排几乎仅发生在iCCA中,发生率10-16%
72
#积极评价#
66
#PE#
55
#FGFR2#
78
#CHMP#
49
#pemigatinib#
77
#评价#
61
#FGFR#
56
#IgA#
50
#融合#
54