Nat Commun:两种关键酶或能双剑合璧促进癌症发生
2016-12-16 佚名 生物谷
图片来源:medicalxpress.com 日前,一项刊登于国际杂志Nature Communications上的研究报告中,来自德克萨斯大学的研究人员通过研究发现,此前彼此独立能够维持癌细胞活性的关键酶类实际上能够互相协作来刺激肿瘤生长,文章中研究者对这两种酶类是否存在一定的关联进行了深入研究。 研究者Jung-Whan Kim表示,这两种分子名为NQO1和HIF-1a,在正常的生理学

图片来源:medicalxpress.com
日前,一项刊登于国际杂志Nature Communications上的研究报告中,来自德克萨斯大学的研究人员通过研究发现,此前彼此独立能够维持癌细胞活性的关键酶类实际上能够互相协作来刺激肿瘤生长,文章中研究者对这两种酶类是否存在一定的关联进行了深入研究。
研究者Jung-Whan Kim表示,这两种分子名为NQO1和HIF-1a,在正常的生理学状况下,NQO1能够保护机体免于自由基和环境毒物(比如烟草烟雾)诱发的促癌损伤,当机体中氧气水平较低时(缺氧),HIF-1a就能够帮助细胞存活,一旦氧气水平恢复HIF-1a就会降解。然而,在很多类型的肿瘤中,这两种酶类的水平会处于持续较高的水平,尤其是NQO1的高水平表达和乳腺癌、结肠癌等多种癌症患者的预后较差直接相关,然而研究者并不清楚该分子高水平表达的原因。
Kim说道,同其它类型的细胞一样,癌细胞需要氧气才能存活,但其生长的速度往往很快,因此细胞就会经常处于缺氧状态,所以癌细胞就会不断适应并且通过多种机制来克服这种低氧的环境,其中一种措施就是增加HIF-1a的表达,这种酶类就会向机体发送信号来制造更多血管从而滋养肿瘤,并且重新编程机体的细胞代谢来适应缺氧状态。
截止到目前为止研究者并不清楚NQO1和HIF-1a的关联,这项研究中研究者就进行了一系列实验来确定哪种蛋白能够同HIF-1a相互作用,让他们不可思议的是他们发现NQO1能够同HIF-1a结合形成一种复合体,通过结合HIF-1a后,NQO1就能够对HIF-1a固定来调节配偶体蛋白,进而抑制HIF-1a分子被机体降解,因此研究者就发现NQO1或许能够通过固定HIF-1a来增强机体肿瘤的生长。
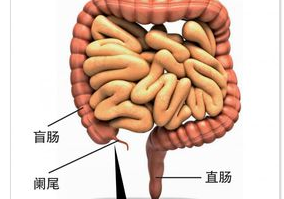
与此同时研究者还对结直肠癌细胞进行了研究,得出了和上述相同的结论,在接下来的实验中,研究者在结直肠癌细胞核乳腺癌细胞中检测了NQO1的水平,他们将修饰后的细胞注入到免疫力缺乏的小鼠机体中,随后他们发现小鼠机体中受抑制的免疫系统能够促进人类肿瘤的生长,在接受不含NQO1的癌细胞的小鼠机体中研究者发现肿瘤的水平会下降,研究者指出,通过降低依赖NQO1的HIF-1a分子的活性就能够特异性地抑制肿瘤的生长。
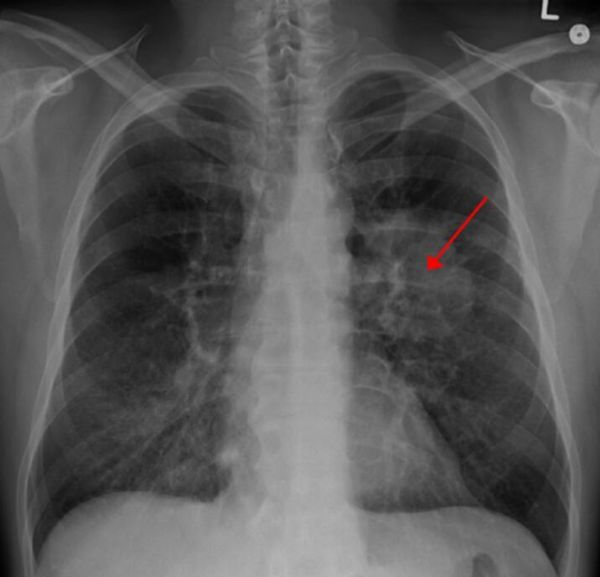
目前研究者正在通过研究调查HIF-1a在特殊类型肺癌中的角色,他们希望通过和其他科学家的联合研究来鉴别出靶向阻断癌细胞中HIF-1a酶的新型分子。尽管研究者们目前发现了一些潜在的候选分子,但他们还需要更为深入的研究,他们希望后期能够寻找到更多的抑制性分子。
原始出处
Eun-Taex Oh et al.NQO1 inhibits proteasome-mediated degradation of HIF-1α.Nat Commun.2016
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#COMMUN#
47
#Nat#
56
事业你学习了好东西
85