肿瘤干细胞之我见——专访钱程教授
2016-04-20 生物谷 梅斯医学
【独家】2016(第二届)肿瘤干细胞转化医学论坛肿瘤干细胞之我见—专访钱程教授 钱程 教授 医学博士,教授,博士生导师 第三军医大学西南医院生物治疗中心主任 长期从事肿瘤发病机理、肿瘤生物治疗和干细胞治疗肝病方面的研究,在肿瘤干细胞生物学、肿瘤侵袭转移、EMT诱导和肿瘤微环境等方面,开展深入的研究工作,已获得很好的研究成果。所获得的研究成果在国际著名的Journal of Clinic
【独家】2016(第二届)肿瘤干细胞转化医学论坛
肿瘤干细胞之我见—专访钱程教授

第三军医大学西南医院生物治疗中心主任 长期从事肿瘤发病机理、肿瘤生物治疗和干细胞治疗肝病方面的研究,在肿瘤干细胞生物学、肿瘤侵袭转移、EMT诱导和肿瘤微环境等方面,开展深入的研究工作,已获得很好的研究成果。所获得的研究成果在国际著名的Journal of Clinical Oncology、Gastroenterology、Hepatology等SCI期刊上发表论文140余篇,总影响因子700, 被Cell、Nature 系列杂志他引4000余次。获得PCT国际发明专利4项。其研究成果对探讨癌症的分子发病机制、肿瘤的生物治疗以及成体干细胞分子调控机制和临床应用具有重要意义。目前,其带领的研究团队,主要从事肿瘤生物治疗和成体干细胞的基础研究、转化医学研究和临床应用,已在国内获得的多项重大项目支持。
生物谷:肿瘤抗药是肿瘤治疗中的一大难题,肿瘤干细胞则可能是这一问题的罪魁祸首。从目前肿瘤干细胞的研究进展来看,我们是否有希望可以攻克这一难关,请为我们分析一下?
回答:随着这些年肿瘤发病率越来越高,传统的手术、放化疗在肿瘤治疗面前凸显出局限性,肿瘤干细胞的研究开始受到政府和研究者的极大关注。经过多年的研究,从证明肿瘤干细胞的存在,到区别于一般肿瘤细胞的特性研究、再到肿瘤干细胞与微环境间的相互作用,研究者对肿瘤干细胞有了更加全面的了解,也就越来越有希望调控及消灭它。比如最初为了了解抵抗放化疗、导致患者复发转移的这一小群细胞,研究者花了很多年去筛选获取这群细胞,应运而生了诸多的肿瘤干细胞的分子标记物即marker。随着研究的不断深入,研究者逐渐发现这群细胞存在异常表达的基因或异常活化的信号通路,这才是它抵抗药物治疗或获得耐药的根源。肿瘤是由许多癌基因和抑癌基因发生遗传学或表观遗传学改变所导致的恶性疾病,因此肿瘤干细胞的表型也是多变的。同时这种多变性还表现在它应对外界环境的能力,包括能够根据机体环境或微环境的变化,调整自身的增殖或定位,诱化周边正常组织。
从肿瘤干细胞目前的研究进展看,我们对肿瘤干细胞的本质和它们自身的调控机制已越来越多的了解,后续的事情就是我们从什么角度能够抑制或消灭它,我对此还是很有信心的,我相信通过选择性杀伤肿瘤干细胞,解决肿瘤抗药的一大难题,只是时间的问题。
生物谷:根据目前的相关研究来看,肿瘤干细胞的研究面临着哪些困难?
回答:肿瘤干细胞比例低是肿瘤干细胞研究的一大困难,无论是肿瘤干细胞的系统性研究或药物筛选鉴定都需要基于大量病人体内获得的肿瘤干细胞,而目前主要还是基于细胞系或病人来源的原代细胞,并不能有效的反映肿瘤患者体内的真实情况。肿瘤干细胞的多变性是肿瘤干细胞研究的另一大困难,从病人体内分离获取的少量肿瘤干细胞,缺失有效的体外培养方法,肿瘤干细胞在体外极易发生表型变化。同时肿瘤干细胞本身也处于幼稚或原始状态,环境的些许变化都会引起肿瘤干细胞分化,给进一步研究带来了极大困难。在此基础上的靶向肿瘤干细胞的药物筛选也存在困难。因此,有效的从病人肿瘤组织中获得肿瘤干细胞和建立肿瘤干细胞稳定的培养体系,是本领域需要解决的关键科学问题。
生物谷:和传统的肿瘤治疗方法相比,针对肿瘤干细胞的诊治具有哪些优势?
回答:传统的肿瘤治疗方法如手术治疗、放化疗可在一定程度上清除大多数肿瘤细胞。但在绝大多数情况下,仍可能存在少数肉眼不可见和(或)耐药的肿瘤病灶和细胞,导致肿瘤的耐药和复发,而在这中间,目前研究认为肿瘤干细胞扮演了关键的角色,成为上述过程的重要事件。只有从根源上消灭这群细胞才能有效的预防肿瘤的复发和转移,因此结合传统治疗和针对肿瘤干细胞的治疗能根除肿瘤。另外需要提到的是,针对肿瘤干细胞的治疗不仅仅是靶向和消灭肿瘤干细胞,肿瘤微环境在肿瘤干细胞的维持以及促使分化型肿瘤细胞逆分化为肿瘤干细胞中发挥重要的作用,所以阻断这个过程也是针对肿瘤干细胞研究的重要方向。
生物谷:近年来,基因测序、基因编辑等技术迅速发展,并随着精准医学的提出,受到广泛关注。您认为肿瘤干细胞的相关研究是否可以和精准医学的概念相结合?它们的结合将会给这一领域带来哪些方面的突破?
回答:精准医学是基于分子生物学、生物信息学以及基因测序技术的发展,结合大数据的分析,实现精准的疾病分类及诊断,制定个性化的疾病预防和治疗方案。在肿瘤治疗中,针对肿瘤干细胞的诊治与精准医学的核心理念是一致的。将肿瘤干细胞的相关研究和精准医学的概念相结合,可以为针对肿瘤干细胞的治疗带来一些新的突破:
1、基于单细胞多组学测序技术/高通量深度测序技术,可利用肿瘤患者极少的细胞就能获得大量的有效数据,为全面、系统的研究肿瘤干细胞的分子分型,耐药机制和个性化治疗提供依据。此外,我们可利用该技术对靶向肿瘤干细胞的小分子化合物、单克隆抗体和免疫治疗等进行快速、高效的筛选和验证,并实现对疾病的精准分型、个性化用药、预后的评估及后续治疗方案的优化。
2、基因编辑新工具的出现,可以使研究者能够方便而精准的对DNA核苷酸序列进行编辑。在癌症中有许多癌基因和抑癌基因发生了遗传学和表观遗传学改变。其中,在由于癌基因或抑癌基因突变累积导致的肿瘤中,我们可以通过基因编辑的手段如CRISPR-Cas9等对肿瘤患者的突变基因进行精确修复。利用基因编辑技术快速模拟肿瘤的遗传学事件、建立相关的肿瘤模型并实现肿瘤基因组编辑等等,进而将基因编辑技术应用到肿瘤干细胞的基础研究、转化医学和临床治疗等不同方面,为肿瘤患者带来新的治疗契机。
生物谷:目前是否有肿瘤干细胞应用于临床的案例?您认为肿瘤干细胞将来在临床应用方面的前景如何?
回答:目前有肿瘤干细胞应用于临床的案例,但仅限于临床试验阶段,对于临床应用的广泛推广可能还有一段路要走。例如:新型ABC转运泵的抑制剂MS-209、VX-710和tariquidar可抑制P-gp和MRP1。最新临床试验显示MS-209在征服乳腺癌和其他实体瘤耐药方面是很有前景的,临床批号:NCT00004886。Tariquidar是另一个很鼓舞人心的抑制剂,联合tariquidar和docetaxel(多西他赛)用于治疗转移性或复发性卵巢癌、宫颈癌、肺癌和肾癌等恶性肿瘤,临床批号NCT00072202。同样,联合tariquidar和Dox、依托泊苷(etoposide)、米托坦(mitotane)和长春新碱(vincristine)正在进行原发性、复发性和转移性肾上腺皮质恶性肿瘤患者的临床试验,临床批号:NCT00073996。
肿瘤干细胞将来在临床应用方面的前景:
1、鉴定肿瘤干细胞标志物将是限制其临床应用的重要方向,找到针对多种肿瘤干细胞的标志物及其与正常干细胞基因表达的差异,才能对症下药,确定肿瘤治疗新靶点;
2、阐明正常干细胞生理和肿瘤干细胞病理生理功能的分子调控途径以及导致肿瘤干细胞形成的分子机制,选择与肿瘤干细胞自我更新相关的信号传导通路予以特异性阻断,将是未来治疗恶性肿瘤的重要方向之一;
3、研究肿瘤细胞群体的异质性并针对肿瘤干细胞的特性设计综合性的治疗方案;
此外,通过设法改变肿瘤微环境,诱导肿瘤干细胞分化也是靶向肿瘤干细胞的治疗策略之一。
目前,在肿瘤的治疗过程中,以小分子抑制剂、单克隆抗体和融合蛋白为主的其它各种靶向肿瘤干细胞的药物也在逐步开发并进行临床试验,另外靶向肿瘤干细胞的免疫细胞治疗也是将来重要的发展方向。总之,以肿瘤干细胞为靶点的抗肿瘤治疗策略,将为彻底治愈癌症带来新的希望。
最新嘉宾摘要

钱程 教授
医学博士,教授,博士生导师
第三军医大学西南医院生物治疗中心主任
演讲题目:靶向肿瘤干细胞治疗癌症的新策略
演讲摘要:肿瘤干细胞是一群具有自我更新、多向分化潜能、具有启动和重建肿瘤组织表型能力的肿瘤细胞。前期研究均表明,肿瘤干细胞参与肿瘤的转移、复发和对化疗和放疗耐受。因此,靶向肿瘤干细胞的治疗策略将有望为癌症的治疗带来希望。我们课题组成功的从肝癌组织中,分离出多能转录因子Nanog高表达的新型肝癌干细胞。证实Nanog阳性的肿瘤细胞具有更强的自我更新、克隆形成和肿瘤起始能力。他们参与肿瘤的复发和对化疗药物的耐受。进一步研究发现,Nanog不仅可作为肿瘤干细胞的分子标志物,同时证明它可通过IGF信号通路参与肿瘤干细胞的自我更新。并且创新性发现Nanog与IGF信号通路存在正反馈调控机制。在这基础上,我们成功的建立以肿瘤干细胞为平台和Nanog为靶点的高内涵药物筛选平台,已筛选出多个靶向肿瘤干细胞的小分子化合物和特异性单克隆抗体。通过该项研究,我们发现HDAC抑制剂可诱导肿瘤干细胞的分化,导致肿瘤干细胞对化疗的敏感性,联合分子靶向药物Sorafenib成功的治疗肝癌。同时靶向肿瘤干细胞的CAR-T细胞也成为治疗癌症新策略。

高建新 教授
上海交通大学医学院仁济临床干细胞研究中心特聘教授
博士生导师、肿瘤发生与免疫研究室主任
演讲题目:肿瘤干细胞广谱、特异性抗原的鉴定、功能和免疫治疗应用前景
演讲摘要:广谱肿瘤特异性抗原是免疫治疗安全、高效的关键靶标。但是,目前肿瘤免疫治疗在这方面遇到了瓶颈。我们曾率先报道,生殖干细胞基因PIWIL2异化激活产物PL2L60广泛表达在各种血癌和实体癌瘤中,介导肿瘤发生发展。然而,它是否可以作为免疫治疗的一个广谱肿瘤特异性抗原尚不清楚。进一步研究表明,PIWIL2 / PL2L60蛋白 特异性单克隆抗体(克隆KAO3)几乎100% 抑制癌前干细胞在免疫缺陷小鼠(SCID)内的致瘤能力,也能有效地抑制多种人和小鼠肿瘤生长,包括淋巴瘤、乳腺癌、肺癌和宫颈癌等。对肿瘤的抑制能力与该肿瘤细胞表面表达KAO3特异性抗原有关。KAO3单抗抑制肿瘤生长的机制包括通过阻滞细胞周期在G2 / M阶段诱导肿瘤细胞凋亡或增殖,抑制DNA合成和激活补体杀伤肿瘤细胞。KAO3+人和小鼠肿瘤细胞的致瘤能力显著高于KAO3- 肿瘤细胞。基因PL2L60过表达导致KAO3+ 细胞增加,伴随着增加干性,增殖和迁移。用PL2L60多肽致敏树突状细胞可以诱导有效的抗肿瘤免疫效应。更重要的是,KAO3+ 细胞可以在不同类型的白血病患者外周血中检测到。因此,我们首次确定了人和鼠肿瘤干细胞表面表达PL2L60,具有广谱肿瘤特异性抗原的特征,可用于各种免疫治疗的新靶标。KAO3单抗具有作为新一代肿瘤免疫治疗药物的潜能。
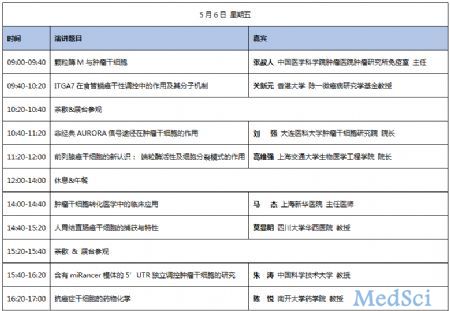
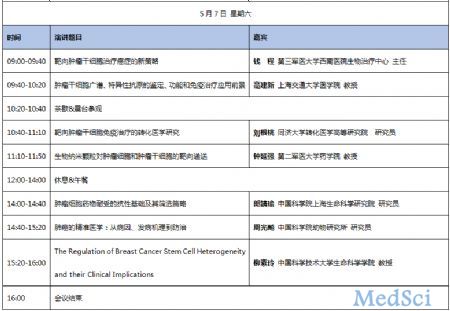
大会初步日程:
重要提示:优惠报名至4月20日截止!请各位代表提早办理注册付款,以享优惠!
会议地址:上海市徐汇区肇嘉浜路500号。
会议时间:2016年5月6日—7日
会议场馆:上海好望角大饭店(中科院上海学术活动中心)
参会咨询/媒体合作:
参会咨询:
徐鹏建
E-mail:pengjian.xu@bioon.com
Tel : 86(21)64879851ext 8109
Mob :139 1828 6340
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













学习
60
#专访#
28