Cell Death Dis:阻断EIF5A的hypusination作用可抑制结直肠癌细胞的生长
2020-12-27 MedSci原创 MedSci原创
结直肠癌(CRC)作为全球第三大致命的和第四大最常被诊断的癌症,其通常从良性腺瘤性息肉开始,发展为具有高度不典型性增生的晚期腺瘤,最终发展成为浸润性癌。在疾病的早期阶段,癌细胞被限制在结肠壁内,且该疾
结直肠癌(CRC)作为全球第三大致命的和第四大最常被诊断的癌症,其通常从良性腺瘤性息肉开始,发展为具有高度不典型性增生的晚期腺瘤,最终发展成为浸润性癌。在疾病的早期阶段,癌细胞被限制在结肠壁内,且该疾病可以通过手术切除的方式来治愈。
随着癌症的发展,癌细胞会通过结肠壁到达区域淋巴结,此时通过外科手术和辅助化疗的联合治疗,可以治愈约70%的CRC病例。当癌症到达晚期,癌细胞从原位转移到远端,导致患者的预后变差,目前的治疗方法的患者平均存活率仅为25-30个月。
尽管对于CRC相关分子机制已有一定的进展,但目前的治疗方案仅包括少数几种疗效有限的药物,患者的总体生存率仍不令人满意。因此,鉴定该疾病的潜在的治疗靶标尤为重要。
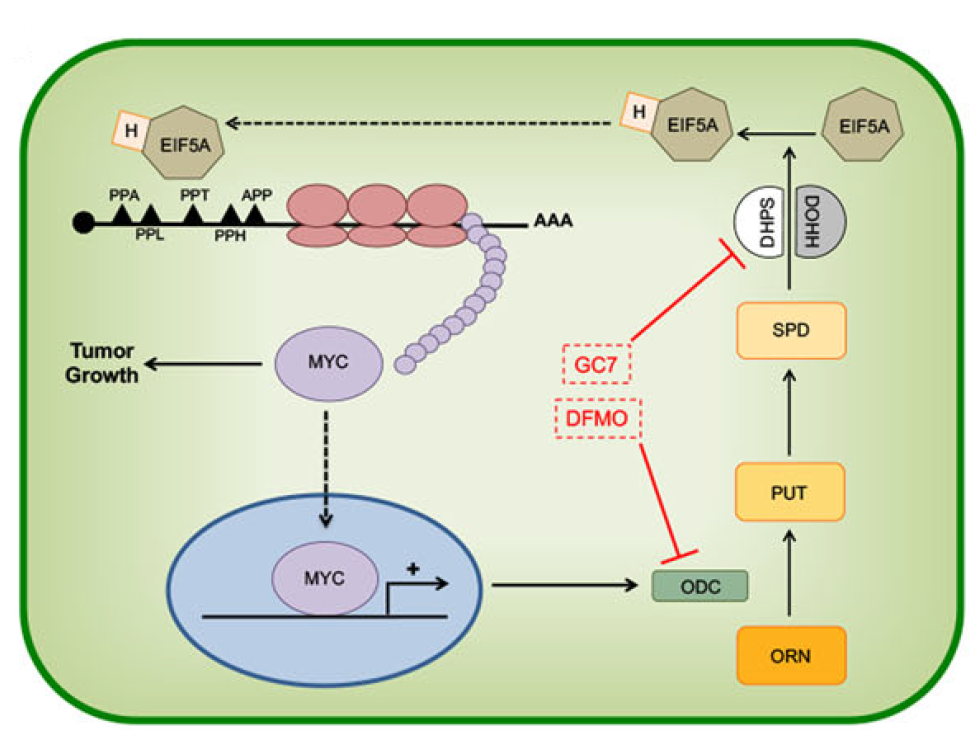
模式图
EIF5A是受hypusination(羟腐胺赖氨酸作用)调节的一种翻译起始因子,hyposination是DHPS和DOHH催化的由多胺精胺开始的一种独特的翻译后修饰。最新的研究数据表明,hypusinated化的EIF5A能够调节如自噬、衰老、多胺稳态、能量代谢等一系列关键的细胞进程,并在癌症中起作用。然而,目前在临床前癌症模型中抑制EIF5A的作用、相关分子机制以及特定的翻译靶标仍知之甚少。
研究结果显示,hypusinated化的EIF5A可通过直接调节特定暂停状态下的MYC的生物合成来促进CRC细胞的生长。通过DHPS抑制剂GC7、慢病毒介导的DHPS或EIF5A的敲低作用抑制EIF5A的hypusination作用,可以抑制CRC细胞的生长。
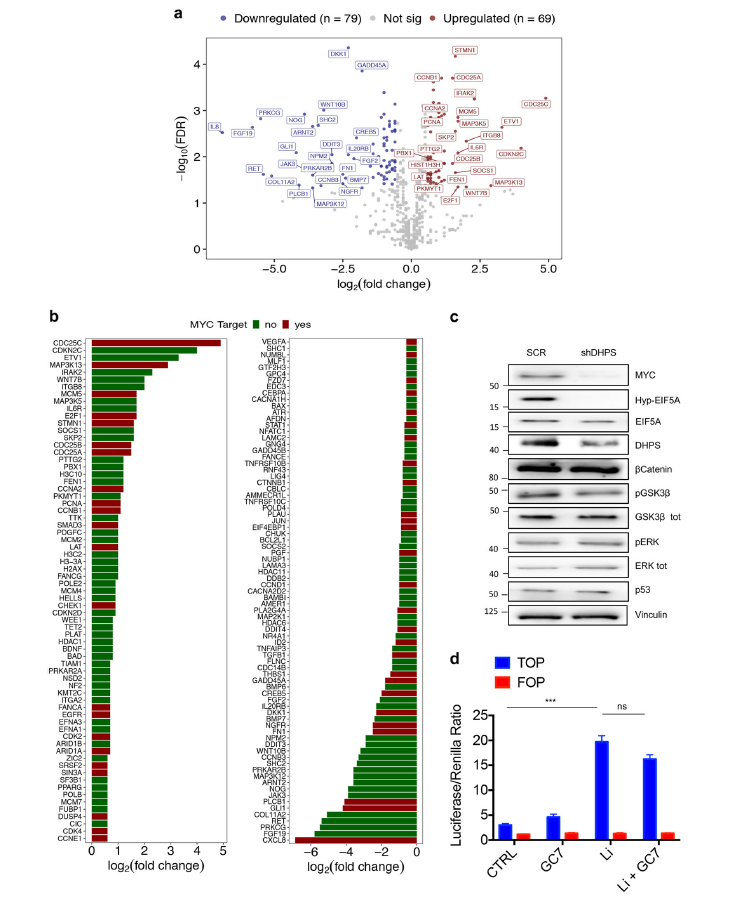
基因表达谱显示抑制DHPS可下调MYC的表达
多基因表达分析显示,对hypusination作用的抑制会损害MYC调控的转录本的表达。研究人员进一步证实,EIF5A调节MYC的合成主要是通过减轻MYC CDS中五个不同暂停基序的核糖体停滞作用,而不影响其mRNA的水平或蛋白质的稳定性。值得注意的是,研究人员发现,在CRC的临床前模型中,对hypusination作用的阻断能够引起显著的生长抑制作用,且能够显著减小家族性腺瘤性息肉病(FAP)APCMin/+小鼠模型中的息肉大小。
总而言之,以上的研究数据揭示了一种前所未有的分子机制,其中hypusinated化的EIF5A的促肿瘤特性与其调节MYC合成的能力相关。该研究结果也为DHPS/EIF5A抑制剂在CRC治疗中的使用提供了一定的理论依据。
原始出处:
Coni, S., Serrao, S.M., Yurtsever, Z.N. et al. Blockade of EIF5A hypusination limits colorectal cancer growth by inhibiting MYC elongation. Cell Death Dis 11, 1045 (10 December 2020).
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#结直肠癌细胞#
65
#CEL#
61
#Cell#
61
#阻断#
61
#Nat#
80
#Dis#
51
#癌细胞#
82
#结直肠#
55
#Death#
71