Nature子刊: 一种新型生物传感装置助力健康监测
2023-09-04 小桔灯网 小桔灯网 发表于上海
作者展示了一种基于PAAm水凝胶衬底的可拉伸晶体管阵列,其有效杨氏模量为5.2 kPa,比传统的器件软两到三个数量级,可以与动态软表面(如具有非零高斯纹理的皮肤)形成更舒适、稳定和不易察觉的接触。
将电子设备作为可穿戴或植入式设备与人体相连接,为健康监测、疾病治疗甚至基础生物学研究提供了大量功能。为了实现无缝和贴合的接口,必须尽量减少电子设备与人体皮肤/组织之间的机械不匹配,其中两个主要方面是柔性(即杨氏模量)和可拉伸性。虽然可拉伸性的实现通常伴随着杨氏模量的降低,但这些可拉伸电子材料和器件的模量仍然比大多数柔性生物组织高3-4个数量级。进一步减少这种模量不匹配对于实现长期稳定的生物界面是非常重要的。首先,机械方面,理论和实验都表明,组织级模量可以显著提高可拉伸装置在非零高斯表面(如人体皮肤或组织)上的贴合性。其次,免疫方面,生物植入物的组织柔软度可以显著抑制对可植入装置的异物反应(FBR) 。总的来说,一个贴合且无疤痕的组织界面对于和调节信号转导的保真度非常重要。
近日,一组来自芝加哥大学和UCLA的研究团队在杂志Nature Communications上发表了一篇题为“Achieving tissue-level softness on stretchable electronics through a generalizable soft interlayer design”的文章。在这项工作中,作者报告了一种可推广的柔性中间层设计,当将其添加到功能层和基底之间时,可以允许使用现有的可拉伸电子材料来构建组织级模量器件,同时实现高拉伸性。利用这种设计,作者展示了一种基于PAAm水凝胶衬底的可拉伸晶体管阵列,其有效杨氏模量为5.2 kPa,比传统的器件软两到三个数量级,可以与动态软表面(如具有非零高斯纹理的皮肤)形成更舒适、稳定和不易察觉的接触。

图片来源:Nature Communications
柔性中间层设计的工作机理
作者通过对由功能薄膜、柔性中间层和超软基底组成的三层结构进行有限元分析(FEA),从理论上研究了中间层的力学功能。在功能膜中引入一个切口,并绘制缺口周围的应力水平图(图a)。结果显示,切口周围的模量越高、夹层厚度越大、分层程度越轻(即粘连性越好),都可以抑制功能层的应力集中(图b-d)。
研究团队通过实验验证了SEBS H1052 (2.83 MPa)可以作为理想的中间层,与超低模量基材(例如水凝胶)具有强粘附性。采用这种中间层设计,即使只有200 nm厚的SEBS中间层,100%应变下半导体薄膜中的拉伸裂纹尺寸和密度明显减小,进一步将SEBS层增加到2 μm有助于实现更少的裂纹扩展(图f)。半导体薄膜的载流子迁移率的变化趋势(图h)也反映了这种SEBS中间层显著提高的拉伸性。
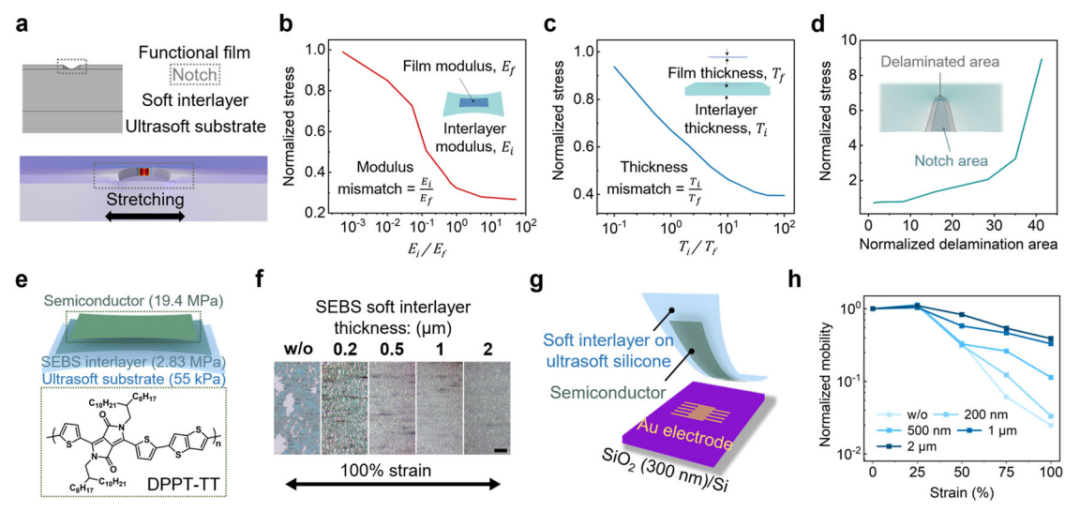
柔性中间层显著提高功能层可拉伸性。
图片来源:Nature Communications
采用柔性中间层设计的超软晶体管
作者尝试使用柔性中间层设计在可拉伸晶体管上实现类似组织的柔软性。采用PAAm水凝胶(200μm,模量2.58 kPa)作为基底,以及SEBS作为柔性中间层,得到的晶体管厚度为200μm,杨氏模量低至14.4 kPa。两个方向的100%应变下,即使重复拉伸1000次,柔性中间层的高拉伸性也能确保稳定的载流子迁移率(图c,d)。
通过在SEBS软中间层上预先设计空间图案有助于有源矩阵实现更低模量,可低至5.2 kPa模量(图g),比之前报道的传统弹性体基底(厚度为100 μm)上的可拉伸晶体管阵列软两到三个数量级,同时保持了相似的可拉伸性。

超软可拉伸晶体管和有源矩阵电路采用柔性中间层设计。图片来源:Nature Communications
超软器件增强了贴合性并减少了机械约束
组织级柔软度的实现可以极大地提高附着在动态皮肤/组织表面上的电子设备信号转导质量的同时,降低不适感。贴合性的改善在非零高斯曲面上得到了证明,如图c, d所示的人类手腕表面。超软设备在皮肤变形下可以更好地遵循原始皮肤表面纹理,这意味着更低的不适感和更好的贴合性。
此外,低杨氏模量的装置最大限度地减少了对柔软皮肤和组织运动的机械约束。低机械约束的好处在包裹变形软组织的情况下更为明显,例如周期性膨胀的血管(图f)。与传统器件(图g右)所看到的明显约束相比,当被超软晶体管阵列包裹时,血管可以更好地保持其原始膨胀程度(图g中)。
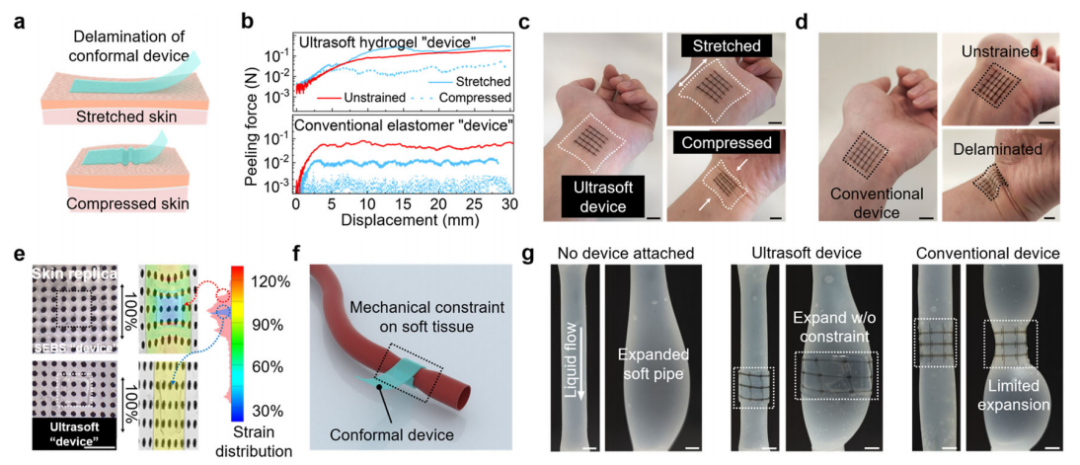
超软器件增强了贴合性并减少了机械约束。
图片来源:Nature Communications
超软器件的生物相容性表征
对于植入式应用的生物相容性,作者比较了三种类型样品上的FBR:水凝胶膜、SEBS膜和SEBS-水凝胶双层样品。这些样品被植入小鼠皮下1个月,以分析组织反应。如图d所示,双层植入体的瘢痕组织(18.3μm)比SEBS植入体(51μm)薄,与水凝胶植入体(15.4μm)相似。结果表明,长期的免疫相容性确实可以从植入物模量的降低中获益。
研究团队进一步将中间层设计应用于超软可拉伸电生理(EP)记录设备(图e)。该设备的超低模量表现出两个主要优点。首先,该设备与心脏表面保持相对稳定的附着,由于心脏跳动而产生的位置移动最小(图f-top),这对于在心脏表面进行长期空间分辨率的ECG记录/映射非常重要(记录的ECG信号如图g-top)。其次,超软装置对心脏跳动的机械约束较低,LVP稳定且增幅最小(图h)。这种益处对于使用慢性集成设备进行微创和稳定的心脏测绘是很重要的。
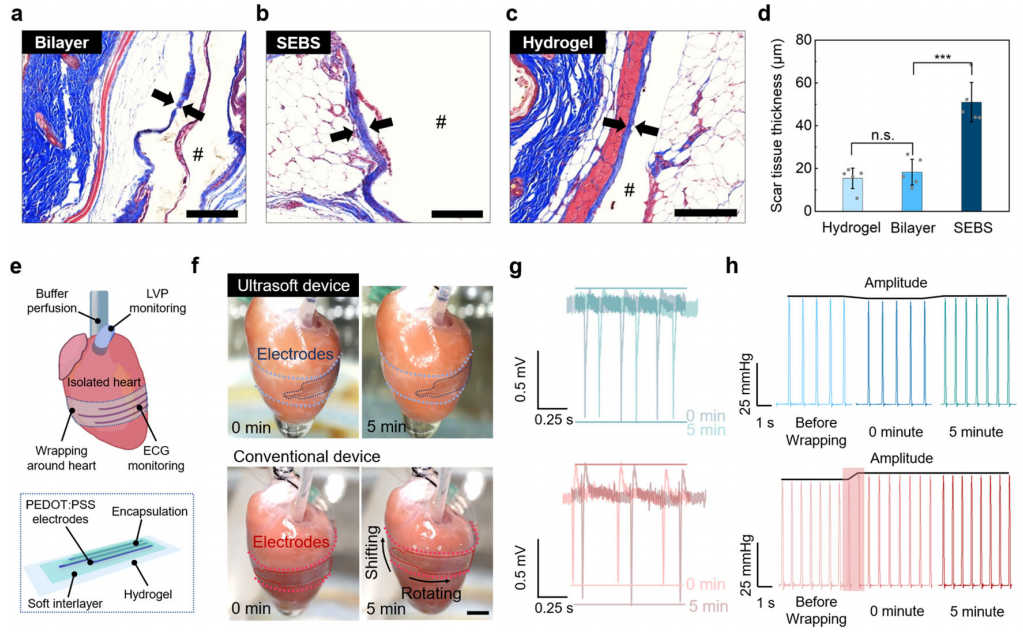
Ultrasoft设备具有抑制免疫反应和与活体组织的机械兼容性。图片来源:Nature Communications
总结
作者展示了一种通用的柔性中间层设计,该设计允许具有相对高模量的可拉伸功能材料用于制造超软和可拉伸电子产品。通过实现均匀的应变分布,该设计可以显著提高基底上功能层的可拉伸性,其模量降低了几个数量级。通过将可拉伸半导体集成到超软基底上而不影响可拉伸性,这种中间层设计使模量低于10 kPa可拉伸晶体管成为可能,这比目前最先进的技术低两个数量级。通过皮肤上整合、皮下体内植入和离体心脏记录,作者证明了类组织模量具有几个优点,包括对不规则表面的良好贴合性、对皮肤和组织的低机械约束和刺激,以及改善的生物相容性。柔性中间层设计的多功能性将使超软模量能够在其他类型的可拉伸设备上实现,如光电探测器、发光二极管、生物传感器和能量收集设备。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













