多篇文章阐明癌症的起源机制
2016-07-26 佚名 生物谷
癌症到底是如何起源发生的?长期以来科学家们在揭示癌症起源的研究上花费了大量的人力和时间,当然他们也取得了一些重大的突破性研究成果。近日刊登在Nature杂志上的一项研究中,来自比利时布鲁塞尔自由大学和剑桥大学研究人员通过对在小鼠研究发现,小鼠机体的皮肤干细胞和祖细胞对一种癌基因激活会产生反应,经过一系列研究,他们最终证实,尽管小鼠机体的祖细胞可以引发机体出现良性病变,但只有干细胞能够发展为致死
癌症到底是如何起源发生的?长期以来科学家们在揭示癌症起源的研究上花费了大量的人力和时间,当然他们也取得了一些重大的突破性研究成果。
近日刊登在Nature杂志上的一项研究中,来自比利时布鲁塞尔自由大学和剑桥大学研究人员通过对在小鼠研究发现,小鼠机体的皮肤干细胞和祖细胞对一种癌基因激活会产生反应,经过一系列研究,他们最终证实,尽管小鼠机体的祖细胞可以引发机体出现良性病变,但只有干细胞能够发展为致死性的侵袭性肿瘤。
本文中,小编盘点了近年来关于癌症起源相关研究的一些进展情况,与各位一起学习!

doi:10.1126/science.aad2197
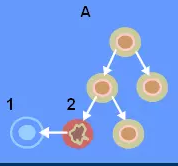
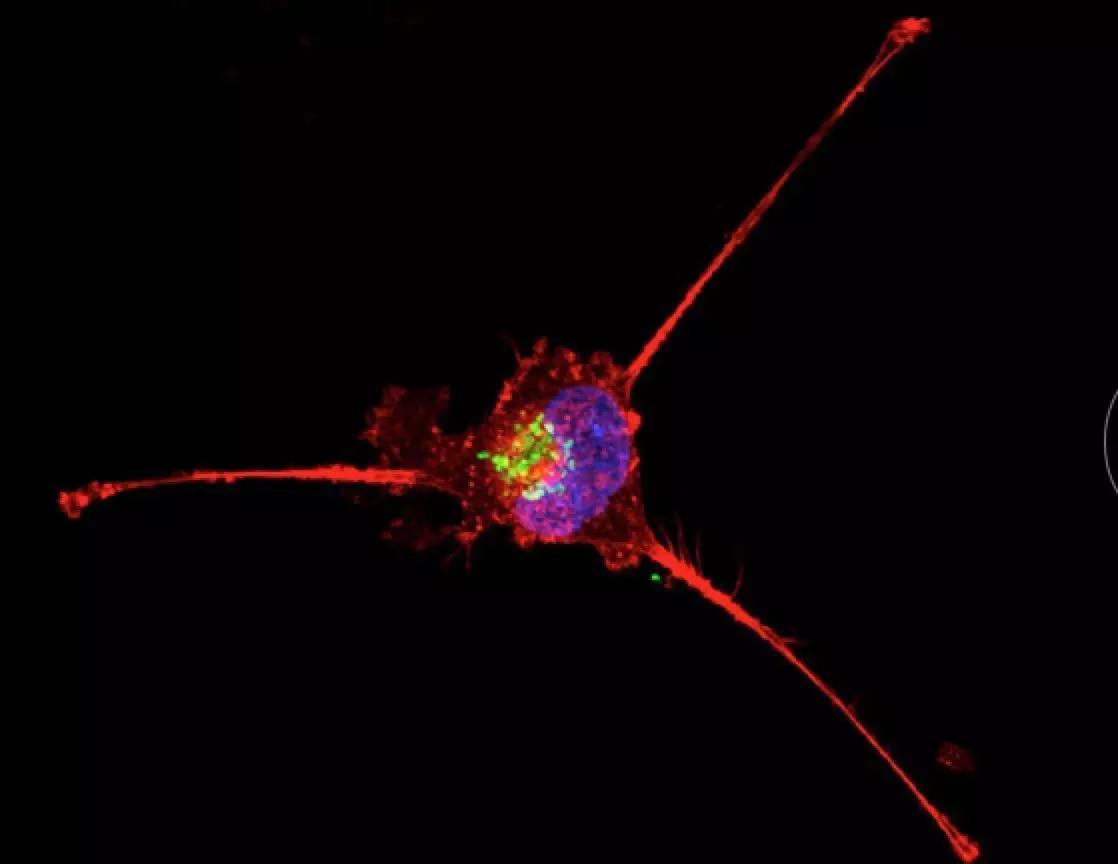
最近,一项刊登于国际杂志Science上的研究论文中,来自波士顿儿童医院的研究人员通过研究首次观察到了癌症起源中受癌症影响的第一个细胞,同时还观察到了癌细胞在活体动物中的扩散情况,相关研究或可帮助研究者理解黑色素瘤及其它癌症的发生机制,并为开发治疗相关癌症的新型疗法提供希望。
研究者Charles Kaufman博士指出,我们并不清楚为何机体中的某些细胞总是在癌症中发生突变,本文研究中我们发现,癌基因激活或肿瘤抑制子缺失后就会引发癌症发生,而且这其中会涉及一些改变将单一细胞推回至干细胞状态,这些改变包括对一系列基因进行靶向作用来阻断癌症开始。
文章中,研究者对活体斑马鱼进行实时成像来追踪黑色素瘤的发生,所有的斑马鱼都携带有人类癌症突变BRAFV600E,这种突变在很多良性痣中存在,但斑马鱼中缺少肿瘤抑制基因p53。研究者对斑马鱼进行工程化操作以便当名为crestin的基因开启时单一细胞会产生出荧光绿,这就可以帮助激活干细胞遗传程序的激活,这种特殊程序在胚胎发育后会被关闭,但偶然间程序中的crestin和其它基因就会开启表达。
新闻阅读:Scientists uncover process that could drive the majority of cancers
p53基因由于在防止基因突变中的突出作用故被描述为“基因组卫士”。超过一半的癌症被认为源于p53突变或丧失作用,而现在最近的一项研究由Richard Moran博士解释了原因。
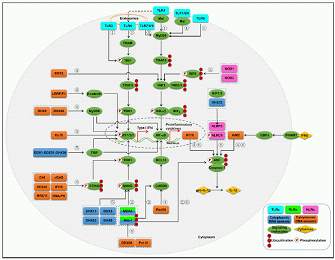
发表在《Molecular Cancer Therapeutics》杂志上的一篇文章研究结果显示,p53基因突变,或失去激活蛋白复合物的功能, 该蛋白复合物称为哺乳动物靶向雷帕霉素复合体1(mTORC1),这有助于调节细胞增殖所需的能源资源。mTORC1由几十种蛋白质组成,细胞使用细胞内的溶酶体胞膜作为支架将所有这些蛋白质聚集在一起。针对正常细胞的需要,p53基因有助于维持适当水平的蛋白质, 在溶酶体中称为结节性硬化症复合体2(TSC2)。当p53功能减退时,研究发现溶酶体TCS2的水平下降,一种小的蛋白质RHEB将取而代之。正是这种RHEB的积累才能激活mTORC1并导致异常的细胞增殖的控制。

doi:10.1073/pnas.1502599112
癌,这个名称是一系列不同恶性组织的统称。一般的理论认为,由单一或者少数细胞起源的恶性增殖组织的生长不受控制,最终形成肿瘤。如果不经治疗,恶性肿瘤会对人体产生很大的伤害,并且最终导致人的死亡。尽管针对癌症的研究已经进行了很多年,而且对于部分癌症在早期也有了针对性的治疗方法,因为缺少相应的模式系统,以及不同癌症起源的复制性,导致我们对于癌症起源的机制还很不清晰。来自中国中山大学、英国索尔福德大学和美国加州大学欧文分校的联合课题组认为,单细胞寄生虫(布氏锥虫和刚地弓形虫)与癌细胞存在一定的相似性,可以使用它们作为模式生物来研究癌症的起源。
癌症的起源现在的理论普遍认为是因为不可控制性的恶性增长和突变的累积,最新的理论还认为,癌细胞所处的组织的选择压力也影响癌症的发展。而且有的癌症似乎是可以传染的。例如一种濒危物种袋獾(Tasmanian devil )可能会通过咬其他个体,导致“袋獾面部肿瘤”从一个个体传染给另一个个体。早在1996年,一个雌性袋獾将这种肿瘤传给其他个体,然后这种肿瘤发展成为两个亚型,在整个种群中传播,并导致了整个种群全部死亡。最近的研究还发现,有些类型的白血病能够从母亲传递给胎儿,从而成为了癌症可以传染的又一个例子。这些传染癌症的例子,与寄生虫的传染存在一定的相似性。
原文来自:Evolution,not just mutation,drives development of cancer
最近发表在《美国科学院院刊》的一篇文章认为,我们对于癌症起因的理论需要进行修改了。这篇文章认为,以前人们认为癌症的起源完全是因为一些基因突变引起的,在致癌基因里的突变导致了癌症细胞的出现并开始扩增。然而,最新的研究认为,在正常的组织中,基因突变的细胞还会受到群体的压力选择,因此这种选择压力和突变一起共同决定着癌细胞以及肿瘤的形成。造成这种选择压力变化的因素与生活方式以及老年化相关。
最新的癌症形成的理论认为,在正常的组织中,本来就由一定的细胞携带着致癌突变,但是健康的个体或者组织中,这些基因突变的细胞还是正常工作着,其致癌的天性一直被正常细胞压制着。直到出现一些偶然或者必然的因素,例如老年化、吸烟、饮酒等,携带者致癌基因的细胞发现环境发生了改变,发展成为癌细胞对自身更加适应,这时候癌细胞便开始爆发。即使在正常组织中,仍然会有很少的癌细胞,但是这些癌细胞并不能竞争的赢正常细胞,因此他们的数量总是低于一定的值,而不会产生肿瘤,但是环境变差,癌细胞会比正常细胞更有适应性,数量开始增加并形成癌症。

近日,来自英国桑格研究所(Wellcome Trust Sanger Institute)等处的研究者通过研究首次揭示了引发肿瘤发育的突变过程,这些突变过程就可以帮助解释30种最为常见的癌症类型,这项研究或可帮助开发治疗以及预防一系列癌症的方法,相关研究刊登于国际杂志Nature上。
每一个突变过程都会留下特殊的突变模式,这就是基因组中引发癌症的印记,研究者通过对人类最常见的癌症中的7042个基因组进行研究,发现了其中20个突变DNA的特性,在这些突变标记中,研究者也鉴别出了隐藏在其背后的生化代谢过程。
所有的癌症都是由于机体细胞的DNA发生突变引起的,尽管我们知道烟草中的化学物可以引发肺部细胞的突变,进而引发肺癌,但是我们对于疾病发病背后的生物学过程却知道地甚少。研究者Ludmil Alexandrov表示,我们鉴别出了癌症的突变标记,这就可以解释病人的癌症发生历史以及其遗传突变标记;目前我们希望通过研究来理解癌症基因组突变标记中的复杂的生物学过程。
英国癌症研究中心的科学家对癌症研究已进入一个新的里程碑。目前已分析了21种癌症,其在健康组织中逐渐癌化的基因突变过程。这一研究的意义体现在能够让科学家更加了解癌症的遗传物质特征,从而可以开发出更好的癌症治疗方法。
目前已知有200多种癌症,光英国每天就有890人被确证为癌症患者。
找出导致突变的原因可找到新的治疗方法。如吸烟是引起的癌症已知的,但是一半以上的癌症病因仍是一个谜。

doi:10.1073/pnas.1120476109
近日,来自巴塞罗那生物医药研究所(IRBB)和斯隆凯特琳癌症研究中心(MSKCC)的研究者揭示了癌症起源新的研究信息,这项研究刊登在了国际著名杂志PNAS上。文章中,研究者表示癌症最初的形式及攻击力取决于机体防卫细胞完整性很多过程的缺失的结合,小鼠实验中,研究者发现高度染色体不稳定性以及程序性细胞死亡的缺失的小鼠很少发展为肿瘤。
肿瘤是否发展依赖于细胞周期中细胞损伤发生的时间,这项研究中,研究者H.Stracker表示,损伤应答可以促使肿瘤发生。
研究者使用癌症关键修复基因突变的小鼠,下一步,他们将这些小鼠和其它有细胞周期关键点或者凋亡相关突变的小鼠结合在一起,直到组合足以启动肿瘤发生或者产生某些类型的肿瘤,这就好比是解构癌症以发现效应因子。分裂细胞在DNA复制期间存在一系列的关键点,复制就在这些合适的关键点来发生。
【8】Nature Methods:不用生物标志物分离出癌症起源细胞
doi:10.1038/nmeth.1430
肿瘤起源细胞也称为肿瘤干细胞。在2月在线出版的《自然—方法学》中,研究人员报告了一种新方法:不用生物标志就可以分离出癌症起源细胞。
尽管有关癌症干细胞的学说有众多争议,但这种学说被广泛接受的一点是,肿瘤中的所有细胞地位并不均等,部分细胞比其他细胞更能启动新的肿瘤。研制出鉴别这种肿瘤起源细胞并将它们从早期肿瘤中分离出的方法,既需要基础研究也需要应用研究。
采用一种非传统的方法,Ivan Radovanovic和同事从人类神经胶质瘤中分离出了癌症起源细胞。分离这种细胞的标准方法要使用蛋白质生物标志,这种标志会在特定的蛋白质中表达出来,但目前即使最好的标志也没有足够的特殊性。Radovanovic和同事指出,根据神经胶质瘤启动细胞天然的自身荧光和细胞形状,可以从人类的神经胶质瘤中反复提取出这种细胞。

来自斯坦福大学医学院的研究人员发现,膀胱粘膜的一种细胞类型导致了大多数的浸润性膀胱癌病例。这项在小鼠中完成的研究首次指出一种正常的细胞类型可以导致浸润性的膀胱癌。它也第一次证实了大多数的膀胱癌及相关癌前病变是由一种细胞所引起,揭示了许多人类膀胱癌在治疗后复发的原因。
研究的资深作者、生物化学和发育生物学教授Philip Beachy博士说:“我们已经知道,在癌症发展的一个中间阶段,一种癌症干细胞和它的后代细胞可以快速并完全取代整个膀胱粘膜。所有这些细胞一路经历数个步骤变成了一种侵袭性肿瘤。因此,当用手术成功切除浸润性癌症时,这一遭到破坏的粘膜仍然存在,并有极高的进展概率。”
尽管这些癌症干细胞以及它们在膀胱粘膜形成的癌前病变普遍表达一种重要的信号蛋白sonic hedgehog,随后形成的浸润性癌症癌细胞却一律不表达sonic hedgehog——这一开关似乎对于侵袭和转移至关重要。这或许可以解释以往人类膀胱癌细胞起源研究某些令人困惑的方面。它也指出了可被治疗靶向的、癌症进化中的一个薄弱环节。

DOI:10.1126/science.1252510
来自纪念斯隆-凯特琳癌症中心,哥伦比亚大学等机构的研究人员在最新一期《科学》(Science)杂志上介绍了肿瘤相关巨噬细胞TAM的细胞和分子发生过程,指出这种特殊细胞的一些具体特征,这将为癌症免疫疗法提出新希望。
一直以来,巨噬细胞都被认为是一种进化历史悠久的细胞类型,参与了组织动态平衡和针对病原体的免疫防御过程。这种细胞能帮助我们的机体对有害刺激和组织损伤做出应答反应,尤其在清除死细胞和外源物质中起重要的作用。此前的一些研究发现巨噬细胞以及它们促成的炎症反应一方面是有益的,如可杀死感染性生物;另一方面也可以是有害的,由此导致不受控制的组织损伤和功能障碍或器官衰竭。
而近年来的一些研究进一步表明,巨噬细胞是癌症发生的调控因子,这种前哨免疫细胞能够调查组织微环境,释放细胞因子响应外源性损伤和内源性事件,如肿瘤的发生。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











有了新的认识,受益匪浅!
122
学习学习!
107