Brain:肌萎缩性侧索硬化症RNA结合蛋白错误定位的新机制
2022-09-23 brainnew神内神外 brainnew神内神外
研究表明神经元发育过程中表现出大部分的瞬时IR的转录物只存在于细胞核,而是瞬时定位于细胞质,并且该转录物池对RBP具有很强的结合亲和力。
导读:
过去研究表明,内含子保留(IR)在哺乳动物中的频率比最初识别的频率更高,从而影响大多数基因的转录本。值得注意的是,与其他类型的细胞相比,具有异常极性和分隔性的神经细胞表现出更高的IR,并在神经元稳态中发挥功能性作用。
IR以前曾通过与RNA降解途径偶联而参与调控转录组。尽管内含子保留转录本(IRTs)主要被鉴定为存在于它们被降解的核内,但是有越来越多的证据表明稳定IRT的细胞质定位。这一现象的普遍程度和作用仍未得到充分研究。
肌萎缩性侧索硬化症(ALS)是一种快速进展且无法治愈的疾病,会导致运动神经元(MNs)相对选择性的变性。其分子病理学特征是关键RNA结合蛋白(RBP)的核到细胞质定位错误。
近日有研究将IR描述为主要的剪接事件,它表征了来自人iPSC的运动神经元谱系限制的早期阶段,受到遗传多样的ALS致突变的干扰。然而,这个过程是否会类似地影响核或细胞质亚细胞区域仍未得到解决。
2021年3月9日,伦敦大学Rickie Patani团队在Brain 上发表了标题为:“Aberrant cytoplasmic intron retention is a blueprint for RNA binding protein mislocalization in amyotrophic lateral sclerosis”的文章。

该研究使用时间分辨的hiPSCs进行运动神经发生的核和细胞质部分的深度测序,揭示了引起ALS的VCP基因突变导致IRT的区室特异性异常积累。这项研究为潜在的病理机制提供了新的见解,并指出异常的细胞质IRTs作为潜在的治疗靶点。
1. 人类运动神经发生过程中核和细胞质部分的高覆盖率RNA-seq数据
人类运动神经发生过程中的时间分辨细胞分离和RNA测序揭示了ALS中广泛的异常细胞质IR。研究表明异常的胞浆IR在肌萎缩侧索硬化症中是一种普遍的现象,产生于运动神经发生的早期阶段。
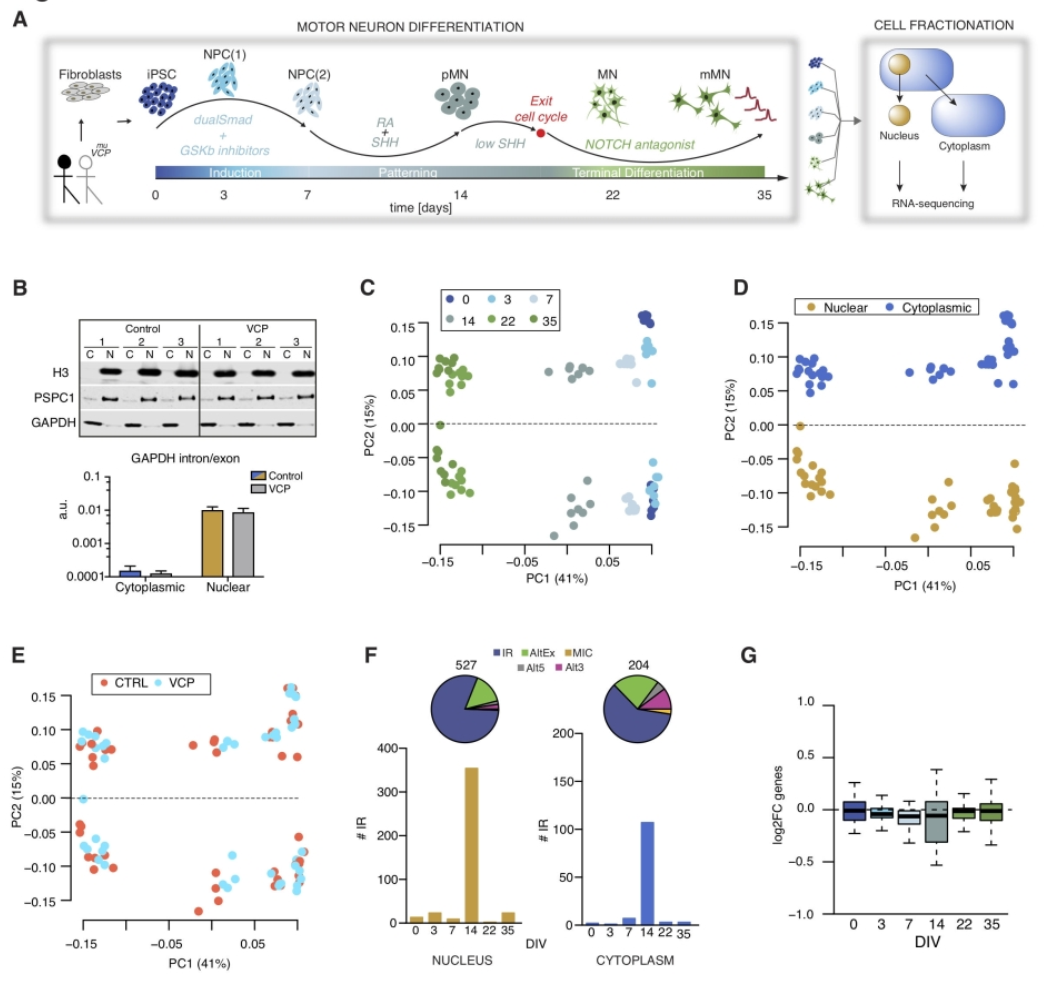
图1:人类运动神经发生过程中的时间分辨细胞分级分离和RNA测序揭示了ALS中广泛的异常细胞质IR
2. 异常的核和细胞质内含子序列表现出明显的特征。
研究发现大量IRT(包括SFPQ, OGT, TUSC3和DDX39)在VCPmu培养中表现出胞质丰度的特定增加,这表明VCP突变导致异常的核输出和/或特定类别IRT的胞质稳定,因此导致细胞功能障碍。
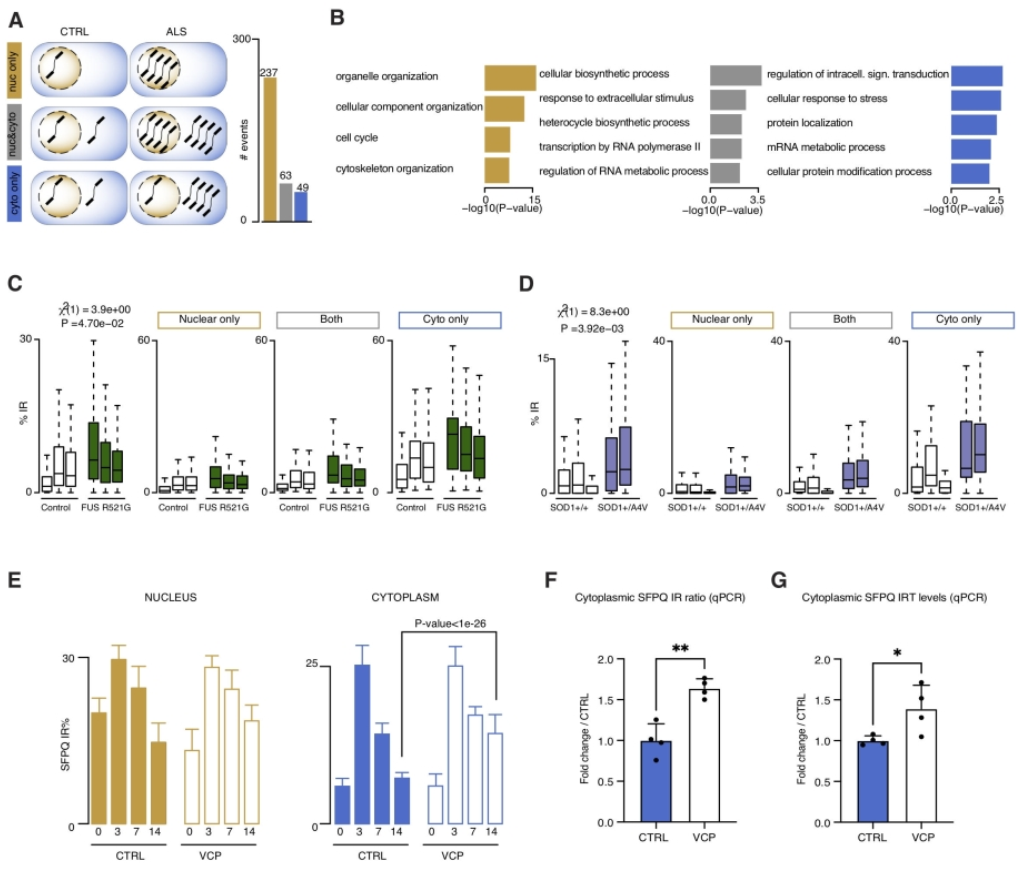 图2:异常的核和细胞质内含子序列表现出明显的特征
图2:异常的核和细胞质内含子序列表现出明显的特征
3. 胞质内含子保留转录本为结合的RBPs创造了一个容易定位错误的环境。
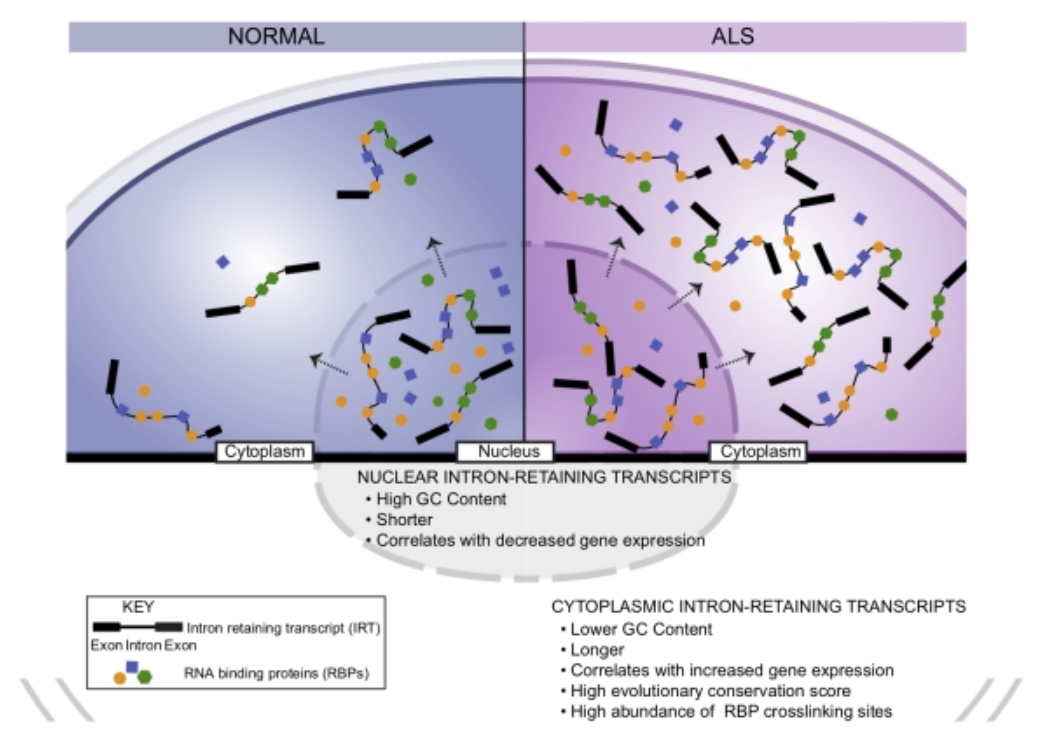
先前的研究表明,保留的内含子平均而言更短且富含G/C,本研究发现只有主要是核异常保留的内含子才表现出这些特征。与此相反,异常保留在细胞质内的内含子平均更长,且G/C含量较低。
该研究使用更丰富的数据集进一步检查了RBP与异常细胞质IRT之间相互作用的性质。与它们的细胞核主要配对物相比,至少27个RBP系统性地显示出与胞质主要保留内含子的结合在统计学上显着增加。这些RBP形成了紧密连接的网络,这些网络由经过实验验证的相互作用蛋白组成,这些蛋白富含mRNA代谢功能。
这进一步暗示了ALS发病机理中转录后剪接的破坏。重要的是,在该RBP网络中也有在ALS中表现出标志性的核到细胞质错位的蛋白,包括SFPQ,反式激活反应DNA结合蛋白TDP-43和FUS。
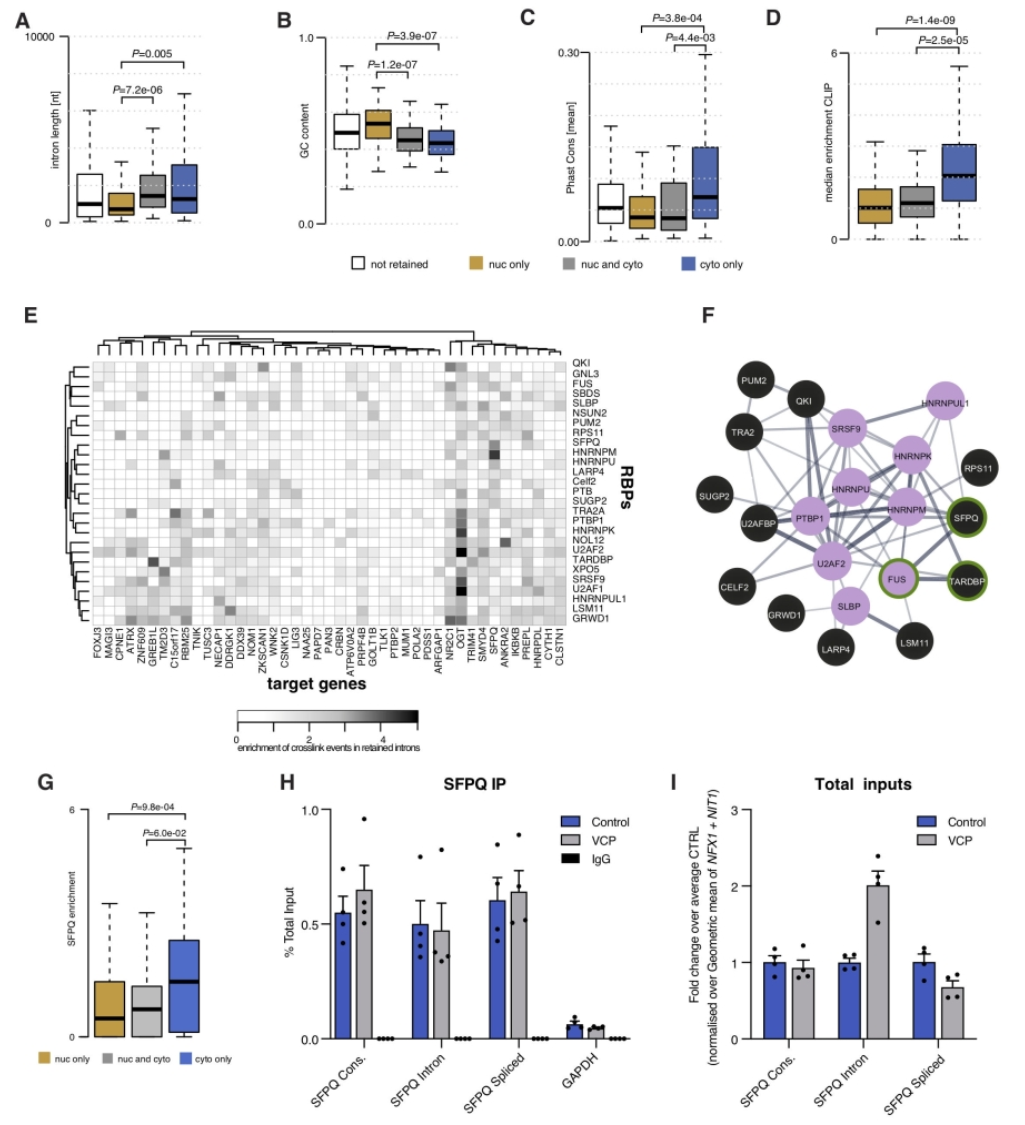 图3:细胞质内含子保留转录物为结合的rbp创造了一个易发生错误定位的环境
图3:细胞质内含子保留转录物为结合的rbp创造了一个易发生错误定位的环境
总结与展望
综上所述,本研究表明神经元发育过程中表现出大部分的瞬时IR的转录物只存在于细胞核,而是瞬时定位于细胞质,并且该转录物池对RBP具有很强的结合亲和力。这给IRTs的潜在作用增加了新的有趣的复杂性,包括在神经元发育过程中调节基因表达。未来的研究将直接评估该假设。
总之,本研究认为细胞质保留的内含子在RBP定位的稳态控制中起RNA调节剂的作用,并且与ALS相关的细胞质IR转录物异常增加会破坏这一过程。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言