Nature:南京医科大学沙家豪/郭雪江等团队合作发现雄性生殖细胞特异性核糖体控制雄性生育能力
2022-12-15 iNature iNature 发表于上海
该研究报道了一种具有专门的新生多肽出口通道的核糖体,RibosomeST,它与雄性生殖细胞特异性蛋白RPL39L组装在一起,RPL39L是核心核糖体(RibosomeCore)蛋白RPL39的副产物。
核糖体是高度复杂的翻译机器,已被证明在调节蛋白质合成方面具有异质性。男性生殖细胞的发育涉及到精子形成过程中复杂的翻译调节。然而,尚不清楚精子形成过程中的翻译是否由特定的核糖体完成。
2022年12月14日,南京医科大学沙家豪、郭雪江及中国科学院生物物理研究所秦燕共同通讯在Nature 在线发表题为“A male germ-cell-specific ribosome controls male fertility”的研究论文,该研究揭示了一种雄性生殖细胞特异性核糖体,能够控制雄性生育能力。该研究报道了一种具有专门的新生多肽出口通道的核糖体,RibosomeST,它与雄性生殖细胞特异性蛋白RPL39L组装在一起,RPL39L是核心核糖体(RibosomeCore)蛋白RPL39的副产物。
小鼠核糖体缺失导致精子形成缺陷,导致生育能力大大降低。作者对小鼠肾脏和睾丸核糖体的单颗粒冷冻电镜结构进行了比较,表明与RibosomeCore相比,RibosomeST具有不同大小和电荷态的核糖体多肽出口通道。核糖体主要共转录调节雄性生殖细胞特异性蛋白质子集的折叠,这对精子的形成至关重要。此外,该研究发现RibosomeST的特殊功能不能被RibosomeCore替代。综上所述,这种精子特异性核糖体的鉴定将极大地扩展人们对核糖体功能和哺乳动物蛋白质表达模式的组织特异性调控的理解。

核糖体是高度复杂的翻译机器,从mRNA催化蛋白质生物合成。越来越多的研究表明核糖体是异质的。例如,含有RPL10A/uL1和RPS25/eS25的核糖体在小鼠胚胎干细胞中翻译不同的mRNAs池。与核糖体蛋白(RP) RPL3相比,RPL3L被发现在心脏和骨骼肌中表达最多,以前被证明可以抑制肌管生长和肌肉功能。
最近的另一项研究表明,RPL22和RPL22L1都被纳入核糖体。RPL22L1蛋白上调与结直肠癌不良预后相关。Rpl38的突变导致了更短的尾巴、额外的肋骨和其他解剖缺陷。总之,这些研究表明核糖体是异质的,在蛋白质生物合成的调节中表现出组织特异性功能。然而,核糖体异质性的精确调控机制仍然知之甚少,需要对核糖体构型的组织特异性变异进行系统的结构功能分析。
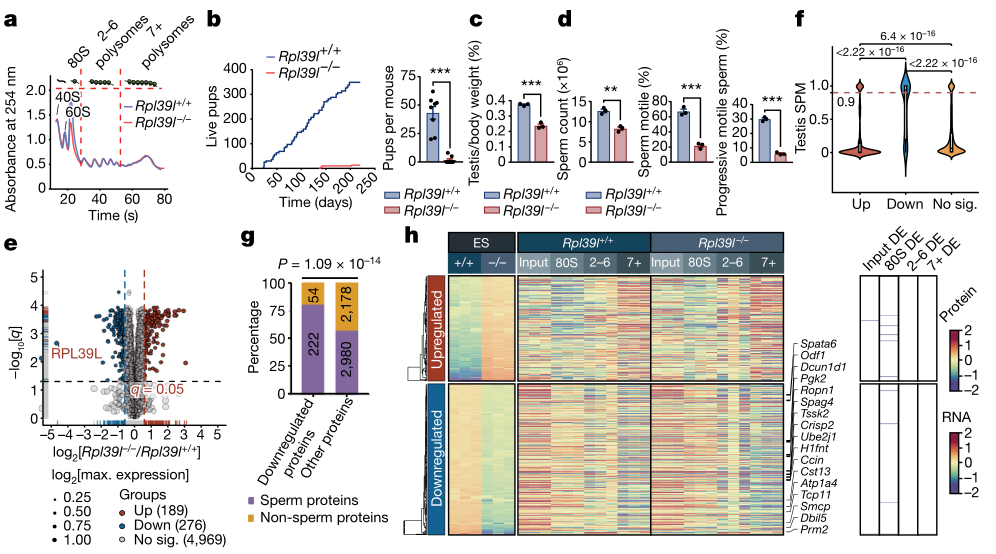
RibosomeST缺失导致雄性不育和ESs蛋白减少(图源自Nature )
在这里,该研究发现RibosomeST共翻译折叠参与精子形成的蛋白质亚群,其特点是高稳定性。小鼠核糖体缺失导致精子形成缺陷,导致生育能力大大降低。作者对小鼠肾脏和睾丸核糖体的单颗粒冷冻电镜结构进行了比较,表明与RibosomeCore相比,RibosomeST具有不同大小和电荷态的核糖体多肽出口通道。
核糖体主要共转录调节雄性生殖细胞特异性蛋白质子集的折叠,这对精子的形成至关重要。此外,该研究发现RibosomeST的特殊功能不能被RibosomeCore替代。这些生殖细胞特有的蛋白质必须在精子中保持稳定,以确保精子在渗透到卵母细胞之前的功能。总之,该发现解决了一个长期存在的难题,即精子蛋白质如何在其一生中保持功能和稳定性。
原文链接:
https://www.nature.com/articles/s41586-022-05508-0
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











学习充电
49