阿斯利康携手第一三共开发的trastuzumab deruxtecan研究结果喜人,HER2阳性转移性乳腺癌患者中位无进展生存期达16.4个月
2019-12-12 不详 生物谷
阿斯利康和第一三共今日公布了针对trastuzumab deruxtecan (DS-8201)的全球关键性II期单臂临床试验(DESTINY-Breast01)的详细数据。这是一款靶向HER2的抗体偶联药物(ADC),用于此前接受过两种或两种以上抗HER2治疗的HER2阳性转移性乳腺癌患者。在接受trastuzumab deruxtecan(5.4毫克/千克)治疗的患者中,经独立中央评估确认,作
阿斯利康和第一三共今日公布了针对trastuzumab deruxtecan (DS-8201)的全球关键性II期单臂临床试验(DESTINY-Breast01)的详细数据。这是一款靶向HER2的抗体偶联药物(ADC),用于此前接受过两种或两种以上抗HER2治疗的HER2阳性转移性乳腺癌患者。
在接受trastuzumab deruxtecan(5.4毫克/千克)治疗的患者中,经独立中央评估确认,作为主要终点的客观缓解率(ORR)达到60.9%。入组患者此前接受过中位达6线(2-27)的针对转移性疾病的相关治疗。
患者的疾病控制率(DCR)为97.3%,中位缓解持续时间(DoR)为14.8个月,中位无进展生存期(PFS)为16.4个月。试验尚未达到患者中位总生存期(OS),患者一年生存率估计为86%。相关结果在各类患者亚组中保持一致。
丹娜法伯癌症研究所Susan F. Smith女性癌症研究中心乳腺癌研究中心副主任,DESTINY-Breast01试验首席研究员Ian E. Krop表示:“这些结果特别引人注目。Trastuzumab deruxtecan能够在很大程度上帮助患者实现持久的肿瘤减灭,而其中大多数患者已几乎用尽了HER2转移性乳腺癌的所有标准疗法。我们对这些结果感到兴奋,它有望为晚期乳腺癌患者带来帮助。”
试验研究结果:
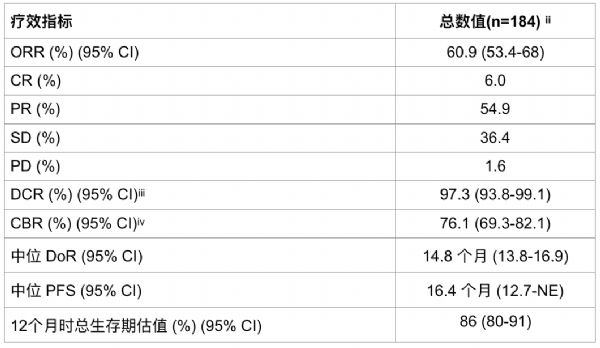
CI,置信区间; CR,完全缓解; PR,部分缓解; SD,稳定疾病; PD,进行性疾病; NE,不可估量。
i经独立中央审查评估
ii 5.4毫克/公斤
iii DCR为(CR + PR + SD)
iv CBR为(CR + PR + SD≥6个月)
相关数据已在2019年圣安东尼奥乳腺癌研讨会上对外发布,并同时在线发布于《新英格兰医学杂志》。
患者此前接受的疗法包括曲妥珠单抗-美坦新偶联物(100%),曲妥珠单抗(100%),帕妥珠单抗(65.8%),其他抗HER2治疗(54.3%),激素治疗(48.9%)以及其他系统性治疗(99.5%)。trastuzumab deruxtecan的中位治疗时间为10个月(0.7-20.5),中位随访时间为11.1个月(0.7-19.9)。截至2019年8月1日的数据,仍有42.9%的患者在接受治疗。
在DESTINY-Breast01试验中, trastuzumab deruxtecan的安全性与耐受性与I期试验中所观察到的保持一致。最常见的3级或更高级别的治疗相关紧急不良事件包括中性粒细胞计数减少(20.7%),贫血(8.7%),恶心(7.6%),白细胞计数减少(6.5%),淋巴细胞计数减少(6.5%)和疲劳(6.0%)。总体而言,通过独立审查确定,有13.6%的患者确诊患有与治疗相关的间质性肺病(ILD)。相关不良事件的严重程度主要为1级或2级(10.9%),仅有一例为3级(0.5%),无4级不良事件。有4例死亡事件(2.2%)被确定归因于ILD。
最近,美国食品药品监督管理局接受了trastuzumab deruxtecan用于治疗HER2阳性转移性乳腺癌患者的上市申请,并授予其优先评审资格。公司还向日本厚生劳动省提交了药品上市申请。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#研究结果#
51
#mAb#
56
#HER2阳性转移性乳腺癌#
89
#AST#
49
#deruxtecan#
82
#TRA#
54
#TEC#
73
#HER2阳性#
78
#生存期#
72
#转移性#
79