美国临床肿瘤学会(ASCO)年会,6月3日,在芝加哥以线上+线下会议的形式举行。作为全球临床肿瘤学研究的“奥林匹克盛会”,ASCO今年收到了全球几十个国家的上千份最新研究进展,其中囊括了各种重磅的大型临床试验(clinical trial)。
梅斯医学近日,采访了上海交通大学附属胸科医院的肺癌研究专家韩宝惠,他推荐了肺癌领域,最值得关注的7个重要领域,即,KRAS,MET,ROS1,靶向治疗,RET, NTRK,免疫领域。
藉此,本文简要总结了这7个领域的重磅研究结果,和大家分享。
1. KRAS领域:
KRAS-G12C突变是当下研究的热点。
KRAS是促进细胞生长和增殖的RAS/MAPK信号级联的一个关键媒介。KRAS-G12C突变,见于14%的非小细胞肺癌(NSCLC)中。
Adagrasib是一种KRASG12C抑制剂,它能不可逆地、选择性地结合KRAS-G12C,将其锁定在无活性状态。Adagrasib经过优化,具有良好的药代动力学(PK)特性,包括长半衰期(~24小时)、剂量依赖性PK和中枢神经系统穿透性;它在1/1b期研究中表现出客观反应和良好的耐受性。

美国Virginia Cancer Specialists Research Institute的Alexander I. Spira等人,基于KRYSTAL-1,这个多队列1/2期研究,评估adagrasib作为单药或联合方案治疗携带KRASG12C突变的晚期实体肿瘤患者。(Abstract #9002)
共116名携带KRASG12C突变的NSCLC患者被纳入并接受治疗,中位随访时间为12.5个月。基线特征包括中位年龄64岁,65%为女性,15.5%/83.6%为ECOG PS 0/1;98.3%的患者在之前接受免疫治疗和化疗后接受了adagrasib治疗。
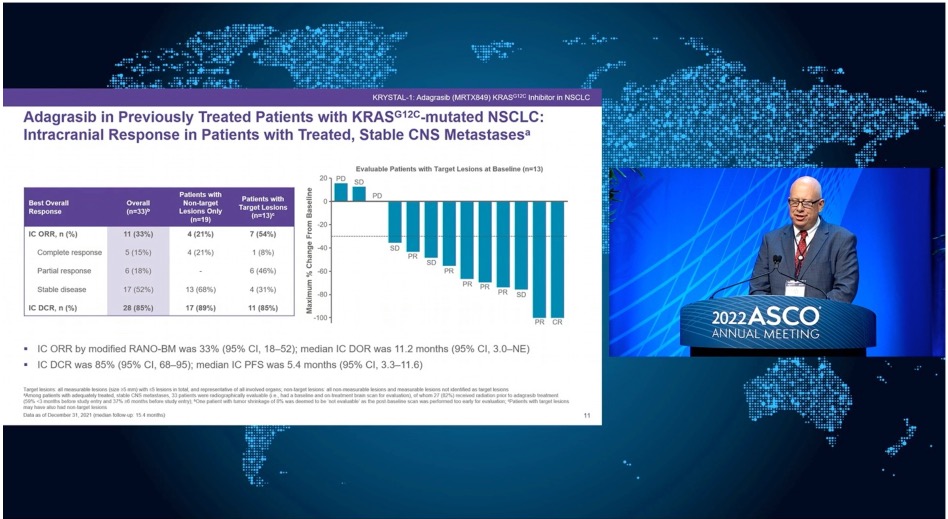
他们发现:Adagrasib对携带KRASG12C突变的NSCLC预处理患者,具有良好的耐受性,并显示出良好的疗效。因此,他们正在进行3期试验,评估并对比adagrasib与 docetaxel的效果,该试验针对先前接受过治疗的KRAS-G12C突变NSCLC患者(NCT04685135)。
2. MET领域:
CHRYSALIS(NCT02609776)是一项正在进行的晚期NSCLC患者Amivantamab的1期剂量升级/剂量扩展研究。(Abstract #9008)
Amivantamab是一种针对表皮生长因子受体(EGFR)和MET的全人类双特异性抗体,已被批准用于治疗先前基于铂金的化疗后有EGFR外显子20插入的非小细胞肺癌(NSCLC)。鉴于其双特异性,在CHRYSALIS研究的MET-2队列中,Amivantamab正在对原发性MET 14外显子跳变(METex14)患者 的治疗效果未知。
有43名METex14患者接受了Amivantamab。中位年龄为70岁(范围43-88),58%为女性,之前的治疗线中位数为2(范围0-10)。
他们发现:无论之前是否接受过治疗,临床获益率都大于54%(如图1)。中位反应持续时间(DOR)未达到(范围为2.1-12.2个月);67%(8/13)的DOR≥6个月。
由此可见,Amivantamab在原发性METex14 NSCLC中显示出抗肿瘤活性,包括在之前的MET抑制剂治疗之后。
3.ROS1领域:
ROS1原癌基因融合( gene fusion),存在于1-2%的NSCLC病例中。由于中枢神经系统转移,在ROS1-融合阳性(fusion positive) NSCLC患者中很常见,并与不良预后有关,因此需要对这些患者进行中枢神经系统活性治疗。
恩曲替尼(entrectinib)和克唑替尼(crizotinib)是ROS1的酪氨酸激酶抑制剂(TKIs),被推荐作为ROS1-fp NSCLC的一线治疗。这两种药物已经显示出强大的这两种药物在ROS1-fp NSCLC患者中显示出强大的系统疗效和良好的耐受性。
荷兰鹿特丹大学-伊拉斯谟医学中心Anne-Marie C. Dingemans 牵头的这项随机、开放标签、多中心的3期试验(NCT04603807)旨在比较:在有或无基线 CNS 转移 (mets) 的局部晚期/转移性ROS1融合阳性 (fp) NSCLC患者中,entrectinib与crizotinib的疗效和安全性。(Abstract TPS9141)
其核心假设:恩曲替尼,可能比克唑替尼有更大的中枢神经系统活性,有可能潜在地解决了ROS1-fp NSCLC患者对中枢神经系统转移的未满足需求。
截至2022年1月12日,有8名患者入选,后续的结果,敬请留意,保持关注。
4.靶向治疗领域:
EGFR ins20突变型NSCLC的治疗,一直是个挑战。虽然最近批准了针对EGFR ins20的新药,但不良事件(AE),特别是野生型(WT)EGFR相关的AE很常见。CLN-081是一种新型的EGFR酪氨酸激酶抑制剂(TKI),对包括ins20在内的EGFR突变具有广泛的活性,并且对ins20与WT EGFR的选择性增强。
CLN-081已被FDA授予突破性治疗指定用药,用于治疗EGFR ins20 NSCLC患者。
藉此,哈佛大学麻省总院的Zofia Piotrowska等人,在晚期EGFR ins20突变NSCLC患者中,对CLN-081的治疗情况,进行了初步多中心 1/2a期研究。(Abstract #9002)
他们纳入了39名接受治疗的患者,剂量为100毫克,每天两次(BID),为期21天。
结果表明,对于接受过大量治疗的晚期EGFR ins20 NSCLC患者,CLN-081具有可控的安全性,在测试的剂量范围内具有抗肿瘤活性。此外,CLN-081在100mg BID的剂量下表现出良好的临床状况,客观反应率令人鼓舞,反应持久,并且没有3级皮疹或腹泻现象。
5.RET领域:
在1-2%的肺腺癌和10-20%的甲状腺乳头状癌中发现RET融合。50-60%的甲状腺髓样癌(MTCs)发生激活的RET突变。Selpercatinib是FDA批准的第一个选择性RET抑制剂,适用于RET融合阳性的NSCLC和甲状腺癌,以及RET突变的MTC患者。
尽管有明显和持久的活性,但最终会通过各种机制产生获得性耐药。LOXO-260是一种高效和选择性的RET抑制剂。
LOXO-NGR-21001是LOXO-260在RET融合阳性晚期实体瘤和RET突变MTC患者中进行的一项全球性、开放标签、首次人体1期研究,这些患者之前接受过一种选择性RET抑制剂。(NCT05241834)
符合条件的患者必须事先接受过选择性RET抑制剂,有记录的RET融合或RET突变,根据疾病特异性标准诊断为局部晚期、不可切除和/或转移性癌症,并且必须对标准疗法有进展或不耐受,或者拒绝这种疗法。(Abstract TPS8595)
这个振奋人心的试验,正在如火如荼的进行中,让我们拭目以待接下来的临床新发现。
6.NTRK领域:
神经营养性酪氨酸受体激酶(NTRK)基因融合,已被确定为包括肺癌在内的多种肿瘤类型的致癌驱动因素。拉罗替尼Larotrectinib是一种高选择性、具有中枢神经系统(CNS)活性的TRK抑制剂。之前的研究表明,在15名研究者评估的肺癌患者中,表现出73%的客观反应率(ORR)(Drilon et al.,JCO Precis Oncol 2022)。
Weill Cornell Medical College的Alexander E. Drilon等人,纳入两个larotrectinib临床试验(NCT02576431和NCT02122913)的TRK融合肺癌患者数据,评估了larotrectinib治疗TRK融合肺癌的效果。(Abstract #9024)
共有26名TRK融合肺癌患者(24名非小细胞肺癌患者,1名非典型类癌患者,1名神经内分泌患者)入组,包括10名基线时有中枢神经系统转移的患者。
在10名有基线中枢神经系统转移的可评估患者中,ORR为80%(95% CI 44-97):8个PR和2个SD。
24个月的反应期和无进展生存期的比率分别为72%和67%。对于10名有中枢神经系统转移的可评估患者,12个月的生存率、PFS和OS率分别为26%、22%和78%。
7.免疫领域:
ADXS-503,是一种具有22种肿瘤相关抗原的肺癌特异性免疫疗法。
Pembrolizumab治疗进展的转移性非小细胞肺癌(NSCLC)患者,无明显效果后,ADXS-503的叠加疗法。藉此,加州大学洛杉矶分校的Aaron E. Lisberg等人,探究Pembrolizumab治疗效果不佳时,A503的免疫原性和潜在的免疫抵抗逆转作用。
他们发现,在13名可以评估的患者(帕博利珠单抗治疗后发生进展的患者)当中,使用ADXS-503后,总体缓解率为达到15.4%,疾病控制率(DCR)为46%。
Pembrolizumab治疗效果不佳而疾病进展时,能诱导先天性和适应性免疫反应,这可能恢复或增强检查点抑制剂的敏感性,使患者临床获益。(NCT03847519 )
参考素材:
Drilon A, Tan DSW, Lassen UN, et al. Efficacy and Safety of Larotrectinib in Patients With Tropomyosin Receptor Kinase Fusion-Positive Lung Cancers. JCO Precis Oncol. 2022;6:e2100418. doi:10.1200/PO.21.00418
Thai AA, Solomon BJ, Sequist LV, Gainor JF, Heist RS. Lung cancer. Lancet. 2021;398(10299):535-554. doi:10.1016/S0140-6736(21)00312-3
Cory L, Chu C. ADXS-HPV: a therapeutic Listeria vaccination targeting cervical cancers expressing the HPV E7 antigen. Hum Vaccin Immunother. 2014;10(11):3190-3195. doi:10.4161/hv.34378
Kim D, Xue JY, Lito P. Targeting KRAS(G12C): From Inhibitory Mechanism to Modulation of Antitumor Effects in Patients. Cell. 2020;183(4):850-859. doi:10.1016/j.cell.2020.09.044
https://ascopubs.org/doi/abs/10.1200/JCO.2021.39.15_suppl.2616
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#荟萃#
83
#ASC#
101
#重磅#
114