【JHO】蔡清清教授:NK/T细胞淋巴瘤的新靶点和新药物
2023-07-31 聊聊血液 聊聊血液 发表于上海
文章描述了NKTCL的主要分子学特征和相应的靶向治疗方法,并对未来发展进行了展望。现整理部分内容供各位老师参考。
NK/T细胞淋巴瘤
NK/T细胞淋巴瘤(NKTCL)是一种罕见的、高度侵袭性的非霍奇金淋巴瘤(NHL)亚型,与EB病毒(EBV)感染密切相关,以结外累及为特征。NKTCL细胞表达高水平的p-糖蛋白,因此对含蒽环类药物不敏感。基于L-天冬酰胺酶的治疗方案可改善NKTCL患者的生存,现在已得到NCCN指南推荐,相关方案包括SMILE(地塞米松、甲氨蝶呤、异环磷酰胺、L-天冬酰胺酶和依托泊苷)方案、改良SMILE(使用培门冬酶代替L-天冬酰胺酶)、P-GemOx (培门冬酶、吉西他滨和奥沙利铂)和DDGP(地塞米松、顺铂、吉西他滨和培门冬酶)方案。尽管取得了这些进展,但复发或难治性(r/r)患者的生存结局仍然很差,在非蒽环类药物一线治疗后复发的患者中位总生存期仅为6个月。
基因检测,特别是高通量测序,已经从根本上改变了NKTCL的治疗前景。《Journal of Hematology & Oncology》近日发表一篇综述,通讯作者为中山大学附属肿瘤防治中心蔡清清教授。文章描述了NKTCL的主要分子学特征和相应的靶向治疗方法(如免疫检查点抑制剂、细胞表面靶向药物、表观遗传学靶向药物、信号通路抑制剂;重点在r/r NKTCL患者中进行评估),并对未来发展进行了展望。现整理部分内容供各位老师参考。

细胞表面靶向抗体
已有多种细胞表面抗原开发用于NKTCL的靶向治疗(图1)。
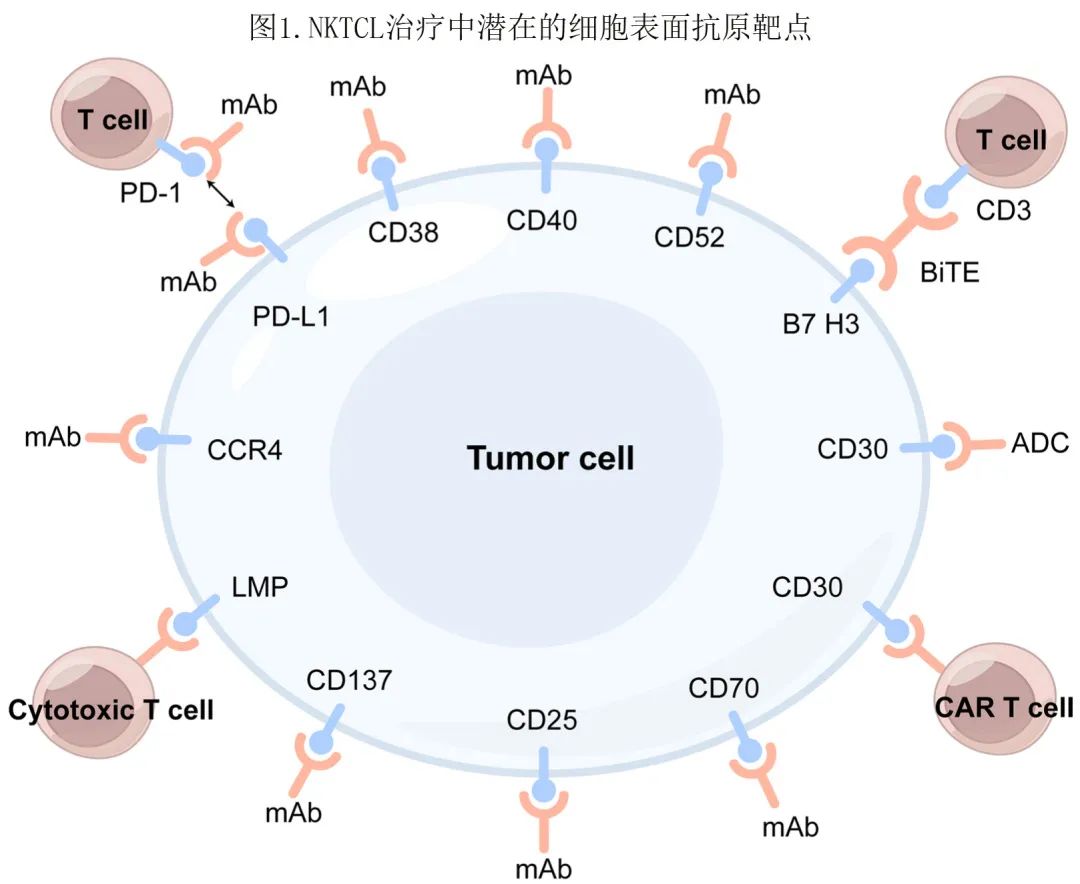
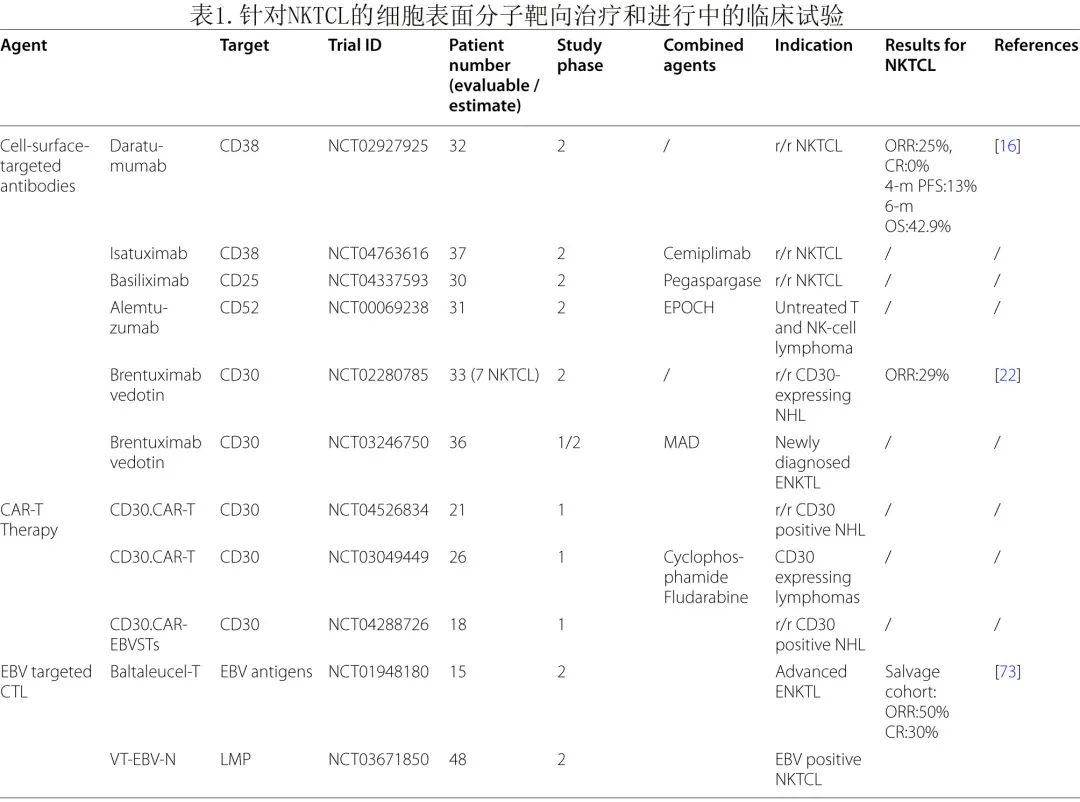
表1列出了NKTCL正在开发中的针对细胞表面抗原及其偶联形式的单克隆抗体(mAbs),包括CD38单克隆抗体(达雷妥尤单抗、isatuximab)、CD30抗体-药物偶联物(ADC)(维布妥昔单抗)、CD52单克隆抗体(alemtuzumab)、CD25单克隆抗体(basiliximab)、CC4单克隆抗体(mogamulizumab,仅针对皮肤T细胞淋巴瘤,NKTCL中无相关试验)、CD40单克隆抗体(dacetuzumab,NKTCL中无相关试验)、B7‑H3双特异性T细胞接合器(BiTEs) (NKTCL中无相关试验),以及仍处于极早期临床前阶段的CD70和CD137单克隆抗体等。
免疫检查点抑制剂(ICI)
39% - 100%的NKTCL患者表达PD-L1。许多ICI,包括PD-1单抗帕博利珠单抗、信迪利单抗、替雷利珠单抗和特瑞普利单抗,PD-L1单抗舒格利单抗、avelumab和IMC-001),以及双靶向抗pd1 /PD-L1抗体IBI318,已在NKTCL中进行研究(表2)。
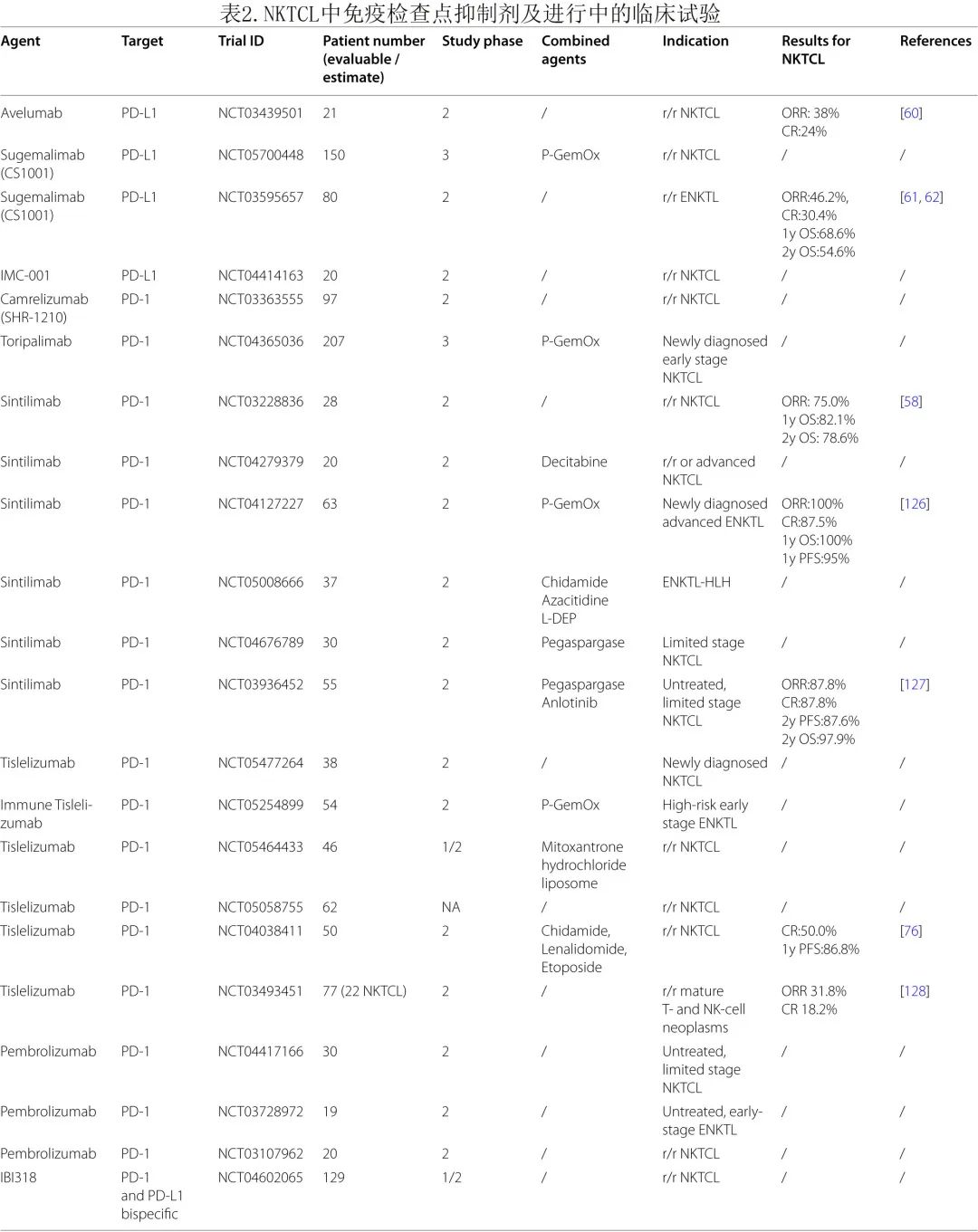
其他免疫检查点分子也在NKTCL患者中上调,但还没有基于这些分子的靶向治疗,包括TGF-β1、CTLA-4、TIM-3、TIGIT、BTLA和LAG-3。
靶向EBV细胞治疗
潜伏期II型EBV抗原(latency II pattern EBV antigens)包括LMP1、LMP2和EBV核抗原1 (EBNA1),在EBV阳性肿瘤细胞中广泛表达,并与NKTCL细胞的存活和增殖有关,LMP1可通过NF-κB通路促进NKTCL细胞的存活、增殖、侵袭和迁移。
EBV靶向细胞疗法(例如LMP2或LMP1/2为靶点的CTL、自体EBV特异性T细胞baltaleucel-T、自体LMP特异性CTL)可以诱导NKTCL患者持续的治疗反应,但仍需要优化细胞毒T淋巴细胞(CTL)扩增。
免疫调节剂
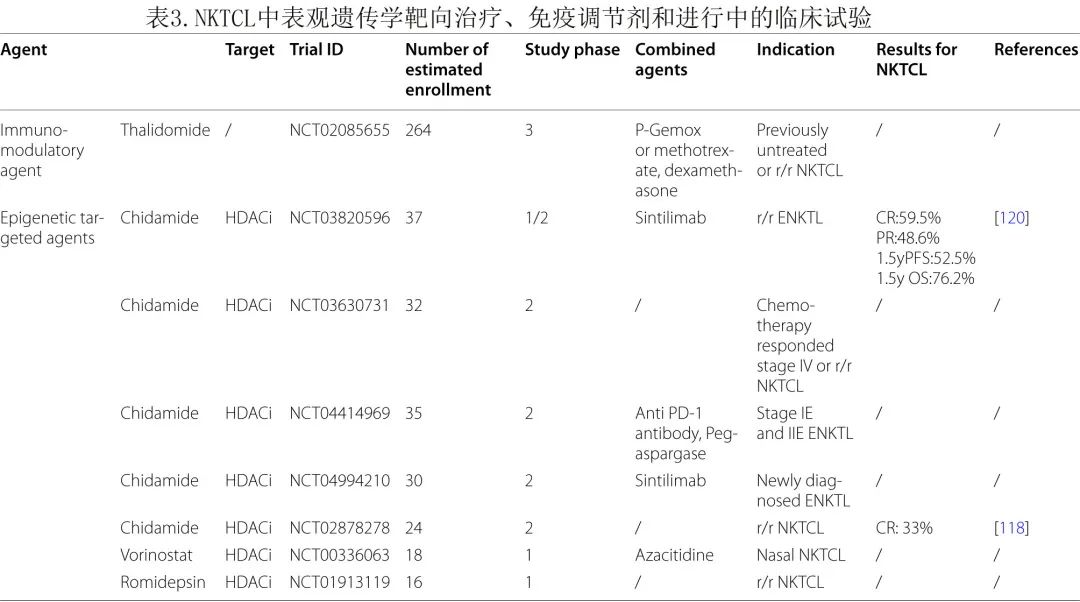
沙利度胺和来那度胺均有小样本研究证实其适度疗效。一项3期试验(NCT02085655)正在进行中,比较P-GemOx联合沙利度胺与AspaMetDex (培门冬酶、甲氨蝶呤、地塞米松)在初治或r/r NKTCL中的疗效(表3)。
CART细胞疗法
CART疗法在NKTCL的使用有限。靶向B7-H3的CAR-T细胞处于临床前研究中,目前正在CD30阳性NHL患者(NCT04526834, NCT03049449, NCT04288726)中开展CD30 CART的几项试验。由于NKTCL与EBV感染密切相关,LMP1可能是CART治疗NKTCL的另一个靶点。
信号通路抑制剂
基因组表达谱(GEP)揭示了NKTCL发病机制的多种机制,并具有开发个体化治疗策略的潜力。图2概述了NKTCL发病机制的六个主要标志特征及相应的靶向治疗。
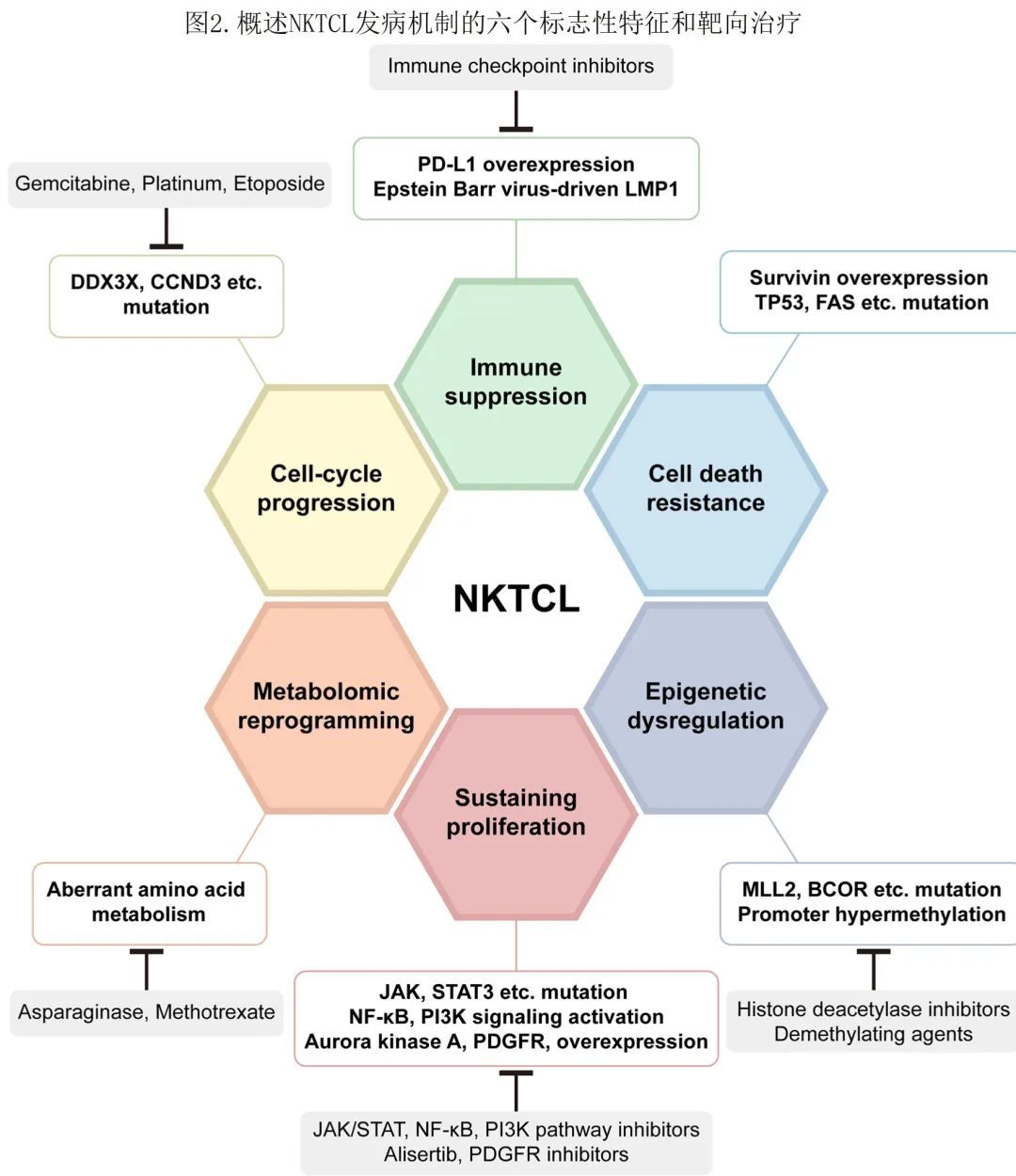
相关信号通路包括JAK/STAT、VEGF、PDGFR、PI3K/Akt/mTOR通路和NF-κB通路(图3)。
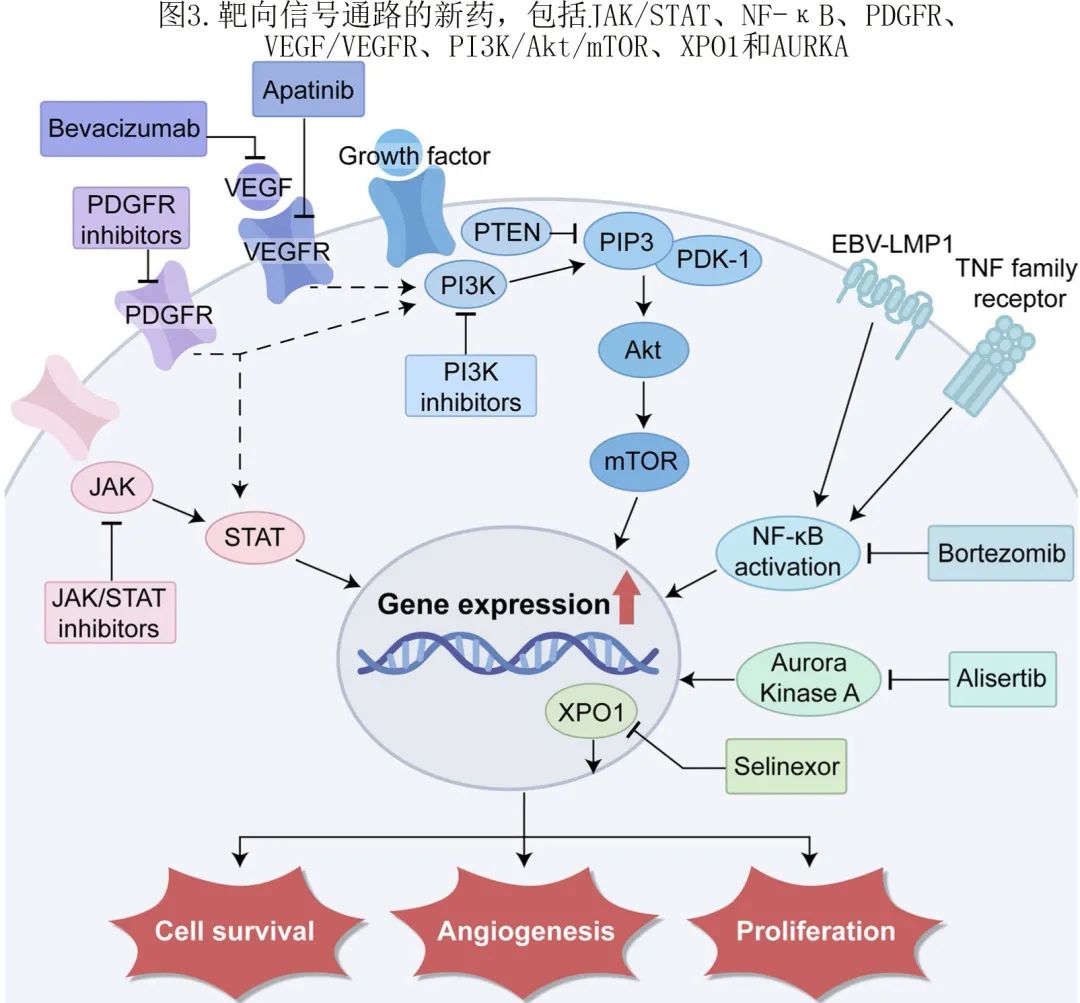
此外,2020年Xiong等在NKTCL中鉴定出三种分子亚型(TSIM、MB和HEA),TSIM和HEA亚型分别参与JAK/STAT和NF-κB通路的激活,并且这些分子亚型对不同的靶向治疗敏感。
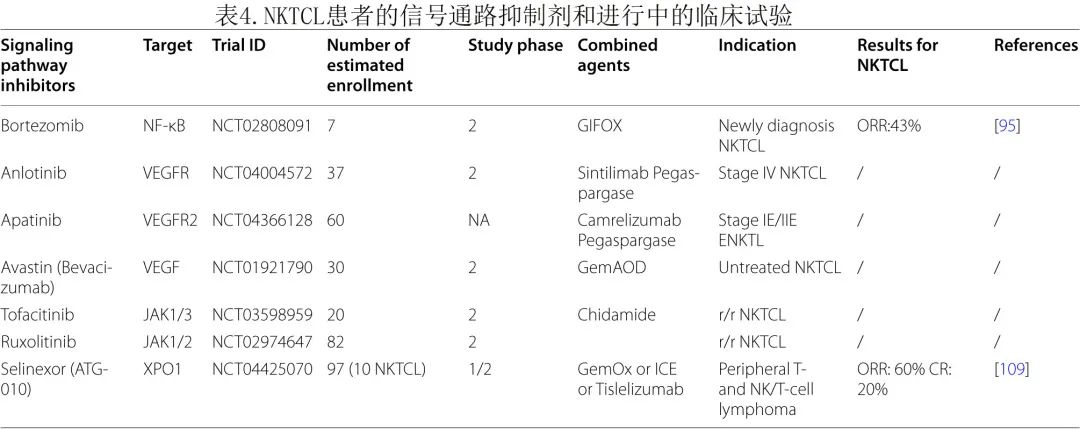
潜在的NKTCL信号通路抑制剂见表4,包括JAK/STAT通路抑制剂(JAK抑制剂托法替尼和芦可替尼治疗r/r NKTCL的研究正在开展;golidocitinib治疗NKTCL患者2/3例获得总体缓解)、NF‑κB信号通路(硼替佐米联合GIFOX的ORR为43%)、VEGF/VEGFR抑制剂(贝伐珠单抗联合化疗的研究正在开展,VEGFR抑制剂阿帕替尼和安罗替尼也在评估中)、PDGFR抑制剂(开发NKTCL新疗法有希望的靶点,但目前尚无相关试验)、XPO1抑制剂(塞利尼索联合GemOx的1b期研究最新结果表明,10例NKTCL中ORR为60%、CR为20%)、极光激酶A抑制剂(Aurora kinase A inhibitors,AURKA抑制剂;目前还没有AURKA靶向药物治疗NKTCL的试验)。
表观遗传学靶向药物
多种实体瘤和血液系统恶性肿瘤存在表观遗传学失调。BCL-6协同抑制因子(BCOR)和混合谱系白血病2 (MLL2)的突变和异常表达模式与NKTCL有关。基于表观遗传学的NKTCL治疗方法见表3。
西达本胺治疗r/r NKTCL,中位随访3.7个月时33%达到CR,且所有达到CR的患者保持无病状态>6个月。在一项纳入37例晚期NKTCL患者的非随机研究中,19例接受西达本胺联合化疗的患者的ORR为40%,而其余18例接受西达本胺单药治疗患者的ORR为15%。在一项针对r/r NKTCL患者的1b/2期单臂研究中,西达本胺联合信迪力单抗的ORR为59.5%,CR为48.6%,18个月PFS为52.5%,18个月OS为76.2%。西达本胺联合其他药物治疗NKTCL的多项研究正在进行中。
口服非选择性HDAC抑制剂Panobinostat联合硼替佐米治疗r/r NKTCL,1/2例患者获得PR。但抑制HDAC可触发EBV再激活,使用罗米地辛(HDAC抑制剂)已报道可引起EBV再激活,因此在使用HDACi治疗时,必须仔细考虑EBV再激活的风险,未来使用抗EBV药物联合HDAC抑制剂的策略可以进一步探索。表3总结了进行中的HDAC抑制剂治疗NKTCL患者的试验。
全局启动子甲基化分析显示,在NKTCL细胞系和患者样本中,许多肿瘤抑制基因(包括BCL2L11 (BIM)、DAPK1和TET2)的启动子都出现了超甲基化;地西他滨治疗可诱导甲基化基因的重新表达,提示去甲基化药物可能具有治疗作用。
总结
以天冬酰胺酶为基础的化疗改善了局部NKTCL患者的生存,但晚期NKTCL仍有重大挑战,超过70%的患者会在诊断后5年内进展。针对r/r NKTCL已经开发了多种新药(图4)。

在这些新型治疗方法中,免疫疗法(ICI、细胞表面靶向抗体和EBV特异性CTL)已显示出有希望的结果,但信号通路抑制剂和表观遗传学靶向药物的证据目前有限,信号通路抑制剂和表观遗传学靶向药物作为单药治疗r/r NKTCL可能无法达到令人满意的疗效。ICI、细胞表面靶向抗体和含蒽环类化疗的联合策略可能有助于提高r/r NKTCL的治疗效果,并具有未来发展的潜力。相关领域其他主要障碍包括可用于临床试验的患者数量有限,以及不同患者的基因突变有差异。
参考文献
Tian, XP., Cao, Y., Cai, J. et al. Novel target and treatment agents for natural killer/T-cell lymphoma. J Hematol Oncol 16, 78 (2023). https://doi.org/10.1186/s13045-023-01483-9
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言