J Biol Chem:利用生物化学和生物物理学来消除前列腺癌中的雄激素受体信号
2021-01-15 AlexYang MedSci原创
去势抵抗性前列腺癌(CRPC)由雄激素受体(AR)持续驱动。使用最先进的生物物理和生物化学技术可以推进对CRPC中AR信号的抑制。
去势抵抗性前列腺癌(CRPC)由雄激素受体(AR)持续驱动。使用最先进的生物物理和生物化学技术可以推进对CRPC中AR信号的抑制。

通过低温电子显微镜对AR及其复合物的结构表征将推进N端域(NTD)和配体结合域(LBD)拮抗剂的开发。AR功能的结构基础不太可能由任何单一的结构决定,由于其NTD的内在无序性,它不仅与核心调控因子相互作用,而且很可能是AR剪接变体(SV)的构成性活性的原因,而这些变体缺乏LBD,并在CRPC中出现。使用缺乏LBD的不同AR结构体,通过探究它们对蛋白质折叠、DNA结合和转录活性的影响可以揭示域间耦合,从而解释AR-SVs的活性。AR还与促进染色质成环的共调节因子相互作用,阐明其中的机制可以发现治疗CRPC的漏洞,而这些漏洞不涉及靶向AR。CDK7对AR共激活物MED-1的磷酸化可以通过使用CDK7抑制剂来阻断。另外,CRPC能够获得对AR信号抑制剂(ARSI)的耐药性。耐药性可能涉及AR-SVs,但其作用需要在疾病进展过程中通过SILAC-质谱法对其进行可靠的定量。ARSI耐药也可通过AKR1C3(5型17β-羟类固醇脱氢酶)催化的瘤内雄激素生物合成发生,其独特之处在于其作为AR的共激活剂。
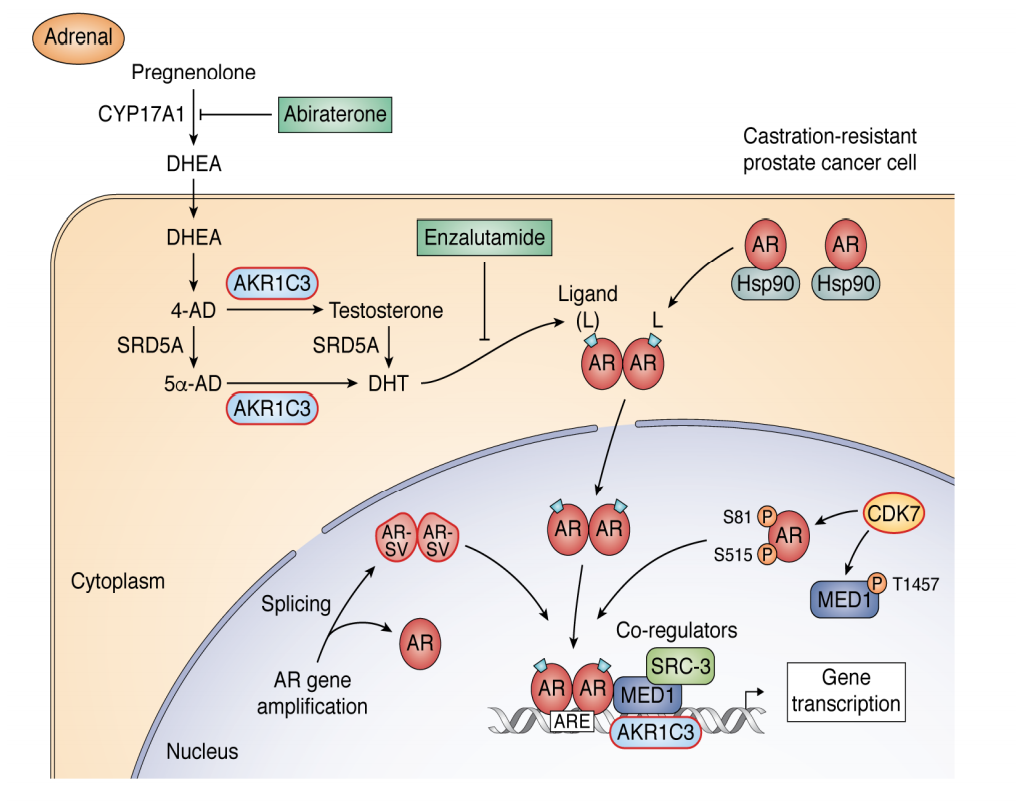
AR信号途径在前列腺癌和CRPC靶标中的核心作用
最后,研究人员指出,可以利用反向胶束核磁共振和基于片段的药物发现来开发新的双功能抑制剂,即竞争性地抑制AKR1C3并阻断其共激活功能。
原始出处:
Irfan A Asangani, Ian Blair, Gregory Van Duyne et al. Using Biochemistry and Biophysics to Extinguish Androgen Receptor Signalling in Prostate Cancer. J Biol Chem. Dec 2020
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#Biol#
82
#物理学#
84
#生物物理学#
77
#Bio#
78
#雄激素受体#
84
#前列腺癌#
196
前列腺癌相关研究,学习了,谢谢梅斯
112