Biomaterials:华西医院揭示Mo2C纳米酶治疗纤维肌痛能量代谢分子机制
2022-10-17 四川大学华西医院 四川大学华西医院
首次发现Mo2C纳米酶对利血平诱导产生的纤维肌痛具有治疗作用,并首次借助综合代谢组学技术揭示了纤维肌痛治疗过程中的能量代谢分子机制。
华西医院疾病系统遗传研究院/疾病分子网络前沿科学中心/蛋白组学-代谢组学平台龚萌副研究员团队与麻醉手术中心/线粒体与代谢研究室李涛研究员团队合作,于2022年7月在Biomaterials(IF:15.304)发表文章“Integrated metabolomics revealed the fibromyalgia-alleviation effect of Mo2C nanozyme through regulated homeostasis of oxidative stress and energy metabolism”,首次发现Mo2C纳米酶对利血平诱导产生的纤维肌痛具有治疗作用,并首次借助综合代谢组学技术揭示了纤维肌痛治疗过程中的能量代谢分子机制。该研究认为Mo2C纳米酶具有作为纤维肌痛治疗药物的潜力,为纤维肌痛的临床治疗提供了新思路。

蛋白组学-代谢组学平台张定坤助理研究员、线粒体与代谢研究室博士蒋玲为共同第一作者,蛋白组学-代谢组学平台龚萌副研究员、线粒体与代谢研究室李涛研究员为共同通讯作者。该研究工作得到了疼痛科肖红教授和疾病系统遗传研究院沈百荣教授的指导。
纤维肌痛(FM)是慢性肌肉和骨骼疼痛的最常见原因,目前在人群中发生概率呈逐年增长趋势。FM与疲劳、焦虑、抑郁、睡眠障碍和认知功能障碍等因素有关,FM患者的生活质量显著下降,精神状态也受到很大影响。自1990年美国风湿病学会制定了第一个FM诊断标准以来,FM被认为是一种广泛存在的慢性疼痛。目前FM几乎影响了世界上5%的人口,且大多数有FM引发的一系列症状。FM内源性和外源性因素的存在与相互作用使其成为一种非常复杂的疾病。然而,尚缺乏FM的新型治疗方法且基于分子水平的详细机制仍不清楚。
研究发现Mo2C纳米酶在小鼠模型中表现出对利血平诱导产生的FM的治疗作用;同时,对该FM模型样品进行了基于气相色谱-质谱和液相色谱-串联质谱的综合代谢组学研究,揭示了治疗过程中的能量代谢分子机制。
研究发现Mo2C纳米酶可以模拟超氧化物歧化酶(SOD)、谷胱甘肽氧化酶(GPx)和过氧化氢酶(CAT)去除血浆中过量的活性氧簇(ROS),并有效促进FM模型中与能量代谢相关的代谢,包括糖酵解、柠檬酸循环、磷酸戊糖途径、脂肪酸生物合成和代谢以及脂质生物合成和代谢,同时该效应也是Mo2C纳米酶抑制氧化应激和线粒体功能障碍的一个重要因素。经Mo2C纳米酶治疗后,FM小鼠模型的多项生理指标在行为学、组织学和形态学水平上也达到了与正常小鼠相似的稳态。综合代谢组学研究结果也表明,Mo2C引起的代谢改变主要表现在氨基酸、有机酸、脂肪酸、磷脂、溶血磷脂和甘油脂水平的变化,而Mo2C优良的生物活性在治疗FM过程中起着至关重要的作用。
研究进一步认为Mo2C纳米酶治疗FM的过程可分为以下几步:(1)Mo2C在血液输送过程中催化清除血浆中过量的ROS;(2)Mo2C促进腓肠肌从ROS诱导的损伤和氧化应激中恢复;(3)保护细胞膜以降低促炎细胞因子的水平;(4)抑制线粒体损伤;(5)恢复体内代谢稳态。
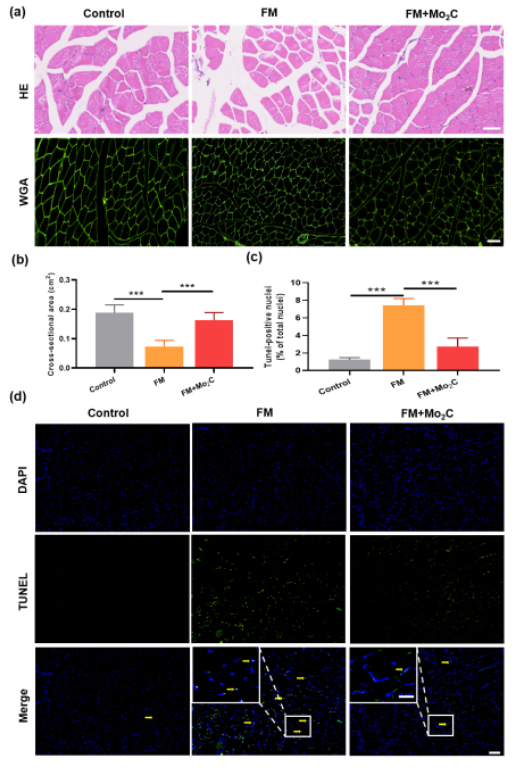
Mo2C纳米酶治疗FM的组织学与病理学研究
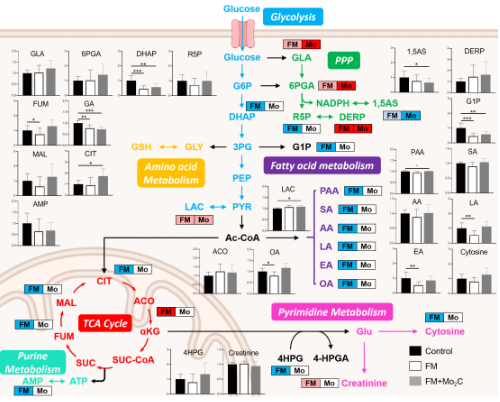
Mo2C纳米酶治疗FM的水溶性代谢组学研究
基于上述结果,研究认为Mo2C纳米酶具有作为FM治疗药物的潜力,其有效清除生物体内ROS以维持体内的正常代谢稳态可能是关键机制之一。虽然研究存在Mo2C纳米酶难以从动物血管中清除的局限,但基于研究结果,可利用Mo2C纳米酶在体外去除血液制品中的ROS或开发可生物降解的纳米酶,以减少可能产生的不良反应。
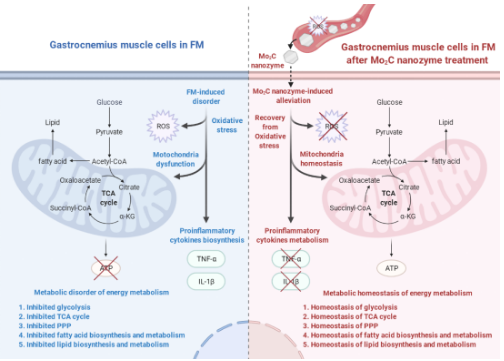
Mo2C纳米酶治疗FM的分子机制
本研究利用综合代谢组学技术揭示了Mo2C纳米酶治疗FM过程中的能量代谢分子机制,是拓展Mo2C纳米酶生物医学应用领域的重要尝试,而Mo2C纳米酶对FM的治疗机制也为FM的临床治疗提供了新的思路。
原文链接:https://www.sciencedirect.com/science/article/abs/pii/S0142961222003180
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言