肿瘤耐药怎么破?恒定自然杀伤T(iNKT)细胞解决胃癌患者耐药问题,刺激T细胞扩增24倍,抑制肿瘤发展!
2024-11-23 《基因启明》公众号 《基因启明》公众号 发表于上海
一项针对iNKT细胞异体移植的临床试验正在紧锣密鼓的开展。这项研究的目的是为了探究来自健康捐赠者的异体iNKT细胞是否能够克服癌症患者的免疫治疗耐药问题。
亮点
1、iNKT细胞疗法克服了免疫治疗耐药问题,患者在治疗期间无严重免疫不良反应发生。
2、iNKT细胞疗法使得患者体内少数预先存在的T细胞克隆从初始的2%扩增到48%,足足增加了24倍。患者淋巴细胞免疫浸润、激活和TH-1极化相关基因表达均大幅度增加。
3、在接受iNKT细胞疗法1个月后,令人惊喜的是,结果显示胃壁增厚稳定,网膜结节间隔缩小;3个月、6个月和9个月(分别为6个周期、12个周期和18个周期)的CT扫描显示,网膜结节进一步缩小。
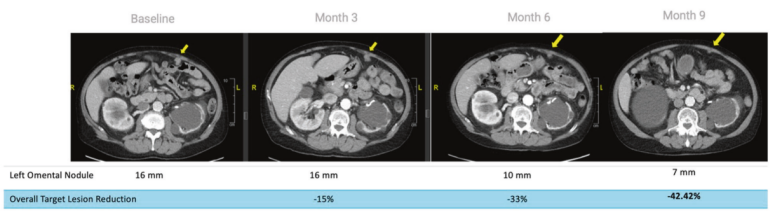
基线、3个月、6个月和 9个月时网膜肿瘤结节(黄色箭头)
胃癌是全球第五大恶性肿瘤,但仅有36%的转移性疾病患者能够存活5年以上。靶向程序性细胞死亡蛋白1(programmed cell death protein 1,PD-1)和程序性死亡配体1(programmed cell death 1 ligand 1,PD-L1)的免疫检查点抑制剂(immune checkpoint inhibitors,ICIs)出现,为胃癌的临床治疗提供了新的策略,但只有10-30%的患者能够在ICI的治疗中获益,尤其抗肿瘤免疫力低下或缺乏抗肿瘤免疫力的癌症患者对ICI的治疗反应欠佳。因此,需要寻找新的免疫治疗方法来克服这一问题。
恒定自然杀伤T(invariant natural killer T,iNKT)细胞在胸腺中发育,聚集在肝脏中,其次分布在脾、骨髓、淋巴结、皮肤粘膜和外周血等其他部位。在外周血中,iNKT细胞约占循环T细胞0.01-0.1%。尽管iNKT细胞数量稀少、来源有限,但由于其共同表达T细胞和NK细胞的典型表面受体,因而发挥着多种抗肿瘤效应。
近期,一项题为Overcoming resistance to programmed cell death protein 1(PD-1) blockade with allogeneic invariant natural killer T-cells (iNKT)的临床研究发现,iNKT细胞可以作为一种新疗法来克服胃癌免疫治疗的耐药问题,iNKT细胞疗法促使患者体内T细胞扩增24倍,同时激活淋巴细胞免疫浸润和激活,抑制肿瘤发展。这项研究为开发新的胃癌免疫疗法提供了新思路,有望在未来为胃癌患者提供更好的治疗选择。

此研究对象为一名73岁男性患者。在常规随访中,该患者被发现患有缺铁性贫血,内窥镜检查显示胃小弯处有一个巨大、溃疡性、非环状肿块;活检显示为中度分化、HER-2阴性腺癌(HER-2为胃癌主要靶点,在胃癌细胞扩增的比例约为 4%~44%);胸部/腹部/盆腔计算机断层扫描(CT)显示,胃底肿块为异质、溃疡和部分坏死,与内窥镜检查时发现的肿块一致,并伴有腹膜癌肿。最终,该患者被确诊为微卫星高度不稳定(MSI-H)晚期胃腺癌。
注:微卫星是短DNA序列的串联重复序列,在肿瘤的基因组中,微卫星存在小的基因突变,导致其不稳定,称为微卫星不稳定性(MSI)。MSI共分为高度不稳定(MSI-H)、低度不稳定(MSI-L)和稳定(MS-S)。
于是,医生对该患者设计了一系列的治疗方案。首先,患者接受了4个周期的Pembrolizumab(一种抗PD-1单克隆抗体)治疗,不巧的是,治疗后CT 扫描显示其腹膜结节增大,内镜检查(胃肠造影)显示之前已发现的胃肿块进展和增大,并伴有出血。鉴于此,患者方案改为Nivolumab(一种阻断PD-1和其配体相互作用的单克隆抗体)联合亚叶酸、5-氟尿嘧啶和奥沙利铂(FOLFOX)治疗,然而22个疗程(17个月)后,CT 扫描显示近端胃壁增厚情况恶化,邻近的网膜结节也有所进展,肿大结节的活检证实为中度分化腺癌。
由此看来,传统的药物治疗已经无法将癌症“扼杀”,难道说该患者真的无药可医了吗?就在众人焦头烂额之际,转机悄然而至……
一项针对iNKT细胞异体移植的临床试验正在紧锣密鼓的开展。这项研究的目的是为了探究来自健康捐赠者的异体iNKT细胞是否能够克服癌症患者的免疫治疗耐药问题。
该患者随即接受了一次 iNKT细胞输注(剂量为4.3 ×106个细胞/千克),并继续接受 Nivolumab维持治疗(剂量200 毫克,每14 天一次)。1个月后对其进行CT 扫描,令人惊喜的是,结果显示胃壁增厚稳定,网膜结节间隔缩小;3个月、6个月和9个月(分别为6个周期、12个周期和18个周期)的CT扫描显示,网膜结节进一步缩小。
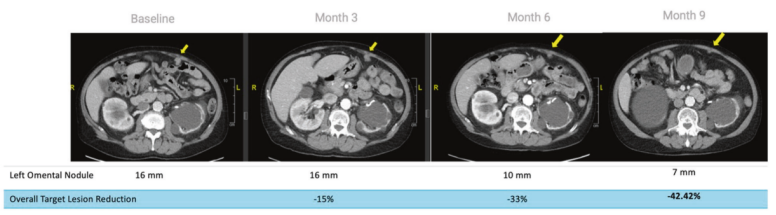
基线、3个月、6个月和 9个月时网膜肿瘤结节(黄色箭头)
此外,研究人员还对这名患者在基线和治疗第15天的肿瘤活检标本进行了全外显子组测序(WES),进一步证实了他的确患有MSI-H型肿瘤,其肿瘤突变负荷甚至高达84 mut/MB。
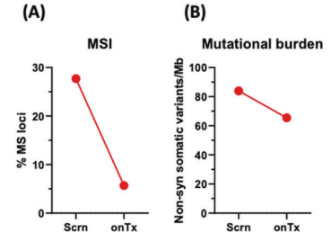
患者患有MSIH型肿瘤及肿瘤突变负荷
那么,注射iNKT细胞治疗是否真的能够产生效果呢?
有趣的是,研究人员发现在iNKT细胞治疗后,患者体内少数预先存在的T细胞克隆从初始的2%扩增到48%,足足增加了24倍。自动图像分析显示,在iNKT细胞治疗后,CD8+ T细胞广泛浸润到肿瘤中;细胞增殖标记物也表明T细胞在肿瘤内大量扩增。
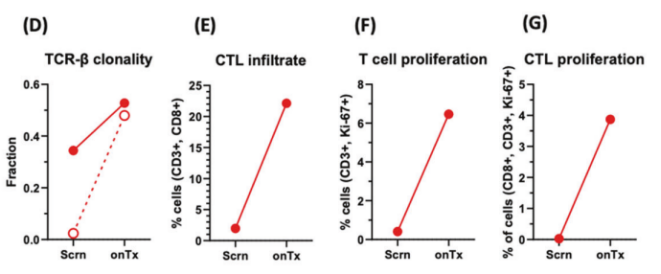
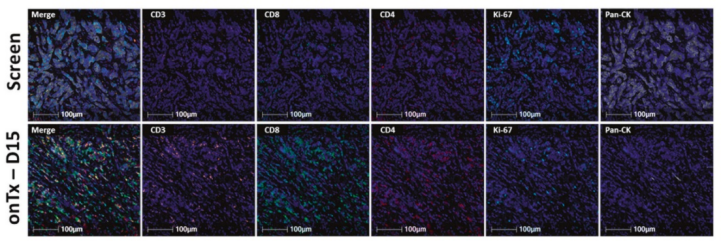
iNKT细胞治疗下T细胞大量扩增
为慎重起见,研究人员还对患者的基线和治疗第15天的肿瘤活检基因表达进行了分析,结果显示,注射iNKT细胞后,免疫浸润、激活和TH-1极化相关基因表达均大幅度增加,表明iNKT细胞治疗在极大程度上克服了患者对PD-1疗法的耐药性,协助了淋巴细胞的抗肿瘤功能。
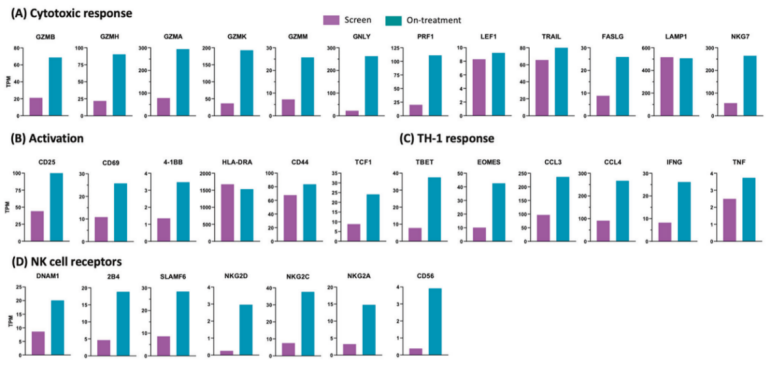
肿瘤活检的RNAseq基因表达分析
值得一提的是,尽管在使用Nivolumab治疗期间,患者出现了2级皮疹,但在使用局部类固醇治疗后皮疹有所好转。除此之外,患者未出现任何其他免疫相关不良反应。
综上,该研究展示了iNKT细胞可以作为一种新的免疫治疗方法来克服胃癌免疫治疗耐药问题。相信在不远的未来,iNKT细胞疗法能为胃癌患者提供更好的治疗选择。
来源:
微信公众号: 基因启明
参考文献:
Hadfield MJ, Safran H, Purbhoo MA, Grossman JE, Buell JS, Carneiro BA. Overcoming resistance to programmed cell death protein 1 (PD-1) blockade with allogeneic invariant natural killer T-cells (iNKT). Oncogene. 2024 Mar;43(10):758-762. doi: 10.1038/s41388-024-02948-y. Epub 2024 Jan 29. PMID: 38281989.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#胃癌# #iNKT细胞#
19