病例报道|以腹水为首发表现的肝淀粉样变性
2020-07-28 消化界 消化界
淀粉样变性为引起腹水的罕见病因,可累及多器官,临床表现多样,预后差,易被漏诊。本例患者以腹水为首发表现,经多学科协作诊治后,最终确诊为肝淀粉样变性所致的肝窦阻塞综合征。消化科医师应重视腹水罕见病因的诊
摘要
淀粉样变性为引起腹水的罕见病因,可累及多器官,临床表现多样,预后差,易被漏诊。本例患者以腹水为首发表现,经多学科协作诊治后,最终确诊为肝淀粉样变性所致的肝窦阻塞综合征。消化科医师应重视腹水罕见病因的诊断和治疗,临床工作中不能忽视少见病因如淀粉样变性引起腹水的可能性,必要时需行肝穿刺检查明确病理诊断。
腹水是指腹腔内游离液体的过量积聚,是临床较常见症状之一。引起腹水的常见原因主要有肝脏疾病、心力衰竭、营养障碍、结缔组织病和恶性肿瘤腹膜转移等,其中以肝脏疾病最常见。但仍有部分患者的腹水病因复杂多样,由一些少见疾病引起,在临床工作中需考虑少见疾病引起腹水的可能性。现介绍1例以腹水为首发表现的肝淀粉样变性病例。
病例介绍
患者男,73岁,因 “腹胀1个月余,伴双下肢水肿、少尿2周” 于2019年7月26日入住上海交通大学医学院附属瑞金医院消化内科。
患者1个月余前无明显诱因出现腹部饱胀不适,进食后明显,伴乏力、食欲减退,后逐渐加重,伴腹泻,为黄色黏液便,4~6次/d,无腹痛、恶心呕吐和发热。肿瘤标志物糖类抗原50为397.88 U/mL,癌胚抗原为9.08 μg/L,CA19-9为219.3 U/mL。正电子发射计算机断层显像检查示腹盆腔积液、脂肪肝、肝多发囊肿、双肾囊肿,双侧髂骨良性改变,全身未见骨代谢异常增高灶。患者近2周症状逐渐加重,出现双下肢水肿,尿量偏少,伴明显乏力,活动耐量下降。近半年来体质量下降10 kg。
患者8年前因粪便中带血丝曾行肠镜检查,结果显示直肠至横结肠可见连续弥漫的糜烂和浅溃疡,表面覆脓苔,黏膜充血明显,病理检查示慢性结肠炎,诊断为中度溃疡性结肠炎(UC)。予柳氮磺吡啶治疗,腹泻和便血缓解,后改为美沙拉秦维持治疗。患者每半年至1年复查1次肠镜,均提示活动性UC。2018年6月6日末次肠镜检查示直肠-降结肠炎,横结肠-回盲部可见黑色点状物质(图1)。病理检查提示黏膜慢性炎。患者40年前曾有消化性溃疡出血史,13年前有背部脂肪瘤手术史。否认肝炎、结核等传染病史。既往有长期吸烟史,已戒烟14年。
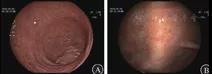
图1. 2018年6月6日肠镜检查结果
A 直肠-降结肠炎症改变 B 横结肠-回盲部可见黑色点状物质
1.临床检查
入院体格检查示体温为36.4 ℃,脉搏为78次/min,呼吸频率为20次/min,血压为95/51 mmHg(1 mmHg=0.133 kPa)。神志清楚,皮肤巩膜黄染,浅表淋巴结未触及,未见肝掌和蜘蛛痣。两肺呼吸音粗,未闻及干湿啰音,心律齐,心脏各瓣膜听诊区未闻及病理性杂音。腹软,稍膨隆,肠鸣音为4次/min,未见腹壁静脉曲张,未见胃型、肠型,全腹软,无压痛、反跳痛,肝脾肋下未及,移动性浊音为阳性。双下肢轻度凹陷性水肿。
血常规示血红蛋白水平为93 g/L,血细胞比容为0.276,平均红细胞体积为97.4 fL,平均血红蛋白水平为32.8 pg。
尿蛋白(+),尿隐血阴性,24 h蛋白尿651 mg(尿量1 L)。
肝功能检查示ALT水平为26 U/L,AST水平为50 U/L,ALP水平为310 U/L,GGT水平为303 U/L,TBil水平为71 μmol/L,DBil水平为39.3 μmol/L,总蛋白水平为51 g/L,白蛋白水平为23 g/L。
肝炎病毒和自身免疫性肝炎相关的抗体等指标均未见明显异常。肾功能检查示血肌酐水平为124 μmol/L。心功能检查示B型钠尿肽前体为883.4 ng/L。
血清免疫固定电泳结果显示免疫球蛋白(immunoglobulin,Ig)G、IgA、IgM,以及Ig轻链κ、轻链λ均为阴性。自身免疫抗体提示抗小核糖核蛋白抗体(±),抗核抗体、抗双链DNA、抗线粒体抗体、肝肾微粒体抗体、肝胞质溶胶抗体、可溶性肝抗原抗体均为阴性。溶血性贫血和阵发性睡眠性血红蛋白尿的实验室检查均未见异常。
腹水生物化学检测示总蛋白水平为16 g/L,白蛋白水平为7 g/L,LDH水平为93 U/L,血清-腹水白蛋白梯度(serum ascites albumin gradient,SAAG)为16 g/L。
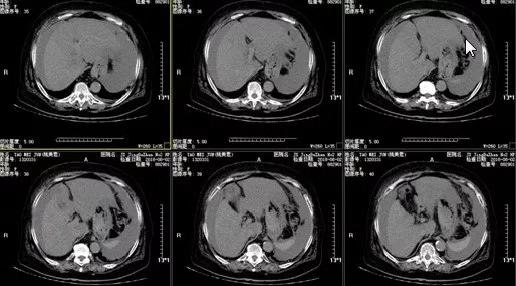
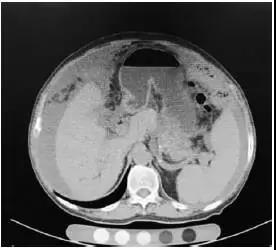
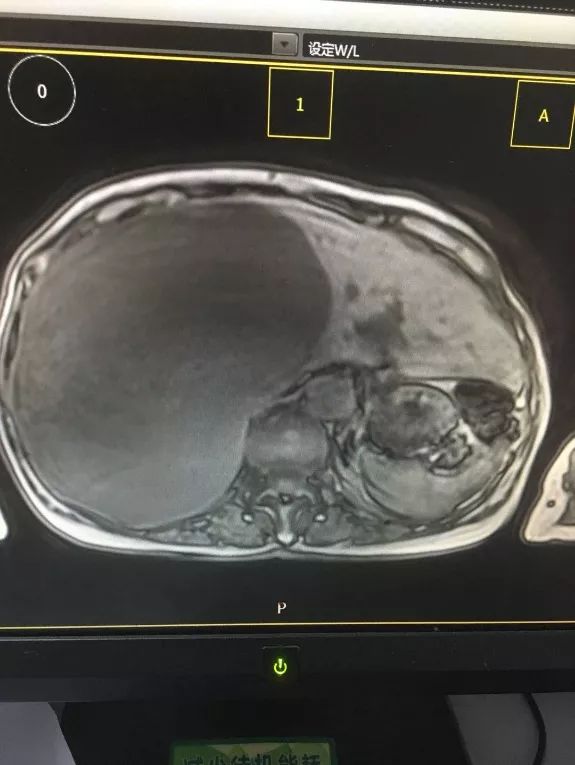
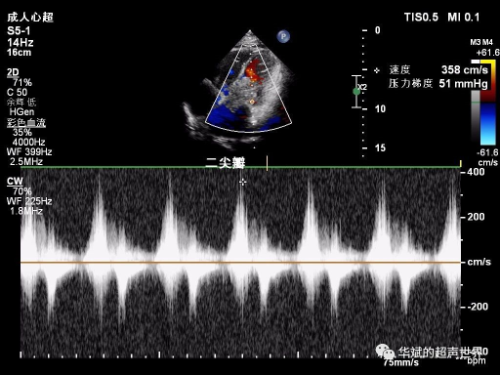
心脏超声检查示左心房增大伴轻度二尖瓣关闭不全,右心房增大。胸部CT检查示慢性支气管炎合并肺气肿伴散在小结节影,双侧胸膜增厚粘连,心包积液。胸腹部超声检查示双侧胸腔积液,腹腔大量积液。腹部CT平扫检查示肝脏饱满、肿大,实质内见多发类圆形低密度影(图2),腹部增强CT检查示腹水、盆腔积液,肝脏稍肿大、强化不均(图3),肝囊肿,胆囊结石,胆囊炎。磁共振胰胆管成像(magnetic resonance cholangiopancreatography,MRCP)示肝总管和胆总管局部显示不清,左肝内胆管稍扩张。

图2. 腹部计算机断层扫描平扫可见肝脏饱满、肿大,实质内见多发类圆形低密度影
图3. 腹部计算机断层增强扫描示肝实质强化不均
2.临床诊断
腹腔积液(待查)、黄疸、肝囊肿、肾囊肿、中度UC。
3.临床治疗
腹腔积液病理检查提示有漏出液,患者需行腹部增强CT检查明确有无肝脏病变,考虑到入院时存在肾功能不全,遂在增强CT检查前后静脉滴注0.9%氯化钠溶液和碳酸氢钠溶液进行充分的血液水化和尿液碱化,促进造影剂的排泄,避免肾功能恶化。
患者曾服用过中药,但未发现所服用中药中存在导致药物性肝损伤的成分。因患者存在不明原因的肝损伤,结合腹水实验室检查考虑为肝源性,于2019年8月1日行CT引导下肝穿刺活组织检查(以下简称活检)。
在等待病理结果的过程中,患者先后出现血肌酐进行性升高、少尿、氧饱和度进行性下降、B型钠尿肽前体进行性升高,胸部CT检查示肺部炎症浸润。治疗上予心电图监护,特利加压素调整血流分布,先后运用头孢曲松、美罗培南、万古霉素、利奈唑胺等抗感染治疗,剂量根据肾功能情况不断调整,此外,给予吸氧,二羟丙茶碱注射液、特布他林、布地奈德解痉平喘,静脉滴注丁二磺酸腺苷蛋氨酸(1.0 g/次,1次/d)和口服熊去氧胆酸(0.25 g/次,3次/d)保肝利胆,输注1 U红细胞和200 mL血浆,维持电解质平衡,纠正低蛋白血症和低纤维蛋白原血症,腹腔穿刺引流减轻腹内压。
经积极治疗后,肾功能有一过性改善,血肌酐水平由387 μmol/L逐渐降至167 μmol/L,24 h尿量由500 mL逐渐恢复至1 500 mL。但患者入院第19天开始出现肝功能、心功能、凝血功能进行性衰竭,同时肾功能再次出现恶化。期间出现黏液血便(5次/d),粪便隐血试验(++++),考虑UC急性发作。因存在难以控制的感染,故仅口服美沙拉秦(1 g/次,4次/d)控制肠道炎症。
2019年8月11日肝脏穿刺病理检查结果显示肝窦阻塞综合征,肝组织广泛淀粉样变性,刚果红染色(+)(图4、图5)。因患者为淀粉样变性,病情复杂危重且合并多脏器衰竭,故仅予对症支持治疗。
2019年8月26日患者出现呼吸急促,氧饱和度进行性下降,室性逸搏,心室颤动,血压过低测不出,瞳孔散大且固定,对光反射消失,行胸外按压等积极抢救治疗无效,患者死亡。
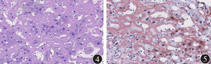
图4. 光学显微镜下见大量粉红色无定型物质和肝窦扩张 苏木精-伊红染色 低倍放大
图5. 光学显微镜下见红色的淀粉样物质 刚果红染色 低倍放大
病例讨论
感染科陈立畅住院医师:患者以"腹水待查"入院,引起腹水的常见原因有肝脏疾病、心血管疾病、肾脏疾病、营养障碍、结缔组织病和恶性肿瘤腹膜转移等,其中以肝硬化最常见。我国肝硬化最常见的病因为慢性乙型肝炎,其他较常见的病因包括慢性丙型肝炎、自身免疫性肝炎、原发性胆汁性肝硬化等。该患者入院后完善了腹水常见病因的检查,但均未发现异常,此时需考虑少见疾病引起的腹水。淀粉样变性可累及多个器官,该患者先后出现肾衰竭、肝功能衰竭、呼吸衰竭和心力衰竭,可能为淀粉样变性沉积至相应器官所致的功能障碍。
放射科赵雪松主治医师:患者入院时腹部CT检查可见肝脏肿大,强化不均,存在肝窦阻塞综合征可能。肝窦阻塞综合征常见于造血干细胞移植后,或服用含有吡咯生物碱的中药,少数发生于化学治疗或大剂量放射治疗后。我国常见的病因是服用含吡咯生物碱的中药制剂,其中以土三七最多见,故需仔细询问患者有无相关中药服用史。部分UC患者会出现胆汁性肝硬化,以乏力、黄疸和ALP升高为特点,MRCP典型特征为"串珠样"改变。
该患者有UC病史,存在乏力、黄疸和ALP升高,故需行MRCP明确胆道情况。肝窦阻塞综合征典型的CT表现为肝脏弥漫性肿大,平扫显示肝实质密度不均匀减低;静脉期和平衡期肝实质呈特征性 “地图状”、“花斑样”不均匀强化。肝淀粉样变性CT的典型表现为肝脏弥漫性肿大,可见弥漫性或局灶性的肝实质衰减值降低,伴或不伴广泛性钙化。该患者腹部增强CT检查结果提示肝脏饱满、稍肿大,实质见多发类圆形低密度影,肝实质强化不均,结合患者病史和病理诊断,符合肝窦阻塞综合征的典型表现和肝淀粉样变性的影像学表现。
放射介入科吴志远主任医师:患者肝功能异常以TBil升高为主,无病毒性肝炎和自身免疫性肝炎,也排除了相关中药所致肝损伤的病因,腹部增强CT检查示肝窦阻塞综合征可能,故需积极行肝穿刺,明确患者肝损伤的原因。但患者行肝穿刺有较大风险,一方面患者存在急性肾衰竭,增强CT检查会导致肾功能进一步恶化,无法行增强CT检查引导下的肝穿刺明确肝内血管情况,而行平扫CT引导下的穿刺又可能导致局部大出血、胆瘘等情况,严重时可危及生命;另一方面,梗阻性黄疸合并腹水为肝穿刺的相对禁忌证,此类患者容易形成胆瘘,以及胆瘘继发的腹膜炎,加重病情。
肾内科李娅主任医师:患者入院时出现少尿和急性肾衰竭等临床表现,存在严重低血压导致的肾脏灌注不足;予特利加压素以降低血肾素浓度,减少血管紧张素Ⅱ的生成,减轻肾血管收缩,增加肾脏血流量,患者肾功能出现好转,综合考虑肾衰竭为肾前性原因引起。需要适当补充血容量等对症支持治疗,改善患者肾脏灌注不足。
患者的肝穿刺病理结果示淀粉样变性,而淀粉样纤维蛋白是一种以不溶性纤维形式沉积的蛋白质,主要存在于器官和组织的细胞外,由于蛋白质折叠顺序发生改变,从而导致淀粉样变性。原发性淀粉样变性通常由各种浆细胞疾病引起;继发性淀粉样变性通常由各种炎症或慢性感染所致的急性期反应物血清淀粉样蛋白A的释放引起,而淀粉样蛋白A是淀粉样蛋白原纤维的前体。
淀粉样变性可累及全身多器官,其中以肾脏累及最常见,约70%的患者存在肾损伤和肾衰竭。肾脏受累时,常表现为蛋白尿和血尿,血清淀粉样蛋白A水平持续升高的患者最终会发展为肾衰竭。该患者表现为双下肢水肿、少尿、蛋白尿和急性肾衰竭,考虑可能是在肾淀粉样变性的基础上由血容量不足引发的肾前性急性肾衰竭。对于淀粉样物质沉积于肾小球引起的急性肾衰竭,可予以白蛋白扩容和白蛋白输注后对症支持治疗,同时可采用血液透析或肾脏移植以改善患者的长期预后。
感染科徐玉敏主任医师:患者入院时存在黄疸,多项肿瘤标志物水平升高,腹部CT增强扫描可见肝脏稍肿大,强化不均,建议完善肝脏增强MRI和MRCP检查,明确有无胆道和肝脏占位;如影像学检查未发现明显异常,可考虑肝穿刺病理活检。淀粉样变性累及肝脏时主要表现为乏力、腹胀、纳差等非特异性症状,常见体征为不明原因的肝肿大,实验室检查常见ALP升高,部分患者ALT、AST升高,当TBil升高时,患者生存期缩短。该患者表现为肝肿大,ALP、AST和TBil均升高,符合肝脏累及的典型特征。对于淀粉样变性累及肝脏的患者,治疗应予以保肝退黄等对症支持治疗,但大多数效果欠佳,必要时仍需进行肝脏移植。
风湿免疫科刘宏磊主治医师:患者入院时出现不明原因的腹水、双下肢水肿和心包积液,需排除累及全身系统的风湿性疾病。入院查抗核抗体阴性,仅抗小核糖核蛋白抗体(±),需进一步完善抗双链DNA、类风湿因子等检查明确有无风湿性疾病的依据。患者胸部CT检查示肺间质性渗出,若由感染引起,渗出常发生在肺的周围;若由风湿性疾病引起,渗出常发生在肺的中央部位。该患者肺的外周和中央均存在大量渗出,无自身免疫病的诊断证据,考虑为多种疾病共同引起,除了难以控制的肺部感染外,淀粉样变性引起的肺累及可能也参与了肺间质的渗出。
血液科许彭鹏副主任医师:患者入院时肝肾功能异常,伴轻度贫血,需进一步明确贫血的原因,必要时行骨髓穿刺排除少见疾病。该患者肝穿刺病理结果明确为淀粉样变性,原发性淀粉样变性由来源于Ig轻链片段的蛋白质发生沉积导致,是一种浆细胞病,95%以上的患者可在尿液或血清中检测出单克隆蛋白;继发性淀粉样变性可由多种疾病引起;遗传性淀粉样变性相对少见,但多数有明确的家族史和独特的临床特征,如遗传或散发性阿尔茨海默病。对于原发性淀粉样变性可以采用化学治疗,符合条件者可以采用自体干细胞移植。对于继发性淀粉样变性,治疗主要目的是控制原发病,减少淀粉样蛋白A。对于遗传性淀粉样变性,可考虑肝脏移植。对于合并器官衰竭的患者,可考虑血液透析和器官移植。
该患者IgG、IgA、IgM等未见异常,病理结果显示病情已恶化,建议进一步明确分型,但患者家属表示暂不考虑行进一步检查。患者病情恶化,肝、肾、心、肺多脏器功能衰竭,目前无法耐受化学治疗、自体干细胞移植,器官移植需肝肾联合移植,但预后极差。
病理科张之涵主治医师:淀粉样变性的确诊依靠活检,对单一器官受累的患者,建议取材部位为受累部位。淀粉样物质在光学显微镜下表现为粉红色,无定形透明物质,伴特征性"破裂"伪像;刚果红染色在偏振显微镜下呈绿色双折射,灵敏度和特异度分别为79%和80%;硫磺素T荧光染色表现为较强的黄绿色荧光。淀粉样变性亚型鉴定的首选方法为液相质谱分析,其次为免疫组织化学、免疫荧光等方法。该患者经过肝穿刺活检证实存在肝淀粉样变性,但确切分型仍需进一步检查。
消化内科姚玮艳副主任医师:腹水是临床常见症状之一,排除常见原因后,需考虑少见疾病,如感染性疾病(阿米巴病、蛔虫病、盆腔炎、沙门菌病等)、血液系统疾病(淀粉样变性、嗜血综合征、白血病、淋巴瘤、多发性骨髓瘤)、其他疾病(系统性红斑狼疮、异位妊娠、子宫内膜异位症)。对于新发腹水的患者,首先需要抽取腹水进行外观分析,检测SAAG、细胞计数、细胞分类计数、腹水细菌培养等明确腹水性质。其次需要根据腹水检查结果进行针对性的检查明确引起腹水的病因,如腹部超声、CT、MRI或MRCP等。若上述常规检查仍无法明确腹水病因,则需要根据已有的证据行腹膜活检、肝穿刺活检或骨髓穿刺等检查。
肝淀粉样变性患者在活检后有出血或肝脏破裂的风险,但尚未得到一致性证实,同时肝淀粉样变性的影像学没有特异性,诊断仍依赖组织活检。引起该患者腹水的主要原因为肝淀粉样变性,一方面患者SAAG为16 g/L(>11 g/L),存在门静脉高压;另一方面淀粉样物质沉积于门静脉周围的狄氏腔,长期压迫肝细胞和肝小静脉,导致肝窦内皮细胞肿胀、脱落、损伤,引起肝窦扩张充血和肝细胞萎缩,诱发门静脉高压,最终形成腹水;患者的低蛋白血症、蛋白尿和肝功能异常也可引起蛋白质合成障碍,形成腹水。
该患者虽最终确诊为肝淀粉样变性,但结合患者病史需要与以下疾病进行鉴别。首先是中药所致肝窦阻塞综合征,患者腹部增强CT检查示肝窦阻塞综合征表现,我国肝窦阻塞综合征常见病因为服用含吡咯生物碱的植物,其中以土三七最多见。该患者虽有中药服用史,但所服用的中药未见明确导致肝窦阻塞综合征的成分,且最终病理证实为淀粉样变性所致的肝窦阻塞综合征。
其次是UC合并硬化性胆管炎,该患者8年前明确诊断为UC,先后服用柳氮磺吡啶、美沙拉秦等控制疾病,并定期复查肠镜,但疾病控制情况欠佳。1%~4%的UC患者在病程中会出现胆汁性肝硬化,早期多无症状或出现乏力,实验室检查结果显示ALP升高,晚期可出现黄疸、肝脾肿大和皮肤瘙痒等,MRCP检查可见局限性或弥漫性胆管狭窄,典型者可呈现"串珠样"改变;活检可见累及肝内外胆管的纤维化改变,该患者虽有UC病史,以及乏力、黄疸和ALP升高等表现,但MRCP和活检均不支持UC合并硬化性胆管炎的诊断。
研究报道,0.53%的IBD后期可发展为淀粉样变性,CD的比例更高,可达1.05%,而UC的比例仅0.08%;IBD所致的淀粉样变性以男性居多,男女比为2∶1。从IBD进展为淀粉样变性需要经过数年的时间,诱发因素尚不清楚。该患者有长期的UC病史且控制不佳,存在UC继发淀粉样变性的可能。淀粉样变性本身可以累及胃肠道,但胃肠镜和影像学常无特异性表现,确诊需行组织活检。患者本次入院后一般情况差,无法耐受胃肠镜检查,故无法证实有无淀粉样变性的胃肠道累及。
结语
淀粉样变性患者最常见的死因为肾衰竭、限制性心肌病或缺血性心脏病。淀粉样变性所致的器官沉积主要集中于肾脏、心脏和肝脏。肾脏受累最常表现为无症状性蛋白尿或明显的肾病综合征,但主要沉积可局限在血管或肾小管,这类患者通常表现为少尿或无尿的肾衰竭。心脏受累可导致心脏收缩或舒张功能障碍,最常表现为心力衰竭,以呼吸困难和水肿为特征。继发性淀粉样变性的患者心脏受累时,预后极差,其中位生存期明显短于老年型系统淀粉样变性患者。胃肠道受累表现为肝肿大,可伴或不伴脾肿大,其他胃肠道表现包括出血、胃轻瘫、便秘,以及由动力障碍导致的假性肠梗阻。淀粉样变性累及肝脏常预后不佳,可能提示患者有相对重度的全身性疾病。有研究纳入98例肝淀粉样变性患者,结果显示中位生存期为9个月。淀粉样变性生存期缩短的独立预测指标包括心力衰竭、TBil水平>34.2 μmol/L和血小板计数>500×109/L。
综上所述,临床工作中不能忽视少见疾病如淀粉样变性引起腹水的可能性,必要时需行肝穿刺明确病理诊断。淀粉样变性是一种少见疾病,根据病因分为原发性、继发性、遗传性、老年型、孤立型和透析相关型。淀粉样变性可造成多器官受累,并出现相应的症状和体征;最常累及的器官为肾脏,当出现肝脏累及时,预后常不良。在治疗方面,针对原发性淀粉样变性可采用化学治疗或自体干细胞移植等;继发性淀粉样变性常采用针对原发病的治疗措施;当患者出现相应器官衰竭时,可采用器官移植的方法。临床上需注意UC和淀粉样变性同时存在的可能性,对于此类患者需要积极行分型鉴定,明确淀粉样变性是原发性还是继发性。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#淀粉样变#
60
#淀粉样变性#
0
#变性#
46