ASCO 2020 来了:前列腺癌领域重磅研究盘点
2020-06-01 MedSci原创 MedSci原创
2020年美国临床肿瘤学会(ASCO)年会终于跟随着时代的潮流“上线”了。今年虽然没有了线下集会的盛景,但层出不穷的各类研究依然热闹非凡。
2020年美国临床肿瘤学会(ASCO)年会终于跟随着时代的潮流“上线”了。今年虽然没有了线下集会的盛景,但层出不穷的各类研究依然热闹非凡。今天来看下前列腺癌领域有哪些重磅研究吧!
首先让我们先来看看多家大药企公布的新药III期临床研究的总体生存率结果。
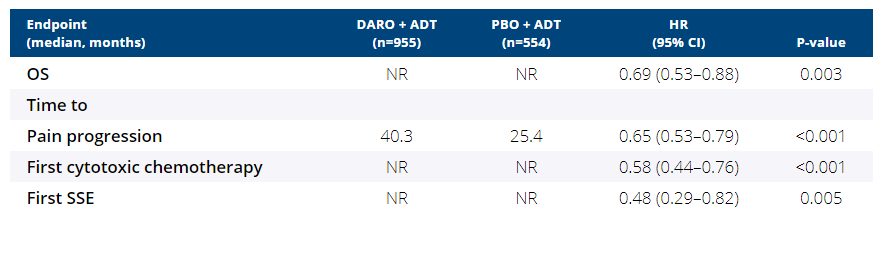
一、雄激素去势疗法(ADT)联合达洛鲁胺(Darolutamide)治疗非转移性去势抵抗性前列腺癌(nmCRPC)的ARAMIS III期的总体生存率(OS)结果。(摘要号:2788)
来自拜耳的药物达洛鲁胺是一种雄激素受体拮抗剂,此前已经获得FDA批准用于治疗非转移性去势抵抗性前列腺癌。在ARAMIS III期临床试验中,与安慰剂相比,达洛鲁胺显著延长了患者的无转移生存期(中位时间分别为40.4个月和18.4个月)。此次大会的报告公布了总体生存率结果和其他次要终点,以及更新的安全性结果。
ARAMIS(NCT02200614)是一项基于一项多中心、双盲、安慰剂对照临床试验,共纳入1509例非转移性去势抵抗性前列腺癌患者。患者随机分为两组,试验组共955例患者,服用达洛鲁胺600mg/次、2次/天,而安慰剂组共554例患者,患者均同时接受雄激素去势治疗。在最初的双盲分析后,有170位患者从安慰剂组转移至了达洛鲁胺组。
试验在观察到254例死亡后(包括15.5%的达洛鲁胺组患者和19.1%的安慰剂组患者)进行了最终分析。达洛鲁胺在总体生存率方面显示出统计学上显著的优势,与安慰剂组相比死亡风险降低了31%。发生率超过5%的治疗紧急不良反应也被作了比较,与初步分析时所得出的安全性结果相似。暴露剂量调整后,不良反应的发生率(包括跌倒、CNS效应和高血压)没有增加。交叉组的不良反应发生情况与达洛鲁胺组相仿。研究人员最后得出结论,表示
对于非转移性去势抵抗性前列腺癌患者,达洛鲁胺在总体生存率方面在统计学上显著更好。此外,与安慰剂相比,达洛鲁胺可延迟癌症相关症状的发作和后续化疗。随着随访时间的延长,其安全性和耐受性良好,并与ARAMIS试验的主要分析结果一致。
二、SPARTAN试验的最终生存结果:阿帕他胺(Apalutamide)对比安慰剂针对非转移性去势抵抗性前列腺癌(nmCRPC)患者的III期临床研究。(摘要号:3339)
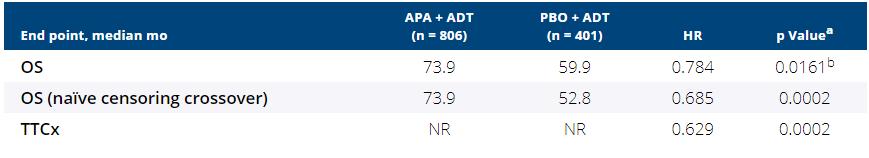
阿帕他胺是一种此前已获FDA批准上市用于前列腺癌的口服雄激素抑制剂,此次ASCO会议上公布了阿帕他胺关键III期SPARTAN研究的最终分析数据。
SPARTAN(NCT01946204)是一项全球多中心、随机、双盲、安慰剂对照、注册III期临床试验,共入组1207例非转移性去势抵抗性前列腺癌患者。这些患者接受持续雄激素去势治疗(ADT),但前列腺特异性抗原水平翻倍耗时不足10个月。研究评估了阿帕他胺联合 ADT 的疗效和安全性,并与安慰剂联合 ADT 进行了对比。研究中,患者随机分配至两组,接受每日一次口服阿帕他胺(240 mg)治疗(N=806)或接受安慰剂每日一次治疗(N=401),同时维持ADT治疗。根据之前公布的数据,研究达到了无转移生存期(MFS)主要终点:与安慰剂+ ADT组相比,APA联合ADT组中位MFS显著延长了2年、发生远处转移或死亡风险显著降低了72%。
而此次公布的数据包括以下内容。在52个月的随访后,共计有428个总体生存率相关事件。中位治疗时间分别为:APA组32.9个月,安慰剂组11.5个月。APA + ADT组相对于安慰剂联合ADT的中位总体生存率多出14个月(73.9 vs 59.9 个月),这个数字在有19%的患者转组交叉后扩大至21个月。APA 组和安慰剂组由于进行性疾病导致的停药发生率分别为42.7%与73.9%,而由于不良事件(AE)导致的停药发生率分别为15.2%与8.4%。安全性与先前的分析一致。令人特别关注的3/4级紧急治疗不良反应的情况为:皮疹5.2%、骨折4.9%、跌倒2.7%、缺血性心脏病2.6%、甲状腺功能减退0%和癫痫发作0%。1例患者发生心肌梗塞的不良反应死亡,可能与APA相关。
三、PROSPER研究的最终总体生存期(OS):一项针对非转移性去势抵抗性前列腺癌(nmCRPC)的恩杂鲁胺(ENZA)的III期、随机、双盲、安慰剂对照研究(NCT02003924)。
恩杂鲁胺为雄激素受体抑制剂,可竞争性地抑制雄激素与受体的结合,并且能抑制雄激素受体的核转运以及该受体与DNA 的相互作用。[a] PROSPER研究已证明了前列腺特异性抗原迅速升高的非转移性去势抵抗性前列腺癌患者使用恩杂鲁胺后的无转移生存率(MFS)在统计学显著改善并具有临床意义。
首次报道时,最终总体生存率数据尚不完备,在ASCO 2020 上研究者们又公布了最终的数据。与安慰剂相比,恩杂鲁胺治疗在统计学上使死亡风险降低了27%,表明在可检测到的转移发生之前进行恩杂鲁胺联合ADT治疗可改善CRPC和PSA迅速升高的男性的总体生存率。安全性与先前的临床试验一致。PROSPER研究的最终总体生存率分析为将无转移生存率作为非转移性去势抵抗性前列腺癌中总体生存率的潜在替代终点提供了前瞻性验证,并支持继续使用恩杂鲁胺联合 ADT作为非转移性去势抵抗性前列腺癌且PSA迅速上升患者的治疗标准。
除了这些补充了重要数据的热门药物,研发中的新药表现也可圈可点,不少用于其他内分泌的疾病都被开发出了在前列腺癌方面的治疗潜力。
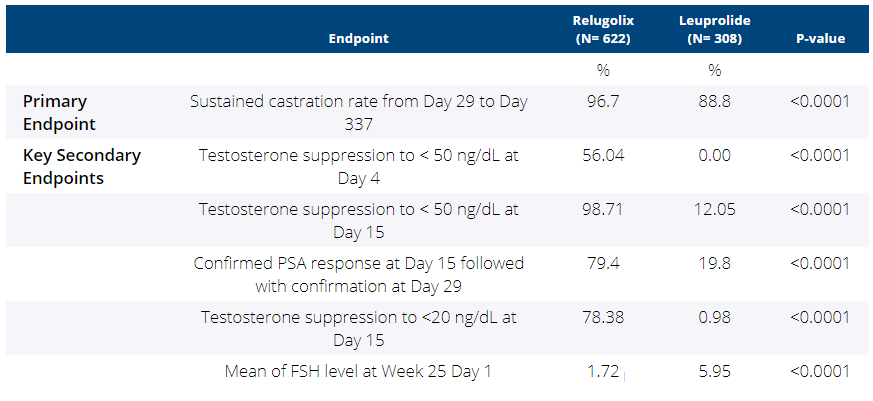
四、HERO III期临床试验:口服Relugolix(一种口服GnRH受体拮抗剂)与醋酸亮丙瑞林治疗晚期前列腺癌的结果比较。(NCT03085095)(摘要号:2969)
Relugolix 是一种促性腺激素释放激素(GnRH)受体拮抗剂,由于能够迅速降低女性雌激素和孕激素,于去年在日本获批用于治疗子宫肌瘤。而由于其在内分泌方面的作用,研究者们尝试将其用于治疗前列腺癌。
LHRH(促黄体激素释放激素,GnRH的别名)激动剂是晚期前列腺癌药物去势的主要手段。但是,它们会导致最初睾酮激增,去势发作延迟,且需要进行长效注射。Relugolix是首个口服GnRH受体拮抗剂,先前已被证明可以迅速抑制睾酮水平。
HERO是一项为期48周的全球关键的III期临床试验,比较了Relugolix和醋酸亮丙瑞林在晚期前列腺癌患者中的安全性和有效性。试验共入组934例雄激素敏感性晚期前列腺癌患者1:1随机分配,分别接受Relugolix 120 mg口服每日一次或大剂量注射醋酸亮丙瑞林3个月。此次发布的研究结果显示,Relugolix 在第4天和第15天时的去势率均优于醋酸亮丙瑞林,并且在持续48周的持续睾酮抑制方面也展现出了优势,且停药后睾酮恢复更快。接受Relugolix治疗的患者中,有96.7%的患者达到并维持了去势,亮丙瑞林组则为88.8%。在睾酮恢复亚组中,停药后90天,Relugolix的中位睾酮水平为270.76 ng/dL,而亮丙瑞林组的中位睾酮水平为12.26 ng/dL。此外心血管不良事件的发生也降低了50%。因此,Relugolix有望成为晚期前列腺癌患者睾酮抑制的新标准。
五、TALAPRO-2:他拉唑帕尼(TALA)联合恩杂鲁胺(ENZA)的安慰剂对照III期研究,用于一线转移性去势抵抗性前列腺癌(mCRPC)患者。(NCT03395197)(摘要号:4555)
近年来PARP抑制剂频频走入人们视线,但大家对它的印象更多是在治疗乳腺癌和卵巢癌方面。来自辉瑞的他拉唑帕尼作为PARP抑制剂最初获批的适应症也是乳腺癌,但现在,研究人员开始谋求拓展它的治疗范围,尝试将其用于前列腺癌的治疗。PARP抑制剂针对前列腺癌治疗的研究并非没有先例,今年,NEJM刊登了一项研究称同为PARP抑制剂的药物奥拉帕利(Olaparib)在某些晚期前列腺癌患者身上的效果比靶向激素治疗药物阿比特龙和恩扎鲁他胺更有效地阻止了前列腺癌的生长,且这种药物几乎没有化疗副作用。[6] 就在五月,阿斯利康和默沙东刚刚联合宣布奥拉帕利获FDA批准用于治疗携带同源重组修复(HRR)基因突变的转移性去势抵抗性前列腺癌患者。
在这样的激烈竞争之下,辉瑞也不甘示弱。在ASCO发布的这项 III 期临床研究,计划在多个地区招募1037例患者(19例进行第1部分剂量确定;1,018例进行第2部分安慰剂对照)。关键资格标准:年龄≥18岁;无症状/轻度有症状的转移性去势抵抗性前列腺癌;ECOG评分≤1;转移性疾病(无脑转移);未接受过针对非转移性CRPC或转移性去势抵抗性前列腺癌的延续生命的系统性疗法。允许先前接受过去势敏感性治疗(不包括新型雄激素受体抑制剂)。 ADT必须在整个研究过程中继续进行。随机双盲部分(第2部分)将评估他拉唑帕尼(0.5 mg 每日)联合恩杂鲁胺(160 mg 每日)与安慰剂联合恩杂鲁胺(160 mg 每日)的安全性、疗效和患者报告结局。主要终点为放射学无进展生存期(rPFS)。
以上就是ASCO 2020大会上有关前列腺癌新资讯的部分内容,更多有关ASCO大会的精彩资讯,欢迎继续关注我们的后续推送!
[1] https://meetinglibrary.asco.org/record/187482
[2] MICHAEL E,SAMEDY O,DONGWON Y,et al. Structure-activity relationship for thiohydantoin androgen receptor antagonists for castration-resistant prostate cancer (CRPC) [J]. J Med Chem,2010, 53(7) : 2779-2796.
[3]https://meetinglibrary.asco.org/record/187437
[4] Eric Jay Small et al., SPARTAN, a phase 3 double-blind, randomized study of apalutamide (APA) versus placebo (PBO) in patients (pts) with nonmetastatic castration-resistant prostate cancer (nmCRPC). Journal of Clinical Oncology, Volume 36, Issue 6
[5]https://meetinglibrary.asco.org/record/187453
[6]https://mp.weixin.qq.com/s/7G6I-kGUhuiXsjzlBvxiBg
[7]https://meetinglibrary.asco.org/record/191602
[8]https://meetinglibrary.asco.org/record/191880
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










好东西
103
#ASC#
89
#ASCO 2020#
77
#重磅#
80
学习中👍👍
146
前列腺癌相关研究,学习了,谢谢梅斯
87