JCI:彭宏凌/傅征/单强/黄伟姗团队揭示如何在CAR-T细胞治疗中延长CAR-T细胞的体内存活时间,并降低肿瘤复发率
2024-12-02 iNature iNature 发表于陕西省
该研究发现,IL-2诱导T细胞激酶(ITK)可以作为基因敲除或抑制的靶点,通过敲除或抑制ITK,促进CAR-T细胞的体内存活,从而更有效地控制肿瘤复发。
近日,中南大学湘雅二医院彭宏凌教授、傅征博士、北京协和医院苏州系统医学研究所单强研究员、路易斯安那州立大学黄伟姗研究员,以及镁伽科技等团队在医学权威期刊《临床研究杂志》(Journal of Clinical Investigation)上发表了一项创新性研究成果——“IL-2-inducible T cell kinase deficiency sustains chimeric antigen receptor T cell therapy against tumor cells”。该研究发现,IL-2诱导T细胞激酶(ITK)可以作为基因敲除或抑制的靶点,通过敲除或抑制ITK,促进CAR-T细胞的体内存活,从而更有效地控制肿瘤复发。此项研究为开发更具持久性的CAR-T细胞疗法提供了新的潜在策略。

嵌合抗原受体T细胞疗法(CAR-T)作为一种突破性的细胞免疫疗法,已广泛应用于治疗白血病等多种癌症。目前,已有10种CAR-T产品获得临床治疗批准。尽管CAR-T疗法在白血病治疗中取得了显著疗效,但其在临床实践中仍面临诸多挑战,尤其是肿瘤复发问题。肿瘤微环境中T细胞的衰竭及CAR-T细胞在体内的短暂存活是影响疗效的主要障碍之一。
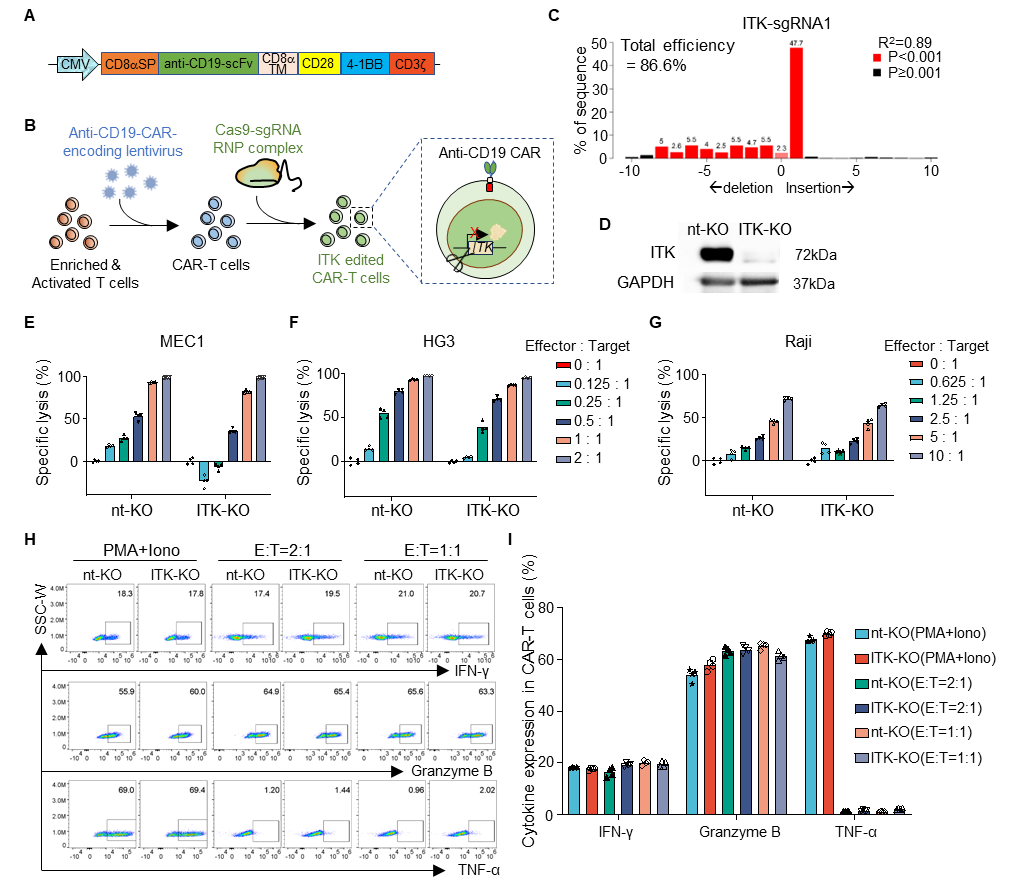
图1. CRISPR/Cas9基因编辑技术敲除ITK轻微地影响了CD19-CAR-T细胞的体外杀伤能力
ITK(IL-2诱导T细胞激酶)主要在T细胞中表达,是T细胞受体(TCR)信号通路下游的关键调节因子,负责调控TCR信号的强度,进而影响T细胞的活化和分化。慢性TCR活化会导致T细胞衰竭,而通过抑制或敲除ITK,可以有效减缓T细胞衰竭,已在小鼠模型中获得成功。然而,ITK在CAR-T细胞抗肿瘤活性中的作用尚未完全阐明。
在本研究中,研究团队结合CRISPR/Cas9基因编辑技术及多种体外和体内CAR-T细胞治疗模型,深入探讨了ITK缺失在CD19-CAR-T细胞中的功能和作用机制。研究发现,ITK缺失不仅不影响CAR-T细胞的体外杀伤功能(图1),还显著提高了CAR-T细胞的长期存活(图2),减少了细胞凋亡,并增强了增殖能力。
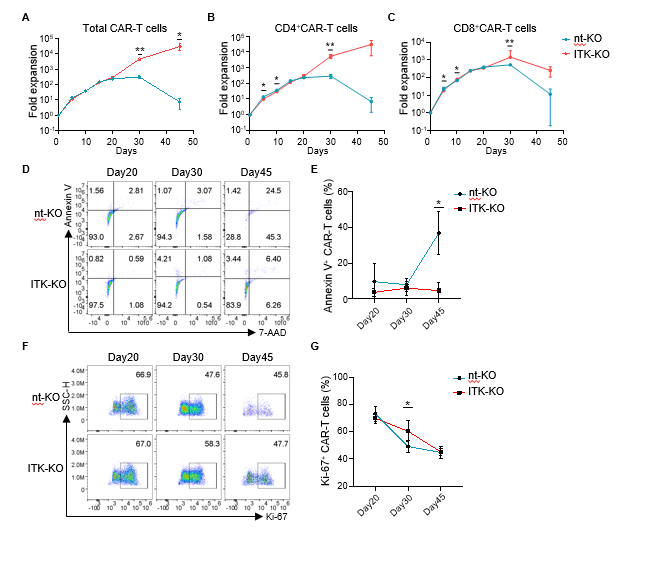
图2. ITK缺失促进了CD19-CAR-T细胞在体外的长期扩增。
T细胞在被激活和快速扩增之后,会进入一个急剧收缩的阶段(contraction phage)。研究团队发现,ITK缺失之后的CAR-T细胞的仍能在体外显著存活更长时间(图2)。进一步的研究结果表明,ITK缺失后的CAR-T细胞的长期凋亡减少,而增殖能力较野生型的CAR-T细胞更强(图2)。
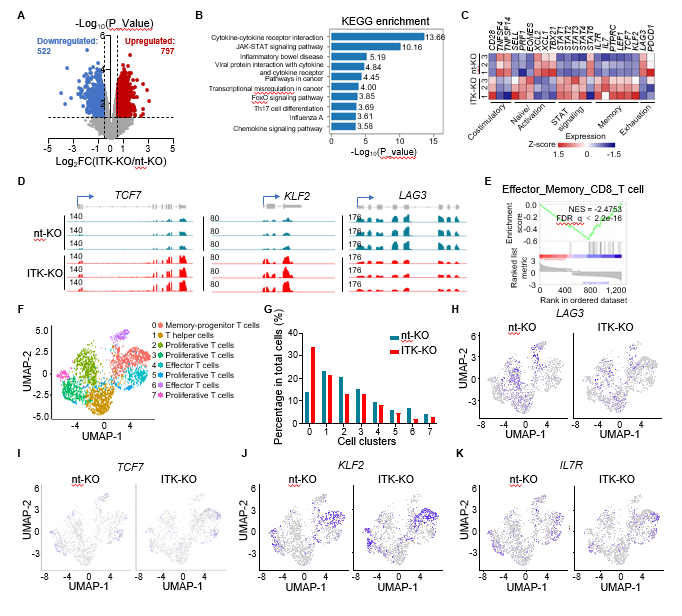
图3. Bulk RNA测序和单细胞测序揭示ITK对CAR-T细胞在转录水平的调控作用。
进一步的研究表明,ITK敲除后的CAR-T细胞在转录水平上发生了显著变化。Bulk RNA测序和单细胞测序显示,ITK敲除可显著降低T细胞衰竭相关分子(如LAG-3)的表达,并增强T细胞记忆相关分子的表达(如TCF7、KLF2、CD127等)(图3)。这些结果表明,ITK敲除可以减少CAR-T细胞的耗竭,促进记忆型CAR-T细胞的产生。
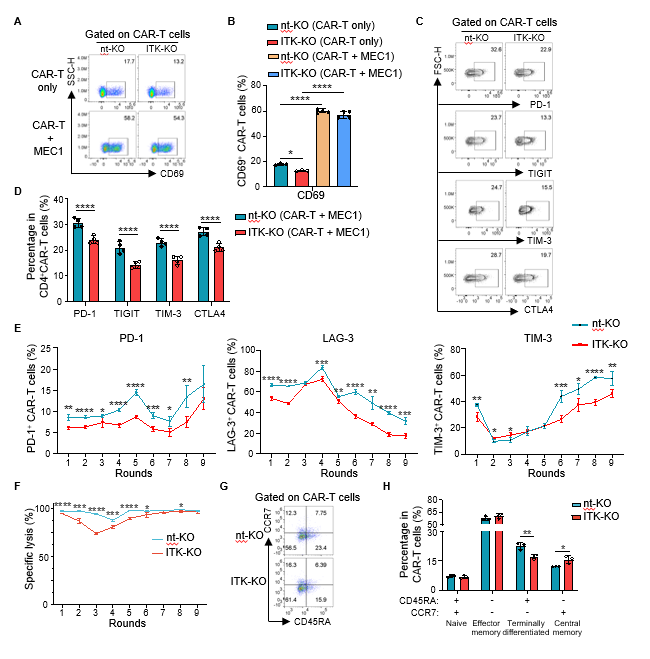
图4. 体外实验表明ITK敲除可以降低CAR-T细胞耗竭以及促进T细胞记忆。
体外实验表明,ITK敲除可以显著降低CAR-T细胞中耗竭分子的表达,并且促进记忆型CAR-T细胞的形成(图4)。
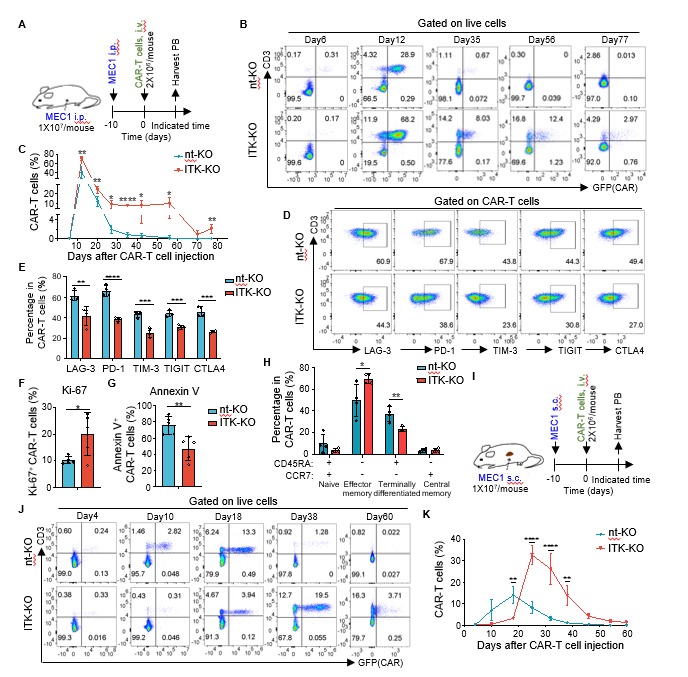
图5. MEC1慢性淋巴性白血病动物实验表明ITK敲除可增强CD19-CAR-T细胞在体内的扩增和长期持久性。
在体内动物肿瘤模型的实验中,研究团队进一步验证了ITK缺失对正常人来源的T细胞制备的CAR-T细胞存活和抗肿瘤效果的影响。在慢性淋巴性白血病(MEC1)模型中,ITK敲除的CAR-T细胞表现出更少的衰竭细胞和更多的记忆细胞,并能有效清除肿瘤(图5)。这些结果表明,ITK缺失有助于降低CAR-T细胞衰竭,并增强其在体内的存活和长期抗肿瘤活性。
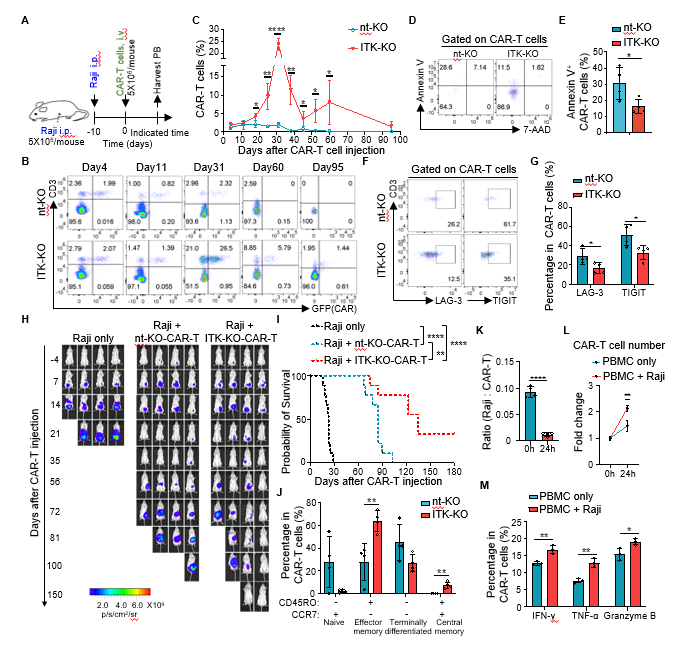
图6. Raji急性淋巴性白血病动物实验表明ITK敲除后CAR-T细胞可以更好控制肿瘤的复发。
在急性淋巴性白血病(Raji)模型中,ITK敲除的CAR-T细胞不仅能够更好地控制肿瘤复发,还显著提高了小鼠的生存率(图6)。这些实验结果表明,ITK缺失显著延长了CAR-T细胞的体内存活时间,进一步降低了肿瘤复发的风险。
此外,研究团队还在慢性淋巴性白血病患者来源的T细胞中验证了ITK抑制的效果。结果发现,ITK抑制不仅可以减少患者来源T细胞的衰竭,还能促进CAR-T细胞记忆功能的增强(图7)。在进一步的实验中,研究团队将慢性淋巴性白血病患者来源的T细胞进行ITK敲除,并注射到MEC1慢淋肿瘤动物模型中。结果显示,野生型慢淋患者T细胞制备的CAR-T细胞未能长期有效地控制MEC1肿瘤,而ITK敲除的患者T细胞制备的CAR-T细胞则能更好地、持续地控制肿瘤,并显著改善小鼠的长期生存率。ITK缺失的CD19-CAR-T细胞在控制肿瘤复发方面表现出色,进一步实现了更持久的治疗效果。
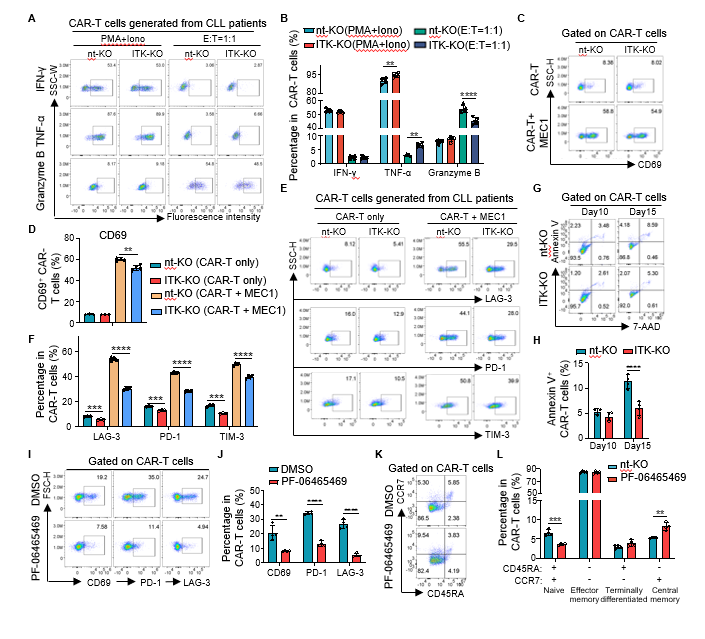
图7. 来源于慢性淋巴性白血病(CLL)患者的CD19-CAR-T细胞中,ITK缺失减轻了衰竭并促进了记忆表型的形成(体外实验)。
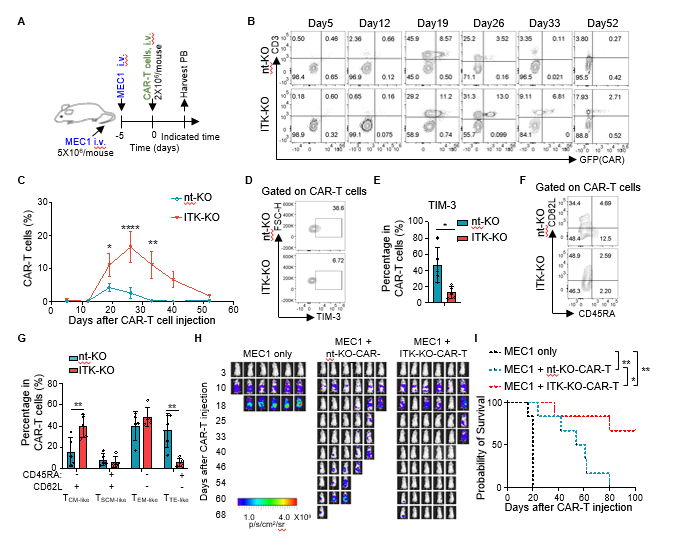
图8. 来源于慢性淋巴性白血病(CLL)患者的ITK缺失CAR-T细胞改善了体内对肿瘤复发的控制(体内动物实验)。
综上所述,ITK的敲除或抑制可以显著减少CAR-T细胞的衰竭,促进记忆性CAR-T细胞的形成,从而延长CAR-T细胞在体内的存活时间,并最终提高肿瘤治疗效果。
该研究表明,ITK敲除作为CAR-T细胞生产中的一种潜在策略,有助于开发更持久、更具功能性的CAR-T细胞疗法。这一策略尤其有望改善T细胞功能较差的患者以及肿瘤复发患者的治疗效果。
该研究的通讯作者为中南大学湘雅二医院彭宏凌教授、傅征博士、北京协和医院苏州系统医学研究所单强研究员和路易斯安那州立大学黄伟姗研究员。傅征博士、黄自能博士和徐浩博士为该研究的共同第一作者。
论文链接:
https://www.jci.org/articles/view/178558
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#CAR-T细胞# #IL-2诱导T细胞激酶#
15