拜耳CKD药物Kerendia获得欧盟批准
2022-02-28 Allan MedSci原创
拜耳近日宣布,欧盟监管机构已批准 Kerendia (finerenone) 用于治疗患有与 2 型糖尿病相关的慢性肾病(CKD)的成年患者。
拜耳近日宣布,欧盟监管机构已批准 Kerendia (finerenone) 用于治疗患有与 2 型糖尿病相关的慢性肾病(CKD)的成年患者。该决定是在欧洲药品管理局(EMA)人用药品委员会的积极意见之后作出的。
拜耳制药部门医疗事务和药物警戒负责人 Michael Devoy 表示:“欧盟对 Kerendia 的批准为医生提供了一条新途径,通过降低心血管 (CV) 事件的风险和延缓肾脏疾病进展来保护这些易受伤害的患者”。Kerendia 的作用是阻断盐皮质激素受体的过度激活,这种过度激活被认为会导致 CKD 进展和 CV 损伤。
这项批准得到了 III 期 FIDELIO-DKD 试验数据的支持,该试验将 Kerendia 与安慰剂进行了比较,将其添加到约 5700 例患有 2 型糖尿病的 CKD 患者的标准护理中。结果显示,Kerendia 组中肾功能衰竭或肾死亡风险显著降低。
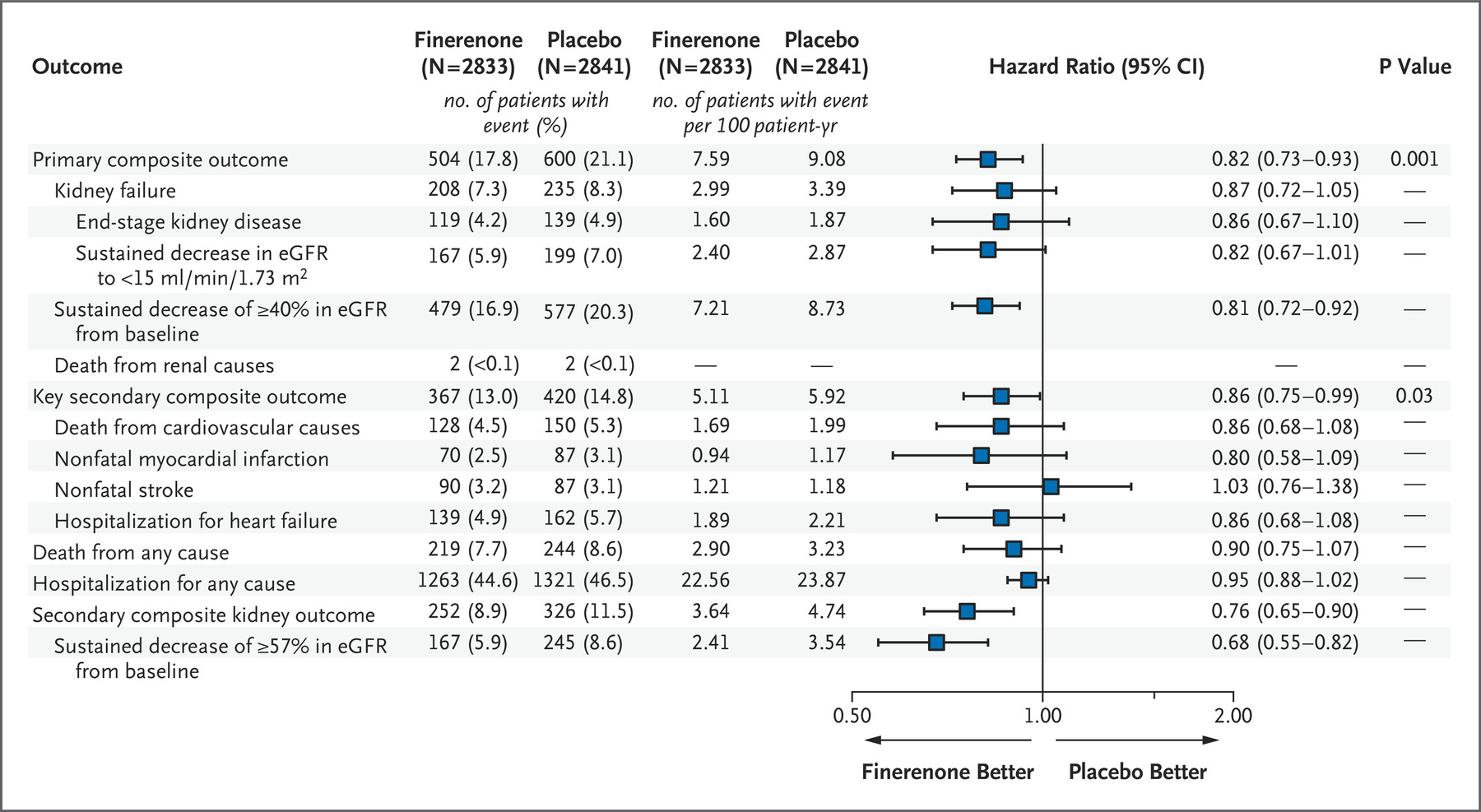
该药物还在 2 型糖尿病相关 CKD 患者的 III 期 FIGARO-DKD 研究中取得成功。去年公布的详细研究结果表明,在 3.4 年的中位随访期间,当加入 ACE 抑制剂或血管紧张素受体阻滞剂时,Kerendia 将复合主要终点(即首次发生 CV 死亡或非致命性 CV 事件的时间)的风险显著降低了 13%。拜耳指出,其治疗方法也已在中国和其他国家提交上市许可,申请正在审查中。
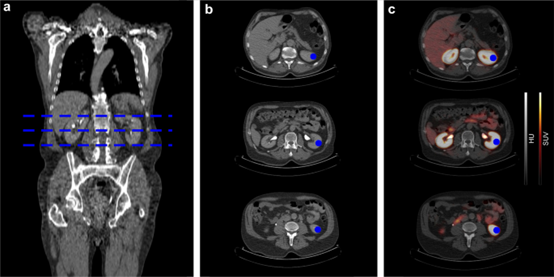
糖尿病肾脏病(DKD)是糖尿病患者的常见慢性并发症之一,是指由糖尿病引起的慢性肾脏病(CKD),表现为尿蛋白水平升高(尿白蛋白肌酐比值≥30 mg/g)和(或)估算肾小球滤过率(eGFR)<60 ml/min/1.73 m2并持续超过3个月,同时排除其他病因CKD而作出的临床诊断。
原始出处:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#DIA#
42
#拜耳#
50
#欧盟批准#
50