尿酸转运蛋白的研究进展
2015-01-28 施映枫 徐柳青 严海东 庄守纲 刘娜 中华肾脏病杂志
尿酸是嘌呤化合物代谢的终末产物,嘌呤代谢紊乱可致尿酸水平升高而产生高尿酸血症。临床研究证实,高尿酸血症与糖尿病、高血压以及高脂血症之间存在着紧密相关性,并可诱发炎性反应,加重血管内皮损伤,最终加速冠心病和肾脏损伤的进展。 现已发现多种转运蛋白参与了肾脏近曲小管对尿酸盐的 转运过程。包括尿酸重吸收蛋白:尿酸盐阴离子转运体1(URAT1),有机阴离子转运体4(0AT4)和葡萄糖转运体9(G
尿酸是嘌呤化合物代谢的终末产物,嘌呤代谢紊乱可致尿酸水平升高而产生高尿酸血症。临床研究证实,高尿酸血症与糖尿病、高血压以及高脂血症之间存在着紧密相关性,并可诱发炎性反应,加重血管内皮损伤,最终加速冠心病和肾脏损伤的进展。
现已发现多种转运蛋白参与了肾脏近曲小管对尿酸盐的 转运过程。包括尿酸重吸收蛋白:尿酸盐阴离子转运体1(URAT1),有机阴离子转运体4(0AT4)和葡萄糖转运体9(GLUT9);尿酸分泌蛋白:有 机阴离子转运体(OAT)家族蛋白、尿酸盐转运体(UAT)、多药耐药蛋白4(MRP4)和钠依赖的憐酸转运蛋白(NPTs),以及其他途径的转运蛋白和 辅助蛋白等。
一、高尿酸血症对全身代谢的影响
尿酸在正常人体代谢中由于产生过多或排泄不足而引起血尿酸水平升高,当间隔的两次空腹血尿酸水平高于420umol/L(男)或360umol/L(女)时,被称之为高尿酸血症(hypei.ui.icemia,HUA)。Mazzali等发现血尿酸值与血压升高水平及高血压相对危险度呈明显正相关。
焦喆等研究了高尿酸血症和糖尿病前期之间的关系,证实高尿酸血症能够加重胰岛素抵抗.促使糖尿病Ⅲ期患者进一步发展为糖尿病,同时胰岛素抵抗又促进了血尿酸的生成,加重高尿酸血症。
临床上高尿酸血症也常与心血管疾病伴发。一项人选了26项研究,420997例冠心病患者的Meta分析研究发现,高尿酸血症是冠心病患者发病的独立危险因素。
随着对HUA研究深度和广度的不断加深,人们对于HUA在心血管疾病方面的认识,已从独立危险因素渐渐向多因素相关的预测因子转变。
Wannametheem研究提示HUA对冠心病的作用是基于与其他危险因子如高血压、代谢综合征、高胰岛素血症等的二次关联上发生的,并认为HUA对冠心病的病程、转归及病死率有重要的预测价值。
综上,均提示高尿酸血症在冠心病的发生和发展中可能起到推波助澜的作用。此外,一项人选了16项研究238449例中风患者的Meta分析研究发现, 高尿酸血症增加患者中风的发生率。这说明除心血管疾病外,高尿酸血症与严重危害人类生存的脑血管疾病发生也存在关联性。
除了心脑血管疾病外,高尿酸血症还和肾脏疾病密切相关。我们课题组在高尿酸血症大鼠模型中证实了血尿酸水平升高可加速大鼠的肾脏损害,肾脏病理显示明 显的肾小管肥大、扩张,肾间质炎性细胞浸润,血肌酐明显升高在一项RCT研究中,随访对象为美国肾病数据库系统的177570例患者,随访时间长达25 年。
研究发现,血尿酸水平增高的患者发生慢性肾脏病(chronickidneydisease,CKD)的风险是尿酸正常患者的2.14倍。同样,在人群动脉粥样硬化危险性试验中发现,血尿酸每增长59.5umol/L,CKD发生的风险增加7%~11%。
Liu等的一项新近研究中,选取了788例接受了冠脉造影但肾功能正常的受试患者,将其分成高尿酸血症组和血尿酸正常范围组,研究表明高尿酸血症组是患者发生急性肾损伤的高危因素.并且多部分患者需要肾脏替代治疗。
血尿酸浓度升高刺激肾小管内尿酸盐结晶的析出,造成相应肾小管的栓塞和破裂.加之尿酸盐结晶本身所引起的炎性反应,共同加剧了肾功能的进展。而肾功能的下降会进一步降低尿酸的排泄,结晶沉积和炎性反应程度进一步加重,最终加速肾脏病的进程。
我们课题组在细胞表型转化方面做了部分工作,肾小管上皮细胞表型转化,表达a平滑肌肌动蛋白(a-smoothmuscleactin,a-SMA),产生大量细胞外基质成分,堆积在肾脏间质,是肾间质纤维化的重要发生机制。
研究显示,高尿酸血症肾损害大鼠模型中,a-SMA表达显著上调,E-cadherin蛋白表达显著下调;别嘌醇处理的尿酸性肾病大鼠,肾小管上皮细胞转分化标志物a-SMA表达显著下调,E-cadherin蛋白表达下调;在体外培养的肾小管上皮细胞中,尿酸刺激肾小管上皮细胞转分化,尿酸转运蛋白抑制剂可抑制尿酸刺激的肾小管上皮细胞转分化。
证实高尿酸血症可能通过诱导肾小管上皮细胞表型转化,促进肾间质纤维化的进展。
二、尿酸转运蛋白分类
由于尿酸酶基因的沉默,导致人类无法将尿酸分解为溶解度更高的尿囊素,导致尿酸生成过多或排泄下降的患者出现高尿酸血症。
已知尿酸的代谢过程包括滤过-重吸收-分泌-分泌后重吸收四个步骤,除了滤过不需要转运蛋白参与外,其余尿酸代谢过程均需要尿酸转运蛋白发挥作用,因此将尿酸转运蛋白分为重吸收蛋白和分泌蛋白两大类。
尿酸重吸收蛋白包括:尿酸盐阴离子转运体1(URAT1);葡萄糖转运蛋白9(GLUT9);有机阴离子转运体(OAT)家族蛋白中的0AT4。
尿酸分泌蛋ft包括:位于基底外侧膜的0AT1和0AT3,以及位于管状上皮细胞顶膜的尿酸盐转运子(UAT);多药耐药蛋白4(MRP4)和憐酸盐转运蛋白(NPT1/NPT4)。
此外还存在其他途径的尿酸转运蛋ft,例如ABC转运蛋内2(ABCG2)和转运体支架蛋白(PDZKl)。这些转运蛋A的表达过量或不足,均能影响正常尿酸转运途径.造成血清尿酸浓度的异常,从而引起高尿酸血症及其他相关的全身疾病。
三、尿酸转运蛋白结构与功能研究
1.尿酸重吸收蛋A:
(1)尿酸盐阴离子转运体1(URAT1):2002年R本学者Enomoto等首次发现了在肾皮质近曲小哲上皮细胞哲腔膜侧大量表达尿酸盐阴离子转运体1,并检测到该蛋A在近曲小哲内重吸收尿酸的量高达50%左右。
URAT1属于有机阴离子转运体(0AT)家族,SLC22A12基因编码的URAT1定位于染色体llql3,包含10个外显子和9个内含子,是由 555个氨基酸残基12个跨膜结构域以及-NH2和-C00H组成的完整跨膜蛋白,其cDNA全长2642bp,编码区1659bp,其氨基酸序列与 0AT4有42%的同源性。
URAT1通过介导管腔内的尿酸与近曲小管上皮细胞内无机阴离子(Cl-)、有机阴离子(乳酸盐和盐酸盐)的交换从而将尿酸从管腔内重吸收至上皮细胞内,重吸收作用依赖于管腔两侧的浓度梯度和电化学梯度。
URAT1基因突变会影响尿酸的重吸收过程,造成血尿酸水平的异常。Shima等和Guan等分别在日木和中国的受试者中,证实了SLC22A12中的rs893006多态性与高尿酸血症密切相关,而G774A的突变又会导致原发性低尿酸血症。
因此,Enomoto等提出无论是原发性高尿酸血症还是高尿酸合并肾脏损害,其患者的URAT1基因都存在突变现象,这更有力的说明了URAT1参与了尿酸的重吸收过程。
URAT1对于底物的选择特异性,使其成为临床药物的新靶点,如苯溴马隆、丙磺舒、苯磺唑酮、氯沙坦和非诺贝特作为URAT1的抑制剂,可降低血尿酸水平。
最新研究发现,乙酰水杨酸与URAT1转运存在剂量依赖性,高剂量乙酰水杨酸(&150mg/L)可抑制尿酸的重吸收,而低剂量(50~100mg/L)可抑制其排泄,这种现象被研究者称为乙酰水杨酸在尿酸排泄上的双重效应。
(2)葡萄糖转运蛋白9(GLUT9):GLUT9又名电势驱动尿酸转运蛋白1(URATvl),属于葡萄糖转运家族。编码基因SLC2A9位于4pl5.3-pl6染色体上,含有14个外显子,其中包括1个非编码子和3个编码子。
GLUT9由12个跨膜螺旋环和位于细胞膜胞质面的氨基末端及羧基末端组成。由于氨基末端的差异性,又将GLUT9分为2个亚型,分别是表达于基底膜 的GLUT9a和表达于细胞膜的GLUT%,也有研究者将他们命名为剪接变异体(异构体),即长型异构体(GLUT9L)和短型异构体(GLUT9S)。
Caulfield等在爪蟾卵母细胞中转人了两种亚型.发现他们都参与了尿酸重吸收过程。又因为GLUT9是尿酸和葡萄糖的双重转运蛋白,所以糖尿病或高血糖都会竞争性的影响尿酸水平。
众多研究提示,GLUT9基因的突变与血尿酸水平相关。Vitart等研究克罗地亚人基因组,发现SLC2A9对尿酸浓度有1.7%~5.3%的变量 贡献率,在此基础上还发现其贡献率存在男女差异性,分别为女性的5%~6%和男性的1%-2%,并且在爪蟾卵模型中证实了其尿酸转运作用。
李长贵等证实了位于GLUT9基因第一外显子起始点上游1156hp处的rsl3137343多态性会增加中国汉族男性原发性高尿酸血症的发病率。
如今,越来越多的研究者们开始把重心放到了GLUT9相关药物的开发上。例如西药中的丙磺舒,苯溴马隆,氯沙坦等,以及与别嘌呤醇的复合制剂(Nul618)都能减少GLUT9的表达量,从而影响尿酸的重吸收过程。
中药方面,Hu等和胡庆华等分别在氧嗪酸钾盐诱导小鼠产生高尿酸血症模型上发现四妙丸和芒果苷也有类似作用。这些研究为促进GLUT9能作为促尿酸排泄药物的新靶点做出了贡献。
(3)有机阴离子转运体4(0AT4):有机阴离子转运体4(0AT4)属于SLC22A家族,是已发现的机阴离子转运体家族(OATs)中为数不多的介导尿酸重吸收的蛋白。
0AT4由SLC22A11基因编码,其cDNA含有2210个碱基对编码的550个氨基酸残基和12个假定的跨膜区域组成。主要表达于肾小管上皮的刷状缘侧和基底外侧上,通过转运尿酸盐与a-酮戊二酸或羟基离子之间的交换完成重吸收过程。
Hagos等证实,0AT4的尿酸转运作用是通过0H-与尿酸之间的交互完成的,但比URAT1的亲和力要弱。现已发现多种0AT4的内源性底物 (cAMP、cGMP、PGE2)和外源性底物(布美他尼、青霉素、甲氨蝶呤),以及丙磺舒的竞争性抑制作用,但其临床药物作用还有待研究。
2.尿酸分泌蛋白:
(1)有机阴离子转运体家族(OATs):自1997年Sekine与Sweet提取第一个OAT家族成员OAT1起,至今已发现10余种亚型的 OATs,并将其统称为有机阴离子转运体家族,由SLC22A基因编码,其中OAT1、OAT2、OAT3、OAT4、0AT10与尿酸转运有关。
宋必卫等总结指出了OATs共有的特点,即①转运底物范围广,介导包括众多带负电的内源性代谢物(如尿酸、甾体激素、前列腺素等)以及不带电荷的分子和有机阳离子。
②OATs底物分子量较小,一般不超过500000。③介导外源性药物的分泌或重吸收,对药物排泄和药动学有重要意义。④因转运细胞毒性产物而损伤细胞。
OATs的转运机制分为肾近曲小哲上皮细胞基底侧和游离侧两类,在基底侧OATs与有机阴离子结合,逆浓度梯度和电梯度而主动转运进人细胞内,其供能来源于Na+浓度梯度并依赖二羧酸的顺向抑制和反向刺激过程。
最新研究认为0ATS的这一转运过程实际由3种不同的蛋白典同参与完成,称为三级转运模式,即Na7K+-ATP酶;Na7二羧酸协同转运蛋白.以及0A/二羧酸盐交换蛋白而游;的转运机制尚未明确,已知其与单羧酸的交互有关联。
0AT1和0AT3是OATViC族中主要负责尿酸分泌过程的蛋白。0AT1由SLC22A6基因编码,位于染色体llqlS.l,由10个外显子和9个内含子组成。0AT3则由SLC22A8编码,其基因位于1lql1.7,包含12个跨膜结构域。
Eraly等发现0AT1基因敲除的小鼠,其肾小哲分泌尿酸盐的能力明显减弱而Bakhiya等发现0AT3通过有机离子与二羧酸的交换来排泄尿酸,与0AT1的功能相似,两者都提示0AT1和0AT3参与了尿酸的分泌过程。
丙磺舒作为0AT家族的非特异性抑制剂,能与0AT1结合,抑制其底物的转运,但其本身不能被0AT1转运;而丙磺舒在竞争性抑制0AT3的同时还能减少体内青霉素的排泄,这是两者的区别之处。
现阶段,对于0AT家族的研究重心已放到了其表达与调控上研究证实,肝细胞核因子(hepatocytenuclearfactors,HNFs)、 促肾上腺皮质激素、性激素、一氧化氮等在不同程度上参与调控OATs的转录水平,例如:HNF-4a缺失会降低小鼠肝内OAT2mRNA的表达量;垂体切 除的小鼠其rOAT1的表达会随之减少;性激素主要体现在OATs的含量存在性别差异性,以及一氧化氮可下调肝细胞内OAT2的表达。
而在磷酸化调节机制方面,Sauvant等发现蛋白激酶A(PKA)可上调OAT1、OAT3的功能,与此相反的是Miller136提出的蛋白激酶C(PKC)可下调OATs的理论。
最新研究还发现,不同病理状态下的OATs的表达水平也存在差异性,实验性肾损伤时,rOAT1和rOAT3的mRNA和蛋白表达均降低,而实验性肝 损时,OAT3的表达量又呈增长趋势。这些发现在一定程度上都为OATs作为肾脏疾病的靶向药物提供了一定的理论基础。
(2)尿酸盐转运子(UAT):UAT又名生电型的尿酸盐转运蛋白,最早在鼠肾皮质细胞中发现rUAT(rat urate transporter),此后在人体内也证实存在UAT,并和galectins家族具有高度同源性,与galectin9的同源性最高可达96%。
Lipkowitz等证实galectin9即为人尿酸转运蛋白(hUAT)。UAT主要位于近端小管的曲段和升段,包含322个氨基酸、两个跨膜结构域及各自的P-半乳糖苷结合位点组成。
Lealpinto等研究了两个β-半乳糖苷结合位点和α-乳糖、D(+)-葡萄糖之间的关系,发现胞外侧的α-乳糖可增加hUAT的转运能力,而D(+)-葡萄糖可调节hUAT通道的活性。
同时胞质内形成的发夹样结构被证实是尿酸盐的作用位点UAT的编码基因位于17P11.2---17P12之间,含有11个外显子,并拥有5种不同的 异构体,负责肾近端小哲上皮细胞内50%的尿酸盐分泌功能。通过其高度选择性的离子通道,将尿酸盐分泌到哲腔中,再经肾脏排出体外。因此认为UAT是一种 关键性的尿酸分泌蛋白。
(3)多药耐药蛋白4(MRP4):多药耐药蛋白4,来源于ABC(ATP-binding cassette,ABC)家族,由基因ABCC4编码.位于染色体13q32,约350kb,由31个外显子组成。
消耗ATP获得供能将肾小哲上皮细胞内的尿酸分泌人小管腔,因此是一种ATP依赖的尿酸转运蛋白。研究证实,利尿剂能拈抗MRP4介导的转运作用而引起高尿酸血症,相反别嘌呤醇可促进尿酸经MRP4的分泌。
(4)磷酸盐转运蛋白(NPT1/NPT4):NPT又称为钠/磷酸盐协同转运蛋白,主要参与体内尿酸的分泌过程Uchino等研究证实 SLC17A1编码的NPT1是一类位于近曲小哲的电压敏感性离子通道,转运包括对氨基马尿酸盐,利尿药,内源性底物尿酸g内的多种有机阴离子而起到分泌 尿酸的作用,此外,还有SLC17A3编码的NPT4,但其作用机理还尚未明确。
3.其他途径的尿酸转运蛋白:
(1)有机阴离子转运体10(OATIO):OATIO又称为孤对转运蛋白(hoRCTL3),在近曲小管中依靠尿酸离子和谷胱甘肽的交换作用来实现其尿酸转运功能,
少量表达于大脑、心脏及肠道。
编码基因为SLC22A13,位于染色体3p21.3,包含551个氨基酸。研究证实,OAT10介导环孢菌素A的转运,对肾小管产生一定毒性作用,并认为可能与高尿酸血症有关。
(2)ABC转运蛋白2(ABCG2):ABCG2最早在十细胞研究中被发现,证实其与肿瘤多药耐药有关,主要参与肿瘤十细胞多药抗性的形成,但其在 尿酸转运方面的作用也不可忽视。ABCG2蛋白也来源于ABC家族,是一种必须以同型二聚体为活化形式的半转运蛋白。其基因位于4q22~23,编码 655个氨基酸残基,主要表达于近曲小管管腔膜侧。
Wrndward等对14783例试验对象进行全基因组关联研究,发现ABCG2基因C421A位点的单核苷酸多态性与尿酸水平有关。同时非洲爪蟾蜍实验也证实了ABCG2以离子栗的身份参与了尿酸的分泌过程。
(3)转运体支架蛋白(PDZK1):在众多的转运蛋白里,PDZK1是一个比较特殊的辅助蛋白,它并不直接参与尿酸的分泌或重吸收过程,而是通过共表达的方式增加其他蛋白的转运效果。PDZK1由PDZ结构域蛋白1编码,分布于肾脏近曲小管的刷状缘处。
研究证实,PDZK1可在上皮细胞内和URAT1、0AT4、NPT1等产生共表达效应,继而增加转运蛋白的稳定性和活性。最新文献提示,PDZK1 的SNPs和基因突变也会影响尿酸的浓度在人体内发现的过氧化物酶体增生物激活受体-α(PPAR-α)可提高PDZK1的表达量,从而影响高尿酸血症的 代谢途径,但具体调节机制还有待进一步明确。
四、总结和展望
高尿酸血症作为一种多系统累及的疾病,与心血管疾病、代谢综合征及肾脏病变之间存在紧密相关性。尿酸在肾脏中的分泌和重吸收异常是高尿酸血症的发病基础,因此在尿酸四步代谢途径中,尿酸转运蛋白起着至关重要的作用。
在现有的研究中,人们已经基本掌握了几类重要的尿酸转运蛋白以及其作用机制和特点。包括负责重吸收的URAT1和GLUT9,负责分泌的0AT家族和UAT,以及其他几类转运蛋白。见图1。
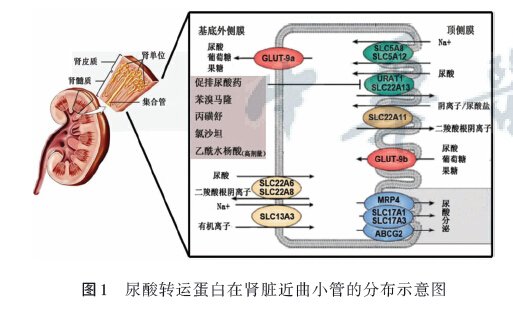
未来的研究方向.将逐渐从对尿酸转运体结构和功能的研究转为对其调控基因的研究。对于这些尿酸转运体细致而深人研究.将为临床高尿酸血症的靶向药物提供重要依据。
中华肾脏病杂志2014年11月第30卷第11期
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








pin、
38
是否能抑制它来改变尿酸排泄
152
#转运#
37
轻度肾脏疾病对母亲和婴儿可能会增加孕期风险
153
现已发现多种转运蛋白参与了肾脏近曲小管对尿酸盐的 转运过程。包括尿酸重吸收蛋白:尿酸盐阴离子转运体1(URAT1),有机阴离子转运体4(0AT4)和葡萄糖转运体9(GLUT9);尿酸分泌蛋白:有 机阴离子转运体(OAT)家族蛋白、尿酸盐转运体(UAT)、多药耐药蛋白4(MRP4)和钠依赖的憐酸转运蛋白(NPTs),以及其他途径的转运蛋白和 辅助蛋白等。
93
#研究进展#
43
尿酸是双面作用
94